
1、(2001·上海)碱金属与卤素所形成的化合物,大都具有的性质是 ( )
①高沸点 ②能溶于水 ③水溶液能导电 ④低熔点 ⑤熔融状态不导电
A.①②③ B.③④⑤
C.①④⑤ D.②③⑤
[解析] 碱金属与卤素所形成的化合物大都是离子化合物,因此具有高沸点、能溶于水、熔融态或水溶液都能导电的性质。
[答案] A
2.碱金属中的一般和特殊之处
(1)Na、K需保存于煤油中,但Li的密度比煤油小,所以Li必须保存在密度更小的石蜡油中或密封于石蜡
(2)碱金属中,从LiàCs,密度呈增大的趋势,但ρ(K)=0.862g/cm3<p(Na)=0.971e/cm3。
(3)酸式盐的溶解度一般大于正盐,但溶解度NaHC03<Na2C03。
(4)氧在化合物中一般显-2价,氢显+1价,但Na2O2 、H202中的氧显-1价,NaH、CaH2中的氢显[-1]价。
(5)试剂瓶中的药品取出后,一般不能放回原瓶,但IA金属Na、K等除外。
(6)一般活泼金属能从盐中置换出不活泼金属,但对IA非常活泼的金属Na、K等除外。如:2Na+CuS04+2H20=Cu(OH)2↓=H2↑+Na2S04。
经典解析
|
名称 |
氢氧化钠 |
氯化钠 |
硫酸钠晶体 |
钠晶体 |
|
化学式 |
NaOH |
NaCl |
Na2SO4·10H2O
|
Na2CO3·10H2O
|
|
俗称 |
苛性钠、火碱、烧碱 |
食盐 |
芒硝 |
苏打、纯碱 |
|
名称 |
碳酸氢钠 |
硫代硫酸钠 |
硅酸钠 |
硝酸钠 |
|
化学式 |
NaHCO3 |
Na2S2O3
·5H2O |
Na2SiO3 |
NaNO3 |
|
俗称 |
小苏打 |
大苏打、海波 |
泡花碱、水溶液叫水玻璃 |
智利硝石 |
重点、难点点拨
1.钠氧化物制取
当钠在氧气中燃烧时,生成的产物是过氧化钠。这是因为氧化钠不稳定,会跟氧气继续起反应,生成过氧化钠。所以工业常用钠在氧气中燃烧制过氧化钠:2Na+O2=Na2O2
氧化钠一般用间接方法来制取,如:
2NaN02+6Na=4Na20+N2↑
通常使用的钾肥:氯化钾、硫酸钾、碳酸钾,由于均易溶于水,在施用时要防止雨水淋失。草木灰中含碳酸钾。
钾肥肥效通常以氧化钾的质量分数表示:
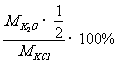
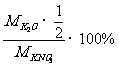
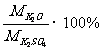
定义:某些金属或它们的化合物在灼烧时使火焰呈特殊的颜色。这在化学上叫做焰色反应。
焰色反应鉴别盐类的步骤:
①铂丝在火焰上灼烧至原火焰色②蘸取溶液(沾取固体)放在火焰上灼烧,观察火焰颜色,观察钾火焰颜色要透过蓝色的钴玻璃去观察。③盐酸洗铂丝④铂丝在火焰上灼烧至原火焰色(如不能灼烧至原火焰色,则需再酸洗,再灼烧)。⑤再蘸取(沾取)另外化学药品进行实验。
钾、钠焰色反应颜色:钾--紫色(透过蓝色钴玻璃)
钠--黄色
2、跟水的反应
碱金属都能跟水反应生成氢氧化物和氢气。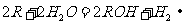 。钠与水反应比锂与水反应激烈,钾跟水的反应比钠更剧烈,常使生成的氢气燃烧并发生轻微爆炸,据此可得出结论:金属单质置换出水中氢越容易说明该元素的金属性越强。因此随着原子的电子层数增多原子半径的增大,碱金属的活动性增强。
。钠与水反应比锂与水反应激烈,钾跟水的反应比钠更剧烈,常使生成的氢气燃烧并发生轻微爆炸,据此可得出结论:金属单质置换出水中氢越容易说明该元素的金属性越强。因此随着原子的电子层数增多原子半径的增大,碱金属的活动性增强。
与常见盐溶液反应的离子方程式:(R表示碱金属元素)

它们都能跟卤素、氧气、硫等非金属直接化合,在反应中表现出很强的还原性。单质都能与水剧烈反应,生成相应的碱和氢气。反应的实质可表示为:
2R+2H20=2ROH+H2↑反应的现象各不相同。与水反应不熔化;钠与水反应时熔化;钾与水反应熔化,且使产生的H2燃烧;铷、铯都与水猛烈反应。碱金属与盐溶液反应,都是先与水反应,若符合复分解反应发生的条件,则生成的氢氧化物继续同盐发生复分解反应。碱金属均不能在水溶液中置换另外的金属单质。
1、跟非金属反应
卤素: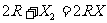
氧气: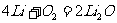

 (K、Rb、Cs与氧气反应,都生成比过氧化物更复杂的氧化物)。
(K、Rb、Cs与氧气反应,都生成比过氧化物更复杂的氧化物)。
氢气:Na、K、Rb、Cs与氢气反应,都生成 RH。
与硫等大多多数的非金属起反应。
4、推论性质递变:随原子核外电子层数的增多原子半径依次增大核对外层电子引力的减弱、失去电子的趋势增强,无素的金属性增强,单质的还原性增强。
3、递变规律:按Li、Na、K、Rb、Cs、顺序,原子半径依次增大,离子半径依次增大。(同种元素的原子半径大于离子半径)。
2、不同点:核外电子层数不同。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com