
15. 现有m g某气体,它由双原子分子构成,它的摩尔质量为M g·mol-1。若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为 mol。
(2)该气体所含原子总数为 个。
(3)该气体在标准状况下的体积为 L。
(4)该气体溶于1 L水中(不考虑反应),其溶液中溶质的质量分数为
(5)该气体溶于水后形成V L溶液,其溶液物质的量浓度为 mol·L-1。
答案:m/M;(2mNA)/M;22.4m/M;100m/(m+1000)%;mV/M
14. 下面是用98%的浓H2SO4(ρ=1.84g/cm3)配制成0.5mol/L的稀H2SO4 500ml的操作,请按要求填空: (1)所需浓H2SO4的体积为 (2)如果实验室有15mL、20mL、50mL量筒,应选用 mL量筒最好。量取时发现量筒不干净,用水洗净后直接量取,所配溶液浓度将 (偏高、偏低、无影响)。 (3)将量取的浓H2SO4沿烧杯内壁慢慢注入盛有约100mL水的 里,并不断搅拌,目的是 。 (4)将 的上述溶液沿 注入 中,并用50mL蒸馏水洗涤烧杯2-3次,洗涤液要 中,并摇匀。 (5)加水至距刻度 处,改用 加水,使溶液的凹液面正好跟刻度相平。
答案:14mL;15mL;偏低;烧杯;防止浓硫酸飞溅;冷却后;玻璃棒;500mL容量瓶;转移到容量瓶;1~2cm;胶头滴管
13. 用NA表示阿伏德罗常数,下列叙述正确的是
A.标准状况下,22.4LH2O含有的分子数为NA
B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA
C.通常状况下, NA 个CO2分子占有的体积为22.4L
D.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA
答案:B
12. 将32 g铜与250mL一定浓度的硝酸反应,铜完全溶解生成硝酸铜,同时产生的NO和NO2混合气体在标准状况下的总体积为11.2L,(假设反应前后溶液体积不变)试计算:
(1)反应后溶液中硝酸铜的物质的量浓度,
(2)反应产生的NO和NO2在标准状况下的体积各为多少。
答案:(1)2mol/L; (2)VNO = VNO2 = 5.6L
11. 有一块锌片投入CuSO4溶液中,过一会儿取出称重,发现质量比原来减少0.1g。试计算:(1)有多少摩尔锌参加了反应?(2)析出多少克铜?
答案:(1)0.1mol(2分); (2)6.4g(3分)
10. 在同温同压下,测得氢气密度为0.089g/L,某种有刺激性气味的气体X的密度为2.848g/L。气体X是三个原子分子并由两种元素组成,两种元素的质量比为1∶1。则气体X的化学式为 。
答案:SO2
9. 9.03×1023个CO2的物质的量是 ,在标准状况下的体积为 L, 质量是 克。
答案: 1.5mol (单位没写扣1分) , 33.6 L, 66 克
8. 下列叙述中正确的是
A、22.4 L氧气中必然含有6.02×1023个氧分子
B、同温同压下,原子数均为6.02×1023个的氢气和氦气具有相同的体积
C、0.50 mol硫酸钠中约含有6.02×1023个钠离子
D、1.0 L浓度为1.0 mol/L的一元酸溶液中含有6.02×1023个氢离子
答案:C
7. 能表示阿伏加德罗常数数值的是( )
A、1 mol金属钠含有的电子数 B、标准状况下,22.4 L四氯化碳所含的分子数
C、1.8 g的NH4+离子中含有的电子数 D、2 g氢气所含原子数目
答案:C
6. 将标准状况下,将V L A气体(摩尔质量为M g·mol -1)溶于0.1 L水中,所得溶液密度为ρ / g·cm-3,则此溶液的物质的量浓度(mol·L-1)为( )
A.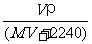 B.
B.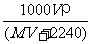
C.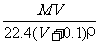 D.100VρM(MV+2240)
D.100VρM(MV+2240)
答案:B
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com