
7.随着互联网的快速发展,越来越多的公民通过网络参与政治生活,以网络为媒介的“政
府-民间”互动模式已成为我国政治文明的重要元素。“政府-民间”互动模式
①方便了公民直接管理国家事务 ②保障了人民群众对政府的质询权
③拓宽了公民参与民主监督的渠道 ④有利于政府了解民意和汇集民督
A.①② B.②③ C.①④ D.③④

6.国家提出,政府机关要实施重大事项社会公示制度。这一制度的实施,是基于公民享有
对涉及公众利益决策的 。
A.决策权 B.知情权 C.监督权 D.表决权
5.政府在决策过程中,通过社会听证制度听取群众意见,其目的是为了
A.以法律保障公民的民主权利 B.了解社情民意
C.集中民智,凝聚民力 D.决策利民
4.《中华人民共和国行政许可法》第46条规定:“涉及公共利益的重大行政许可事项,行政
机关应当向社会公告,并举行听证。”由此可见
A.国家注重保障公民的基本民主权利 B.我国人民直接管理国家事务
C.我国人民当家作主的权利具有真实性 D.社会主义民主是全民的民主
近年来,我国民主政治建设加快,出现了听证会、旁听制度、公示制度、民主弹劾制度等诸多新的民主形式,促进了决策的民主化和科学化,保障了人民的利益。回答5-6题。
3.我国公民在享有广泛的政治权利和自由的同时,还必须履行以下政治性义务
①维护国家统一和民族团结 ②树立权利意识,监督政府行为
③维护国家安全、荣誉和利益 ④服兵役和参加民兵组织
A.①②③ B.②③④ C.①③④ D.①②④
2.我国公民享有对国家机关及其工作人员的监督权。公民可通过下列渠道行使监督权,实
行民主监督。
①信访举报制度 ②人大代表联系群众制度 ③舆论监督制度
④重大事项社会公示制度 ⑤民主评议会
A.②③④⑤ B.①②③④ C.①②④⑤ D.①②③⑤
1.政治自由是人民行使当家作主权利的重要形式,是社会主义民主的具体表现。公民在行使政治自由时
①必须坚持权利与义务的统一
②必须在宪法、法律规定的范围内行使
③不得损害国家、集体和其他公民的合法权利
④可以完全按照自己的意志行使
A.①②③ B.②③④ C.①②④ D.①③④
12.(2009年梁丰质检)已知Ksp(AgCl)=c(Ag+)·c(Cl-)=1.8×10-10,Ksp(Ag2CrO4)=1.9×10-12,某同学通过实验验证醋酸银(CH3COOAg)的Ksp,实验中用了如下反应:2Ag+(aq)+Cu(s)=2Ag(s)+Cu2+(aq),该学生将已知质量的铜片加入到CH3COOAg饱和溶液中,待充分反应后,将铜片冲洗干净、重新称量。
(1)CH3COOAg的Ksp=2.0×10-3,没反应前铜片的质量为23.4 g,将铜片放在100 mL的CH3COOAg饱和溶液中,此饱和溶液中没有CH3COOAg固体,通过计算说明充分反应后铜片中铜的质量为何值时,CH3COOAg的Ksp得到证实。
(2)为什么做此实验时CH3COOAg饱和溶液中必须没有CH3COOAg固体?
11.(2009年海南模拟)如下图所示,横坐标为溶液的pH值,纵坐标为Zn2+离子或
Zn(OH) 42-,离子物质的量浓度的对数,回答下列问题。
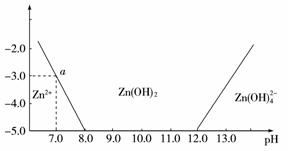
(1)往ZnCl2溶液中加入足量的氢氧化钠溶液,反应的离子方程式可表示为:____________ 。
(2)从图中数据计算可得Zn(OH)2的溶度积(Ksp)=-____________________________________ 。
(3)某废液中含Zn2+离子,为提取Zn2+离子可以控制溶液中pH值的范围是____________ 。
(4)往100 L 1.00 mol·-1L ZnCl2溶液中加入NaOH固体至pH=6,需NaOH____________ mol。
(5)已知:往ZnCl2溶液中加入硝酸铅或醋酸铅溶液可以制得PbCl2白色晶体;25 ℃时,PbCl2固体在盐酸中的溶解度如下:
|
c(HCl)/(mol·-1L) |
0.50 |
1.00 |
2.04 |
2.90 |
4.02 |
5.16 |
5.78 |
|
c(PbCl2)/(mol·-1L)×10-3 |
5.10 |
4.91 |
5.21 |
5.90 |
7.48 |
10.81 |
14.01 |
根据上表数据判断下列说法正确的是____________(填字母序号)
A.随着盐酸浓度的增大,PbCl2固体的溶解度先变小后又变大
B.PbCl2固体在0.50 mol·-1L盐酸中溶解度小于在纯水中的溶解度
C.PbCl2能与浓盐酸反应生成一种难电离子的阴离子(如配合离子)
D.PbCl2固体可溶于饱和食盐水
10.已知常温下,FeS的Ksp=6.25×10-18 mol2·L-2,ZnS的Ksp=1.2×10-23 mol2·L-2,H2S的饱和溶液中[H+]与[S2-]之间存在如下关系:[H+]2·[S2-]=1.0×10-22 mol3·L-3。试回答下列有关问题:
(1)向ZnS的饱和溶液中:①加入少量固体Na2S,则溶液中[S2-]____________(填“变大”、“变小”或“不变”,下同);②加入ZnS固体,则溶液中[S2-]____________;③加入FeS固体,则溶液中[Zn2+]____________。
(2)在常温下,将适量的FeS投入到氢硫酸饱和溶液中,欲使溶液中[Fe2+]达到1 mol/L,应调节溶液的pH=__________(已知:lg2=0.3)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com