
13.下列说法中,不正确的是
A.室温下,CH3COOH分子可以存在于pH=8的碱性溶液中
B.在0.1mol•L-1的氢溴酸中加入适量的蒸馏水,溶液的c(H+)减小
C.在由水电离出的c(OH-)=1×10-12mol•L-1的溶液中,Al3+不可能大量存在
D.在NaAlO2溶液中,HCO3-不可能大量存在
12.下列各溶液中能大量共存的离子组是
A.使酚酞试液呈红色的溶液中:Mg2+ Cu2+ SO42- K+
B.使pH试纸呈红色的溶液中:Fe2+ I- NO3- Cl-
C.c(H+)=1-14mol/L的溶液中:Na+ 、 [Al(OH)4]-、 S2- SO32-
D.水电离出的c(H+)与c(OH-)乘积为10-28的溶液中:K+ Na+ HCO3- Ca2+
11.对下列离子在溶液中能否大量共存的判断正确的
A.pH=0的溶液中Na+、[Al(OH)4]-、S2-、SO32-能共存
B.Na+、[Al(OH)4]-、HCOO-、MnO4-能共存
C.在c(HCO3-)=0.1mol/L的溶液中Al3+、H+、NH4+、Cl-能共存
D.在使甲基橙变红的溶液中Cu2+、Mg2+、Cl-、NO3-能共存
10.用pH大小表示溶液的酸碱性相对强弱有许多不足之处。因此,荷兰科学家HenkVan Lubeck引入了酸度(AG)的概念,即把电解质溶液中的酸度定义为c(H+)与
c(OH一)比值的对数,用公式表示为AG=lg [c(H+)/c(OH一)] 。常温下,在AG=1的溶液中能大量共存的离子是。
A.Ca2+、K+、Cl- 、NO3-- B.NH4+、Fe3+、 I一、SO42-
C.Na+ 、K+、ClO--、S2- D.Na+、S2O32-、[Al(OH)4]- 、K+
9.下列各组离子在溶液中既可以大量共存,且加入过量氨水后也不产生沉淀的是
A.Na+、Ba2+、Cl-、SO42- B.K+、[Al(OH)4]-、NO3-、OH-
C.H+、NH4+、 Al3+、SO42- D.H+、Cl-、CH3COO-、NO3-
8.某一无色溶液,若向其中加入足量饱和氯水,溶液呈橙黄色;再向橙黄色溶液中滴加BaCl2溶液,产生白色沉淀;若向原溶液中加入铝粉,有气体放出。该溶液可能大量存在的一组离子是
A.K+、H+、NO3-、Na+ B.H+、Br-、SO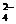 、Na+
、Na+
C.SO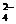 、Br-、OH-、Fe3+ D.H+、Br-、SO
、Br-、OH-、Fe3+ D.H+、Br-、SO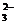 、K+
、K+
7.下列各组离子在碱性条件下可以大量共存,而在强酸性条件下能发生氧化还原反应的是
A.Ca2+、Fe2+、NO3-、Cl- B.K+、Mg2+、HCO3-、PO43-
C.Na+、K+、SO42-、SO32- D.Ba2+、Na+ 、I-、NO3-
6.下列各组离子,在碱性溶液中能大量共存,且无色透明,但加入硫酸酸化后,溶液变色,同时无沉淀、无气体生成的是
A.Na+、I-、MnO4-、SO42- B.K+、I-、SO42-、SiO32-
C.Ca2+、Cl-、H2PO4-、NO3- D.Na+、SO42-、Br-、
5.若在加入铝粉能放出氢气的溶液中,分别加下列各组离子,可能共存的是
A.NH4+、NO3-、CO32-、Na+ B.Na+、Ba2+、Mg2+、HCO3-
C.NO3-、Ca2+、K+、Cl- D.NO3-、K+、[Al(OH)4]-、OH-
4.下列各组离子中,能在水溶液中大量共存且溶液显酸性的是 (
A.Al3+、HCO3-、Na+ B.Al3+、Mg2+、SO42-
C.[Al(OH)4]-、HCO3-、Na+ D.Al3+、[Al(OH)4]-、Cl-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com