
15.W、X、Y、Z是原子序数依次增大的同一短同期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X各自的最高价氧化物对应的水化物可以反应生盐和水,该反应的离子方程式为 。
(2)W与Y 可形成化合物W2Y,该化合物的电子式为 。
(3)X的硝酸盐水溶 液显 性,用离子方程式解释原因 。
(4)Y的低价氧化物通入Z单质的水溶液中,发生反应的化学方程式为 。
(5)比较Y、Z气态氢化物的稳定性__>__(用分子式表示)
(6)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是:
__>__>__>__。
14.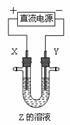 利用右图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产。下列说法中正确的是
利用右图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产。下列说法中正确的是
A.氯碱工业中,X、Y均为石墨,Y附近能得到氢氧化钠
 B.铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4
B.铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4
C.电镀工业中,X是待镀金属,Y是镀层金属
D.外加电流的阴极保护法中,Y是待保护金属
第Ⅱ卷(共72分)
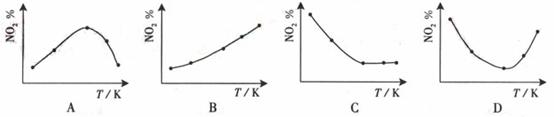
13. 取5等份NO2 ,分别加入温度不同、容积相同的恒容密闭容器中,发生反应:2NO2(g) N2O4(g),△H<0。反应相同时间后,分别测定体系中NO2的百分量(NO2%),并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是BD
N2O4(g),△H<0。反应相同时间后,分别测定体系中NO2的百分量(NO2%),并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是BD
12. 下列比较中,正确的是
A.同温度同物质的量浓度时,HF比HCN易电离,则NaF
溶液的 pH 比 NaCN 溶液大
B.0.2 mol·L-1NH4Cl和 0.l mol·L-1 NaOH 溶液等体积混合后:
c(NH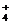 )>c(Cl-)) >c(Na+)>c(OH-)>c(H+)?
)>c(Cl-)) >c(Na+)>c(OH-)>c(H+)?
C.物质的量浓度相等的 H2S 和 NaHS 混合溶液中:c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH―)
D.同浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3·H2O;c(NH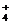 ) 由大到小的顺序是:①>②>③>④
) 由大到小的顺序是:①>②>③>④
11. 对Na、Mg、Al的有关性质的叙述正确的是 ( )
A.碱性:NaOH < Mg(OH)2 <Al(OH)3 B.第一电离能:Na < Mg < Al
C.电负性:Na > Mg > Al D.还原性:Na > Mg > Al
10. 下列离子方程式正确的是
A.用惰性电极电解饱和氯化钠溶液:2Cl- + 2H+  H2↑+ Cl2↑
H2↑+ Cl2↑
B.用银氨溶液检验乙醛中的醛基:
CH3CHO +2Ag(NH3)2+
+ 2OH- CH3COONH4
+3NH3 + 3Ag↓+ H2O
CH3COONH4
+3NH3 + 3Ag↓+ H2O
C.苯酚钠溶液中通入少量CO2:CO2 + H2O
+ 2C6H5O- 2C6H5OH
+ 2CO32-
2C6H5OH
+ 2CO32-
D.Na2SO3溶液使酸性KMnO4溶液褪色:5SO32- + 6H+ + 2MnO4- == 5SO42- + 2Mn2+ 3H2O
9. 对于白磷引起的中毒,硫酸铜溶液是一种常用的解毒剂,有关反应如下:
 11P+15CuSO4+24H2O==5Cu3P+6H3PO4+15
H2SO4。下列关于该反应的说法正确的是
11P+15CuSO4+24H2O==5Cu3P+6H3PO4+15
H2SO4。下列关于该反应的说法正确的是
A.CuSO4发生了氧化反应
B.生成1 mol H3PO4时,有10 mol电子转移
C.氧化产物和还原产物的物质的量之比为6:5
D.P只作还原剂
8. 下列各组离子在给定条件下能大量共存的是
A、在pH=1溶液中:NH4+、K+、ClO-、Cl-
B、有SO42-存在的溶液中:Na+、Mg2+、Ca2+、I-
C、有NO3-存在的强酸性溶液中:NH4+、Ba2+、Fe2+、Br-
D、在c(H+) =1.0×10-13mol/L的溶液中:Na+、S2-、AlO2-、SO32-
7. 有A,B,C三种短周期元素,已知A元素的原子最外层电子数等于其电子层数,B元素的原子最外层电子数是其电子层数的2倍,C元素的原子最外层电子数是其电子层数的3倍.由这三种元素组成的化合物的化学式不可能是( )
A.A3BC4 B.A2(BC4)3 C.A2BC3 D.ABC4
6. 下列关于氧化物的各项叙述正确的是 ①酸性氧化物肯定是非金属氧化物 ②非金属氧化物肯定是酸性氧化物 ③碱性氧化物肯定是金属氧化物 ④金属氧化物都是碱性氧化物 ⑤酸性氧化物均可与水反应生成相应的酸 ⑥与水反应生成酸的氧化物不一定是酸性氧化物,与水反应生成碱的氧化物不一定是碱性氧化物 ⑦不能跟酸反应的氧化物一定能跟碱反应
A.①②③④ B.⑤⑥⑦ C.②③⑥⑦ D.③⑥
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com