
6.(2010年江西省余江一中模拟)下列句子标点符号使用正确的一项是( )
A.对于爱因斯坦,生与死的区别仅仅在于是不是在研究物理学问题?是不是在思索大自然的统一结构?是不是在不断地接近“他”,即接近斯宾诺莎的上帝--自然。
B.在我们为中华民族腾飞于世界而奋力拼搏的时代,不妨赋予“生无所息。”这句格言以崭新的含义,并将其写在我们的旗帜上。
C.人是由三部分组成的:对往事的追忆;对现时的把握;对未来的憧憬。
D.庄子永远有着我们不懂的地方,山重水复,柳暗花明;永远有着我们不曾涉及的境界,仰之弥高,钻之弥坚。
解析:选D。A项,两个问号改为逗号。B项,去掉引号中的句号。C项,将两个分号改为逗号。
5.下列句子中,标点符号使用正确的一句是( )
A.“广州城,香港地,澳门街”。这种百年称谓一向把袖珍小城澳门叫做“街”。街坊情谊亦就成为澳门一大特色。
B.回归十年,在一国两制、澳人治澳、高度自治的方针指引下,澳门实力增强,活力迸发。这是继香港回归之后,一国两制由构想变为现实的又一成功范例,是祖国和平统一征程上的又一里程碑。
C.11月16日,全国“扫黄打非”办公室下发了《关于严厉打击手机网站制作、传播淫秽色情信息活动的紧急通知》。那么,“手机黄祸”目前究竟有多严重,其背后隐藏着怎样的利益链条,在3G时代,我们如何才能规范手机信息传播秩序,遏制手机网站淫秽色情信息蔓延的势头呢?
D.在过去的20年间,《儿童权利公约》在世界范围内改变了人们看待和对待儿童的方式,它对国家和国际立法、政策和项目、公共和民间机构、家庭、社区及个人产生了广泛而深远的影响。
解析:选D。A项,将“澳门街”后的句号放在引号里面。B项,分别给“一国两制”和“澳人治澳”加双引号。C项,分别把“严重”“利益链条”后的逗号改为问号。
4.下列句子中,标点符号使用正确的一句是( )
A.因为信息化,战斗机可以在超视距外,发动对地空目标的精确打击;因为电磁干扰和攻击,指挥控制系统会失灵……在解放军理工大学的实验室里,就在真正的一瞬间,强电磁波像一张无形的大手,猛力地拍打着演示计算机,巨大的冲击波使屏幕剧烈地抖动、变黑、瘫痪。
B.奥巴马临行前在驻韩美军乌山基地盘点这次马拉松式出访的三大收获:给美日同盟注入新活力;美国与亚太国家承诺促成更自由的贸易关系;与中国达成更积极的伙伴关系。
C.尼泊尔总理尼帕尔在珠穆朗玛峰雪山会议后举行的新闻发布会上说,珠穆朗玛峰是地球环境的标志,而气候变化对这一地区民众的生存、生态环境、社会经济发展等都造成了影响。
D.钟南山还表示,禽流感致死率高,要警惕甲流和禽流感发生重组变异的可能。这种情况若出现,“将是一个非常大的灾难。”
解析:选C。A项,要用较强的语气强调动词谓语“抖动”“变黑”“瘫痪”,将最后的两个顿号改为逗号。B项,将两个分号均改为逗号。D项,将句号放在双引号外。
3.(2010年天津河西区质检)下列各句标点符号使用合乎规范的一项是( )
A.在地震中逃生是人本能的反应,作为老师在地震时逃生是可以理解的,但我不知道“范跑跑”(范美忠老师)为什么在逃生后说出“连亲娘也不救”的话来?
B.2009年《考试大纲》将“正确使用标点符号”一项前的“*”去掉了,这表明标点符号将成为今年高考试题的卷面内容。
C.他从报上看到某大学研究生院和《中国文化》编委会联合主办《中国文化与世界文化暑期讲习班》的招生启事,立刻写信去报名。
D.桃花开了,红得像火;梨花开了,白得像雪;郁金香也开了,黄色、紫色交相辉映,好一派万紫千红的灿烂春光。
解析:选B。A项,问号改为句号;C项,第二个书名号改为引号;D项,最后一个逗号改为冒号。
2.下列句子中,标点符号使用正确的一句是( )
A.全世界每个地区都要对传统的儿童发展领域进行投资(营养、保健、教育、水与环境卫生),提高学校和社区环境教育的质量,增强对风暴、洪水、干旱等灾害的预警。
B.“一年来,我在熟悉了解学校工作,整个教育工作保持在过去的水平上时,队伍不乱、人心不散、成效不减。”校长简单概括在新岗位上的体会。
C.作为目前世界经济体的第三大国(赶超日本成为世界第二经济大国也是近在咫尺)--中国,在这场危机中还是意识到了自己在某些关键问题的处理上处于一种“被动”的局面。
D.具有推荐学生上北大资质的中学,如存在弄虚作假等情形,一经发现,立即取消中学及校长的推荐资质,获推荐的学生,如存在弄虚作假等情形,一经发现,立即取消学生的资格。
解析:选C。A项应将“(营养、保健、教育、水与环境卫生)”放在“领域”后。B项应将两个顿号改为逗号,起强调语气。D项应将“推荐资质”后的逗号改为分号。
1.(2010年山东枣庄模拟)依次填入下列序号处的标点符号,正确的一项是( )
他还透露,第一期讲座将讲一本名为《书法有法》的书①古时候,手势和笔法合在一起称为‘书法②就像一种行为艺术③他说④现在却失掉了一半了⑤
|
|
① |
② |
③ |
④ |
⑤ |
|
A |
。“ |
’, |
,” |
,“ |
。” |
|
B |
,“ |
,’ |
,” |
;“ |
。” |
|
C |
。“ |
’, |
”, |
;“ |
”。 |
|
D |
,“ |
,’ |
”, |
,“ |
”。 |
解析:选A。先根据④处判断,人物说话的内容在“说”的两边,“说”后应为逗号,据此排除B、C两项;⑤处是说话内容的全部结束,应为句号且在引号内。
3、化学性质--硫原子最外层6个电子,较易得电子,表现较强的氧化性。
(1)与金属反应 Na+S--Na2S (剧烈反应并发生爆炸)
(Na+S--Na2Sx)
 Al+S △ Al2S2(制取Al2S3的唯一途径)
Al+S △ Al2S2(制取Al2S3的唯一途径)
 Fe+S △ FeS(黑色)
Fe+S △ FeS(黑色)
思考:①21g铁粉跟8g硫粉混合加热,冷却后将所得固体溶于足量盐酸,在标准状况下可得气体多少升?
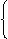 (据Fe-FeS-H2S↑可知,不论谁过量,有1molFe,必须生成1mol气体,则所得气
(据Fe-FeS-H2S↑可知,不论谁过量,有1molFe,必须生成1mol气体,则所得气
Fe-H2↑
体体积为: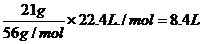 )
)
②若为21g硫粉和8g铁粉混合,在空气中加热,冷却后,所得固体质量为多少克?
 (解:Fe + S △ FeS
(解:Fe + S △ FeS
56g 32g
8g 21g
则硫过量,但由于在空气中加热,过量的硫与O2反应生成了SO2气体,因此,所得固体只能为FeS。其质量为: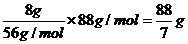 )
)
 2Cu + S △ Cu2S(黑色)
2Cu + S △ Cu2S(黑色)
思考:①进行该实验时,将硫固体加热熔化至变成蒸气,再将光亮的铜丝放入硫蒸气中发生反应。实验时间较长,能否改成将铜丝加热后插入硫粉中?
 (不能,若将铜丝在酒精灯上加热,Cu+O2 △ CuO(黑色),铜转化为氧化铜,反应将不再发生)
(不能,若将铜丝在酒精灯上加热,Cu+O2 △ CuO(黑色),铜转化为氧化铜,反应将不再发生)
②对铜,铁与硫的反应产物进行分析,硫与Cl2的氧化性哪个更强?理由是什么?
(氯气更强,因为S只将铜,铁氧化到低价,而氯气则将它们氧化到高价)
 (2)与非金属的反应 S+O2 点燃 SO2
(2)与非金属的反应 S+O2 点燃 SO2
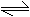 思考:已知2SO2+O2 2SO3+Q(Q>0)反应温度对SO3的产率影响更大。硫在空气中和纯氧中燃烧,均能产生少量SO3,问在空气中或纯氧中燃烧哪个产生更多的SO3?为什么?
思考:已知2SO2+O2 2SO3+Q(Q>0)反应温度对SO3的产率影响更大。硫在空气中和纯氧中燃烧,均能产生少量SO3,问在空气中或纯氧中燃烧哪个产生更多的SO3?为什么?
(空气中。因为纯氧中燃烧,尽管O2浓度大,但产生的热量更多,而在空气中燃烧,速率较小,产生的热量能及时分散到空气中)
 S+H2 H2S(说明硫化氢不稳定)
S+H2 H2S(说明硫化氢不稳定)
(3)与化合物的反应


 S+6HNO3(浓) △ H2SO4+6NO2↑+2H2O
S+6HNO3(浓) △ H2SO4+6NO2↑+2H2O
S+2H2SO4(浓) △ 2SO2↑+2H2O
 S+NaOH △ Na2S+Na2SO3+H2O
S+NaOH △ Na2S+Na2SO3+H2O
思考:由硫能溶于热碱溶液可知,用热碱溶液可洗去试管壁上的硫,实验室为何常用热Ca (OH)2溶液而不用热NaOH溶液除去试管内的硫?(因NaOH碱性强,腐蚀玻璃)
S + Na2S = Na2Sx
S + Na2SO3 △ Na2S2O3
例1、硫与热强碱溶液可生成S2-和SO32-;生成物继续与硫作用得Sz2-和S2O32-。过滤后除去过量硫,向滤液中加入一定量的强碱后,再适入足量的SO2,SO2与Sz2-也完全转化为S2O32-。问:
(1)S+SO2+OH-完全转化为S2O32-的离子方程式____________________
(2)amolS最终转化为Na2S2O3,需SO2、NaOH的物质的量分别为________
(3)若amolS最终转化为Na2Sz耗原热碱溶液6molNaOH,则Na2Sx中x值为
_________。
 解析:3S+6OH‑ △ 2S2-+SO32-+3H2O …………①
解析:3S+6OH‑ △ 2S2-+SO32-+3H2O …………①


 S2-+(x+1)S Sx2- ………………②
S2-+(x+1)S Sx2- ………………②
SO32-+S △ S2O32- ……………………③
由①②③迭加得:(2x+2)S+6OH- = 2Sx2-+S2O32-+3H2O …………④
SO2+Sx2-+OH---S2O32-+H2O ………………⑤
由④⑤迭加得:S+SO2+2OH-=S2O32-+H2O …………………………⑥
答:第(1)问时,实质不必要这么繁的过程,因Sx2-、SO32-均为中间产物,只要抓住反应物为S和SO2及OH-,生成物为S2O32-和水即可得反应⑥。
由⑥式可知每有1mol硫需1molSO2和2molOH-,则SO2和OH-分别为a、2amol。
(2)由④式可知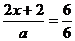 x=
x=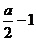
例2、工业上将硫黄混入Na2SO3溶液中共热至沸可制取Na2S2O3。制备Na2S2O3的另一种方法是把SO2通入Na2S和Na2CO3的混合液中,在反应过程中,先生成黄色沉淀,其量逐渐增多,然后又逐渐减少。当形成无色透明溶液时,反应完成:
(1)写出用上述反应制备Na2S2O3的化学方程式
①_________________________ ②____________________
③_________________________ ④Na2SO3+S △ Na2S2O3
(2)原料中Na2CO3、Na2S、SO2的物质的量比最佳是___________________。
(3)若SO2过量,则又会有黄色沉淀出现,其原因是(用离子方程式表示)______________。
解析:由于SO2溶于水生成H2SO3,而H2SO3是中强酸,其酸性比H3PO4还要强。则
(1)①SO2+H2O+Na2S= Na2SO3+H2S
②SO2+Na2CO3= Na2CO3+CO2
③SO2+2H2S= 3S↓+2H2O
(2)要求三种物质的最佳配比,必须牢牢抓住关键的反应式④,其反应物为S和
Na2SO3,S由反应③生成,Na2SO3由反应①②形成,由反应③可知每生成3molS需2molH2S和1molSO2,则反应④可改为3Na2SO3+3S=3Na2S2O3,而生成2molH2S则需2molNa2S和2molSO2,同时生成2mol Na2SO3,现还差1mol Na2SO3,由反应②提供。则Na2CO3、Na2S、SO2的最佳物质的量比为1:2:4。
(3)若SO2过量,又生成3H2SO3,H2SO3+S2O32-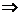 H2S2O3+SO32-,H2S2O3极不稳定,H2S2O3→H2O+S+SO2,SO2与SO32-又能继续转化为HSO3-,因此,该反应的离子方程式为:
H2S2O3+SO32-,H2S2O3极不稳定,H2S2O3→H2O+S+SO2,SO2与SO32-又能继续转化为HSO3-,因此,该反应的离子方程式为:
SO2+H2O+S2O32-=S↓+2HSO3-

 2e 10e
2e 10e
 S + 3C +2KNO3
点燃 K2S+N2↑+3CO2(黑火药爆炸)
S + 3C +2KNO3
点燃 K2S+N2↑+3CO2(黑火药爆炸)
橡胶的硫化(化学变化,将橡胶从线型结构转化为体型网状结构,增强橡胶的强度和弹性)
2、物理性质:硫有多种同素异开体。如单斜硫、斜方硫、弹性硫等。不同温度硫分子含硫原子数不同、常温是S8、高温蒸气主要是S2。常温为淡黄色晶体(淡黄色固体有:Na2O2、AgBr、黄铁矿、T、N、T等)。
注意:①在溶液中通过化学反应生成少量硫时,有时称乳白色。
②硫的溶解性:不溶于水,微溶于酒精,易溶于CS2。因此用物理方法洗去试管壁上的硫,只能用CS2作溶剂。
1、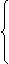 游离态--自然界存在于火山喷口、地壳岩层。人类在远古时代发现并使用硫。
游离态--自然界存在于火山喷口、地壳岩层。人类在远古时代发现并使用硫。
存在
化合态--存在形式有:FeS2(非盐)、CuFeS2(复盐)、石膏、芒硝、煤和石油
中含少量硫--污染大气物主要来源。
1.氧族元素原子结构、单质性质
|
元素名称和符号 |
氧(O) |
硫(S) |
硒(Se) |
碲(Te) |
|||||||
|
原子 结构 |
原子序数 |
8 |
16 |
34 |
52 |
||||||
|
结构示意图 |
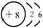 |
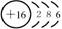 |
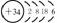 |
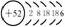 |
|||||||
|
电子式 |
·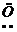 ∶ ∶ |
·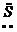 ∶ ∶ |
·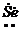 ∶ ∶ |
·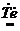 ∶ ∶ |
|||||||
|
主要化合价 |
-2 |
-2,+4,+6 |
-2,+4,+6 |
-2,+4,+6 |
|||||||
|
相同点 |
最外层电子数相同,都是6个电子 |
||||||||||
|
不同点 |
原子核外电子层数不同,依次增大 |
||||||||||
|
原子半径 |
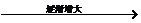 |
||||||||||
|
物 理性 质 |
颜色和状态 |
无色无味气体 |
淡黄固体 |
灰色固体 |
银白色固体 |
||||||
|
密度 |
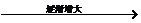 |
||||||||||
|
熔点(℃) |
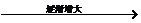 |
||||||||||
|
沸点(℃) |
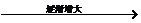 |
||||||||||
|
水、有机溶济溶解度 |
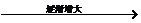 |
||||||||||
|
化学反 |
与金属反应 |
易与金属反应 |
易与金属反应 |
反应较难 |
多数不反应 |
||||||
|
与非金属反应 |
易与H2、C、P、S等反应 |
能与H2、C、O2反应 |
反应难 |
一般不反应 |
|||||||
|
与化合物应 |
能与许多物质反应 |
能与氧化性酸、强碱反应 |
反应少 |
反应很少 |
|||||||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com