
7.草拟·起草
都指文章、文件的拟稿。“草拟”还指初步设计。如:草拟规划。
6.摒除·驱除
都指除去,都用于思想、感情等。如:摒除杂念;驱除疑虑。“驱除”还指赶走。如:驱除蚊蝇。
5.摒弃·抛弃
都指舍弃。摒弃:多指不良思想、观点、主张等。抛弃:不仅指思想、事物,也可指人。“摒弃”属书面语。
4.变换·变幻
变换:指事物的形式或内容的更换。如:变换位置。变幻:指事物的形式或内容不规则地或奇异地变化,不能带宾语。如:风云变幻。
3.抱怨·埋怨
抱怨:表示怨恨,语义较重。埋怨:表示责怪,语义较轻。“埋怨”的对象可以是自己;“抱怨”无此用法。
2.包含·包涵
包含:指里边含有。包涵:指请人原谅。如:请多包涵。
1.包括·包罗·囊括
包括:指包含。其范围小于“包罗”。包罗:指大范围事物。如:包罗万象。囊括:指全部包罗在内。如:囊括全部金牌。
例1、A和B是同一主族的元素。A的最高正价与它的负价绝对值相等,可生成气态氢化物,其中氢的质量分数为25%;B跟氧形成的二氧化物是一种难溶于水的固体,其中氧的质量分数为53.3%,试推断A和B是什么元素,及它们在元素周期表中的位置。
解:因为A元素的最高正价数等于负价数,则A处于IVA族,设A和B的原子量为M1 和M2。
A的氢化物的化学式为AH4,则
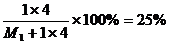
M1=12
B的二氧化物化学式是BO2,则
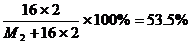
M2=28
答:A是碳,位于第二周期IVA族。B是硅,位于第三周期IVA族。
例2、同一周期X、Y、Z三种元素,已知最高价氧化物对应水化物的酸性是HXO4>H2YO4>H3ZO4,则下列判断错误的是
A、原子半径X>Y>Z B、气态氢化物的稳定性HX>H2Y>ZH3
C、非金属性X>Y>Z D、阴离子的还原性Z3->Y2->X-
解析:由三种元素最高价氧化物的水化物的化学式知X、Y、Z的最高正价分别为+7、+6、+5,推知它们分别位于第VIIA、VIA、VA族。由同一周期元素性质的递变规律。可确定A符合题意。
答案:A
例3、处于相邻2个周期的主族元素A、B、C、D。它们原子半径依次减小。A离子和B离子的电子层相差2层,且能形成BA2型的离子化合物。C的离子带3个单位正电荷。D的气态氢化物通式为H2R,在其最高价氧化物中D质量分数为40%。D的原子序数大致等于其原子量数值的一半。试回答
①A是______ B是______ C是______ D是______
②B、C、D单质的还原性从大到小的顺序是______。
③向D的氢化物的水溶液中,滴入少量A单质,写出反应的化学方程式。
解析:由H2R可知D可显-2价,D的最高价为+6,最高价氧化物为DO3。

解得:D=32,D的原子序数为16,D 为硫元素符合题意。
由A离子和B离子相差2个电子层,且能形成BA2型离子化合物,说明B为IIA族元
素,A为VIIA族元素。再由A、B、C、D原子半径依次变小,D为S可知,A为Br、B为Mg、而C为Al。
答案①Br、Mg、Al、S ②Mg>Al>S ③H2S+Br2=S↓+2HBr
例4、A、B、C、D为周期表中前三周期元素,A元素原子的次外层电子数是最外层电子数的二分之一,B的阴离子核外只有一个电子层、C单质在标准状况下密度是1.43g/L,D元素的焰色反应呈黄色。将以上四种元素组成的结晶盐3.4g加热反至完全失去结晶水,其质量减少1.35g,所得无水盐中C元素的质量分数为39%,将该无水盐与适量盐酸作用得到一种弱酸,再将所得弱酸完全燃烧可得0.9g水和1.12L标准状况下的CO2,已知这种弱酸的一个分子中共有32个质子。试回答:①A、B、C、D四种元素各是什么元素?②求结晶盐化学式。
解析:A元素原子的次外层电子数是最外层电子数的二分之一,则只有碳元素符合,所以A是碳。B的阴离子只有一个电子层,可推断B是氢。根据……所得到弱酸完全燃烧,知此弱酸为有机酸。
C的摩尔质量=1.43g/L×22.4L/mol=32g/mol,所以C是氧。
弱酸中:
nc= =0.05mol
=0.05mol
nH= ×2=0.1mol
×2=0.1mol
n0=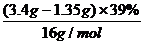 =0.05mol
=0.05mol
所以弱酸的最简式为:CH2O,其中共有6+2+8=16个质子,根据一个分子中有32个质子,故弱酸化学式为:C2H4O2是醋酸CH3COOH。

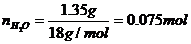

答案:①A为碳 B为氢 C为氧 D为钠
②CH3COONa·3H2O
3、核素和同位素区别
 (1)核素:具有一定数目的质子和一定数目的中子的一种原子。如1H(H)、2H(D)、3H(T)就各为一种核素。
(1)核素:具有一定数目的质子和一定数目的中子的一种原子。如1H(H)、2H(D)、3H(T)就各为一种核素。
(2)同位素:同一元素的不同核素之间互称同位素。 160、17O、180是氧元素的三种核素,互为同位素。
(3)元素、核素、同位素之间的关系如右图所示。
(4)同位素的特点
①同种元素,可以有若干种不同的核素。至今已发现了110种元素,但发现了核素远多于110种。
②核电荷数相同的不同核素,虽然它们的中子数不同,但是属于同一种元素。
③同位素是同一元素的不同核素之间的互相称谓,不指具体的原子。
④17O是一种核素,而不是一种同位素。160、17O、180是氧元素的三种核素,互为同位素。
⑤同一种元素的不同同位素原子其质量数不同,核外电子层结构相同,其原子、单质及其构成的化合物化学性质几乎完全相同,只是某些物理性质略有差异。
规律:
不同价态的同种元素与其氢氧化物酸碱性的关;变价元素氧化物对应水化物的酸性与价态有关,价态越低其对应水化物的酸性越弱,碱性越强。例如:
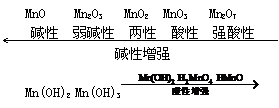 HCl0 HCl02 HCl03 HCl04,
HCl0 HCl02 HCl03 HCl04,

2、判断元素非金属性的强弱。
a、跟随氢气形成气态氢化物的难易,易则强。
b、氢化物的稳定性,稳则强。
c、最高价氧化物的水化物的酸性强弱,酸性强则强。
d、置换反应,强换弱。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com