
21.(8分)由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有图示的转换关系,已知C为密度最小的气体,甲是电解质。
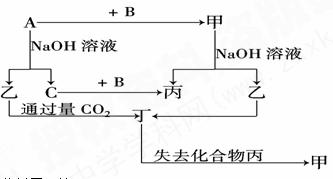
根据图示转化关系回答:
(1)写出下列物质的化学式:
B ,乙 ,丁 .
(2)组成单质A的元素在周期表中的位置是__________;
(3)写出下列方程式:
①A与NaOH溶液反应的化学方程式____________________________________。
②乙与过量CO2反应的离子方程式 _。
20.(8分)向Ba(OH)2溶液中逐滴加入稀硫酸.请完成下列问题:
(1)写出反应的离子方程式 ;
(2)下列三种情况下,离子方程式与(1)相同的是________(填序号).
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO恰好完全沉淀
 C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
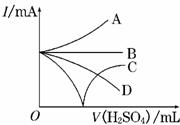
(3)若缓缓加入稀H2SO4直至过量,整个过程中混合溶液中的导电能力(用电流强度I表示)可近似地用左图中的曲线表示是________(填序号)。
(4)若有一表面光滑的塑料小球悬浮于Ba(OH)2溶液中央,如图所示.向该烧杯里缓缓注入与Ba(OH)2溶液等密度的稀H2SO4至恰好完全反应.在此实验过程中,小球将_________________________________。
19.(8分)(1)0.3 mol NH3分子中所含氢原子数与 个H2O分子中所含氢原子数相等。
(2)含0. 4 mol Al3+的Al2(SO4)3中所含的SO的物质的量是 。
(3)已知16 g A和20 g B恰好完全反应生成0.04 mol C和31.76 g D,则C的摩尔质量为 。
(4)2.3 g Na中含 mol e-,在跟足量水反应中失去 mol e-。
18.(9分)某化学课外活动小组欲制取纯Na2CO3溶液并讨论实验过程中的相关问题.可供选择的试剂有:
A.大理石 B.盐酸 C.氢氧化钠溶液 D.澄清石灰水
三名同学设计的制备实验方案的反应流程分别如下:
甲:NaOH溶液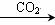 Na2CO3溶液
Na2CO3溶液
乙:NaOH溶液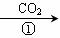 NaHCO3溶液
NaHCO3溶液 Na2CO3固体
Na2CO3固体 Na2CO3溶液
Na2CO3溶液
丙:NaOH溶液 NaHCO3溶液
NaHCO3溶液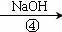 Na2CO3溶液
Na2CO3溶液
请回答下列问题:
(1)请指出甲、乙两方案的主要缺点:
甲方案:____________________________________________________;
乙方案:____________________________________________________。
(2)若采用丙方案制取纯Na2CO3溶液,其实验的关键是
。
(3)假设反应②所得的Na2CO3固体中混有未分解的NaHCO3,乙同学选择澄清石灰水测定其中NaHCO3的质量分数,乙同学__________(填“能”或“不能”)达到实验目的;若能,请说明计算所需的数据;若不能,请简要说明理由:
。
17.(9分)掌握仪器的名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。
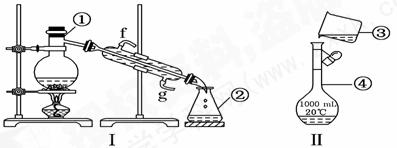
(1)写出下列仪器的名称:① ,② ,④ .
(2)仪器①-④中,使用时必须检查是否漏水的有 (填序号)
(3)若利用装置Ⅰ分离四氯化碳和酒精的混合物,还缺少的仪器有 ,将仪器补充完整后进行的实验操作的名称为 ;冷凝管的进水口是 (填“f”或“g”);现需配制250 mL 0.2 mol/L NaCl溶液,装置Ⅱ是某同学转移溶液的示意图,图中的错误是
。
16.向含有1 mol明矾的溶液中逐滴加入Ba(OH)2溶液,充分反应,下列说法不正确的是 ( )
A.当Al3+恰好完全沉淀时,消耗Ba(OH)21.5 mol
B.当SO恰好完全沉淀时,Al3+全部转化为AlO
C.随着加入的Ba(OH)2的物质的量不断增大,沉淀的物质的量不断增大
D.当向溶液中加入1.5 mol Ba(OH)2时,反应可用离子方程式2Al3++3SO+3Ba2++6OH-
===2Al(OH)3↓+3BaSO4↓表示
第II卷(非选择题,共52分)
15. 科学家指出,食用虾类等水生甲壳类动物的同时服用维生素C容易中毒,这是因为对人体无害的+5价砷类物质在维生素C的作用下,能够转化为有毒的+3价砷类化合物。下列说法不正确的是( )
科学家指出,食用虾类等水生甲壳类动物的同时服用维生素C容易中毒,这是因为对人体无害的+5价砷类物质在维生素C的作用下,能够转化为有毒的+3价砷类化合物。下列说法不正确的是( )
A.维生素C具有还原性
B.上述过程中砷元素发生还原反应
C.上述过程中+5价砷类物质作氧化剂
D.1 mol+5价砷类物质完全转化为+3价砷,失去2 mol电子
14.对某酸性溶液(可能含有Br-,SO,H2SO3,NH)分别进行如下实验:
①加热时放出的气体可以使品红溶液褪色;
②加碱调至碱性后,加热时放出的气体可以使润湿的红色石蕊试纸变蓝;
③加入氯水时,溶液略显黄色,再加入BaCl2溶液,产生的白色沉淀不溶于稀硝酸.
对于下列离子,不能确认其在原溶液中存在的是 ( )
A.Br- B.SO
C.H2SO3 D.NH
13.在配制一定物质的量浓度的盐酸时,下列错误操作可使所配制溶液的浓度偏高的是( )
A.用量筒量取浓盐酸时俯视量筒刻度进行读数 B.溶解搅拌时有液体飞溅
C.定容时俯视容量瓶瓶颈刻度线 D.摇匀后见液面下降,再加水至刻度线
12.下列离子方程式正确的是 ( )
A.用醋酸溶解大理石粉末:CaCO3+2H+==Ca2++CO2↑+H2O
B.向FeCl3溶液中加入足量铜屑:Fe3++Cu==Fe2++Cu2+
C.AlCl3溶液中加入过量的浓氨水:Al3++4NH3·H2O===AlO+4NH+2H2O
D.Ca(HCO3)2溶液与足量NaOH溶液反应:Ca2++2HCO3-+2OH-==CaCO3↓+2H2O+CO32-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com