
3、我国能源消费结构的调整
天然气对于环境是清洁能源,对于消费者是廉价能源,而目前在中国能源消费结构中仅占2.7%。因此,我国必须调整能源消费结构,提高天然气的消费比重。
当我国能源消费结构得到调整,天然气消费比重上升,有助于我国大气环境的改善,减轻煤炭废渣污染,减轻交通运输负担。
当然,提高天然气消费比重,并不是要以天然气取代煤炭。我国是一个煤炭大国,是世界上主要的产煤国。因此在相当长的一段时间内,我们国家仍然会以煤炭为主体能源。此外,天然气还是重要的化工原料,也不可能完全作为能源资源消耗。
2、煤炭与天然气优缺点比较(参见课本图11.2)

注意:煤炭的价格便宜指的是煤炭单位质量的价格低廉;而天然气的比较价格低指的是用户在获得相同热值条件下,与石油、煤炭相比较,天然气所需支付的价格低。
1、煤炭在我国能源消费结构中的地位及影响
在我国的能源消费结构中,煤炭一直占到70%。由此带来一系列问题:
表11-3 煤炭的高消耗给中国带来的问题
|
环境问题 |
煤炭燃烧排放的粉尘是我国大气中可吸入颗粒物的主要来源之一。 |
|
煤炭燃烧排放的SO2是造成我国酸雨危害范围大、危害重的主要原因。 |
|
|
煤炭的堆放、燃烧后的废渣都会造成固体废弃物污染。 |
|
|
运输问题 |
北煤南运给我国的铁路与公路运输造成很大压力。 |
能源资源是区域发展不可或缺的重要资源。我国区域能源资源赋存量与区域发展水平很不匹配。特别是东部沿海地区与中西部地区的能源生产和消费存在着显著的差异:
[参照课本图11.1及课文,归纳要点如下表11-2所示]
|
|
东部沿海 |
西部地区 |
|
|
能源消费 |
需求量 |
大 |
小 |
|
原因 |
人口众多,经济发达,经济发展水平高,能源消费量大。 |
人口较少,经济较落后,能源消费量小。 |
|
|
能源生产 |
生产量 |
相对较小 |
相对较大 |
|
原因 |
能源相对贫乏,因而产量相对较小。 |
能源相对丰富,因而产量相对较大。 |
|
|
影响 |
经济优势得不到充分发挥。 |
资源优势得不到充分开发利用。 |
|
|
实例 |
长三角地区作为我国最大的综合性工业基地和最大城市群,能源消费很大,但是却是能源资源极度匮乏区,一次能源全靠区外输入。 |
新疆能源资源非常丰富,但是新疆及其周边地区对能源的需求量很小。 |
[一次能源与二次能源]
一次能源:人类直接从自然环境中获取的,直接用于生产生活的能源。又称天然能源或能源资源。比如煤、石油、天然气等等。
二次能源:指经由一次能源加工转化而成的能源。比如煤气、石油液化气、柴油、焦炭等等。
1.①化学能转变成了电能,有电流通过;
②加盐酸时平衡右移,加NaOH溶液时平衡左移,两种情况下产生的电流的方向相反;
③2I--2e→I2;
④AsO33-+H2O-2e→AsO43-+2H+
11、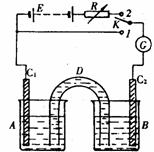 装置如右图:D是允许通过离子的盐桥,E是48V稳压电源,R是可变电阻,K是开关,G是灵敏电流计,C1、C2是碳棒,A、B是烧杯。
装置如右图:D是允许通过离子的盐桥,E是48V稳压电源,R是可变电阻,K是开关,G是灵敏电流计,C1、C2是碳棒,A、B是烧杯。
已知AsO43-+2I-+2H+ AsO33-+I2+H2O是可逆反应。若A中盛KI-I2溶液,B中盛Na3AsO4和Na3AO3溶液,则当K接1,并向B中滴加浓盐酸时发现G中的指针发生偏转;改向B中滴加40%的NaOH溶液时,G中的指针则向反方向偏转。
AsO33-+I2+H2O是可逆反应。若A中盛KI-I2溶液,B中盛Na3AsO4和Na3AO3溶液,则当K接1,并向B中滴加浓盐酸时发现G中的指针发生偏转;改向B中滴加40%的NaOH溶液时,G中的指针则向反方向偏转。
①两次操作过程中指针偏转的原因是
②指针偏转方向相反的原因是
③加盐酸时C1上发生的反应是
④加NaOH溶液时C1上发生的反应是
10、⑴ Fe2O3+3CO== 2Fe+3CO2 ⑵ 3Fe+ 4H2O= Fe3O4+ 4H2↑,油漆隔绝铁与空气接触, 起保护层作用,以防发生电化腐蚀。 ⑶铁作负极, 碳粉作正极, 发生吸氧腐蚀而放热。
10、铁是自然界里分布最广的金属元素之一,在地壳中的质量约占5%左右。铁矿石的种类很多,重要的有磁铁矿石(主要成分是Fe3O4)、赤铁矿石(主要成分为Fe2O3)等。工业上用一氧化碳作还原剂炼铁。铁及其化合物是生活、生产中必须的元素之一。
(l)、写出工业用赤铁矿炼铁的主要化学反应式:____________________________
(2)、红热的铁能与水蒸气起反应,有一种产物是可燃气体,则其反应式为:_______________________________________________。在常温下,铁跟水不起反应。但是,在水和空气里的氧气及二氧化碳等的共同作用下,铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢材年产量的四分之一。刷油漆是重要的防腐蚀措施之一。油漆防腐蚀的主要原因是___________________________________。
(3) 、一种冬季用“热敷袋”,内盛还原铁粉、碳粉及其它必要物质,用力搓此袋,袋则发热。请解释可能的原因_________________________________________。
9、由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱溶液反应制得纯净的Fe(OH)2沉淀。若用下图所示实验方法则可制得纯净的Fe(OH)2沉淀,已知两极材料分别是石墨和铁。
(1)、a电极材料为 ,其电极反应式为
(2)、在纯水、NaCl溶液:NaOH溶液与CuC12溶液中选择电解液d,可以是 ,此时白色沉淀在电极上生成;也可以是 ,此时白色沉淀在两极之间的溶液中生成。
(3)、液体c为苯,其作用是 ,在加入苯之前,对溶液进行加热处理的目的是
(4) 、为了在较短时间内看到白色沉淀,在① 改用稀硫酸作电解液、② 适当增大两极间电压、③ 适当缩小两极板间距离、④ 适当降低电解液的温度这四项措施中,可以采取的合理措施有 (填序号)。
(5)、若d改为硫酸钠溶液,当电解一段时间看到白色沉淀后,再反接电源继续电解,除了在电极上看到气泡外,另一明显现象是
解析:a极连接电源的正极,应为阳极,在阳极发生氧化反应。为获得Fe2+,应用铁作阳极,在此极上铁原子失去电子变为Fe2+。若用NaOH溶液作电解液,则Fe2+立即与OH- 结合,在阳极上生成白色沉淀;若用NaCl溶液作电解液,则在阴极是H+ 得至电子产生H2,由于H+ 的浓度减少,OH- 的浓度相对增多,OH-离子向阳极移动,与在阳极生成而向阴极移动的Fe2+结合为白色沉淀。
由于Fe(OH)2极易被空气中的O2所氧化,为防止此反应发生,在电解液上面覆盖一层苯(汽油也可)以隔绝空气。在加苯前,将溶液煮沸,驱赶溶解在水中的O2。
电解的速率与电压成正比,与两极间距离成反比;若加稀硫酸则沉淀溶解,若降低温度则离子迁移速率减慢,均不利于沉淀生成,将电解液改为硫酸钠溶液,在生成白色沉淀后,若反接电源,则阳极是石墨,为惰性阳极,结果与电解水相同,在阳极产生O2,将Fe(OH)2氧化为红褐色Fe(OH)3。
答案:(1)铁,Fe一2e-=Fe2+ 。 (2)NaOH;NaC1。
(3)隔绝空气,防止Fe(OH)2被空气氧化;赶走电解液中溶解的氧气。
(4)②③, (5)白色沉淀迅速变成灰绿色,最后变为红褐色。
8、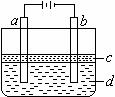 2009年3月,佳得利集团在法国拍卖会上拍卖在火烧圆明园时流失的国宝:铜铸的牛首、猴首和虎首。普通铜器时间稍久容易出现铜绿,其主要成分:Cu2(OH)2CO3。这三件1760年铜铸的国宝在240年后看上去仍然熠熠生辉不生锈,下列对其原因的分析,最可能的是
( D )
2009年3月,佳得利集团在法国拍卖会上拍卖在火烧圆明园时流失的国宝:铜铸的牛首、猴首和虎首。普通铜器时间稍久容易出现铜绿,其主要成分:Cu2(OH)2CO3。这三件1760年铜铸的国宝在240年后看上去仍然熠熠生辉不生锈,下列对其原因的分析,最可能的是
( D )
A.它们的表面都电镀上了一层耐腐蚀的黄金
B.环境污染日趋严重,它们的表面的铜绿被酸雨溶解洗去
C.铜的金属活动性比氢小,因此不易被氧化
D.它们是含一定比例金、银、锡、锌的铜合金
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com