
19、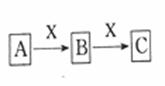 (本小题8分)具有如图转化关系的物质A、B、C有多种组合,请你根据下列要求回答问题。(如果有多组答案符合题意的,写出其中一种即可。)
(本小题8分)具有如图转化关系的物质A、B、C有多种组合,请你根据下列要求回答问题。(如果有多组答案符合题意的,写出其中一种即可。)
(1)若A是固态非金属单质,B是形成酸雨的物质,则C的分子式是 。
(2)若A是能使湿润红色石蕊试纸变蓝色的气体,符合要求的A→B的化学反应方程式为 。
(3)若A是强碱溶液,符合要求的B→C的离子反应方程式为
。
(4)若A是能使湿润淀粉碘化钾试纸变蓝色的气态非金属单质,符合要求的B→C的离子反应方程式为 。
18、(本小题8分)某无色溶液由Na+、Ag+、Ba2+、Al3+、AlO、MnO、CO、SO中的若干种组成。
取该溶液进行如下实验:
A、取试液适量,加入过量稀盐酸,有气体生成,得到溶液甲;
B、向溶液甲中再加入过量碳酸氢铵溶液,有气体生成,且析出白色沉淀乙,过滤得到溶液丙;
C、向溶液丙中加入过量氢氧化钡溶液并加热,有气体生成,且析出白色沉淀丁。
根据上述实验回答下列问题:
(1)溶液中一定不存在的离子是 。
(2)溶液中一定存在的离子是 。
(3)生成沉淀乙的离子反应方程式是
。
(4)写出步骤C中产生气体的离子方程式是
。
17、(10分)下图是元素周期表的一部分,请回答:

(1)形成元素化合物种类最多的元素是________(填元素名称);
(2)D、E、F的氢化物稳定性由强到弱的顺序是
______________________________(用相应的化学式填空);
(3)高温下,B置换出C的化学方程式:
_______________________________________;
(4)元素C的氧化物与A的最高价氧化物对应水化物反应的离子方程式:_________________________________________________;
(5)在元素周期表前10号元素中,两种元素原子的核外电子层数之比与最外层电子数之比相等的元素有_______对。
16、在粗碘中含ICl和IBr,受热时I2、ICl、IBr均可升华,在粗碘中加入一种物质后,再进行升华可制得精碘,应加入的物质是
A、H2O B、Zn C、KI D、KCl
株洲四中 醴陵二中 醴陵四中
2009年下期期中考试三校联考高三年级化学科考试答卷
计分:
15、向含有amolAlCl3的溶液中加入bmol NaOH 溶液,观察到的现象是先有白色沉淀,后沉淀部分溶解,则生成Al(OH)3沉淀的物质的量是
A、a mol B、(4a-b)mol C、b mol D、(4b-a)mol
14、用NA表示阿伏加德罗常数的值。下列叙述正确的是
A、常温下,2.24LN2和O2的混合气体所含原子数为0.2NA
B、常温下,0.01mol/L的醋酸溶液中所含有的H+数小于0.01NA
C、标准状况下,生成1mol氧化钠和1mol过氧化钠转移的电子数分别为2NA和4NA
D、标准状况下,6.72L CH4中所含的共用电子对数为1.2NA
13、下列反应的离子方程式中正确的是
A、钠与水的反应:Na + 2H2O = Na+ + 2OH-+ H2↑
B、在NaHSO4溶液中加Ba(OH)2至中性:HSO+Ba2++OH-= BaSO4↓+H2O
C、过量的SO2通入NaOH溶液中:SO2+2OH-=SO+H2O
D、碳酸氢钠溶液与足量氢氧化钡溶液混合:HCO+Ba2++OH-= BaCO3↓+H2O
12、钡和钠相似,也能形成O离子的过氧化物,则下列叙述错误的是
A、过氧化钡的化学式是Ba2O2
B、1mol过氧化钠或过氧化钡跟足量水反应都生成0.5mol氧气
C、过氧化钡是离子化合物
D、过氧化钠和过氧化钡都是强氧化剂
11、如图所示是元素周期表的一部分,X、Y、Z、W均为短周期元素,若W原
子最外层电子数是其内层电子数的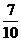 ,则下列说法中不正确的是
,则下列说法中不正确的是
A、原子半径由大到小排列顺序Z>Y>X
 B、Y元素的两种同素异形体在常温下都是气体
B、Y元素的两种同素异形体在常温下都是气体
C、最高价氧化物对应水化物的酸性W>Z
D、阴离子半径由大到小排列顺序Z>W >X>Y
10、配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是
A、所用NaOH已吸潮
B、向容量瓶加水时液面低于刻度线即摇匀
C、有少量NaOH溶液残留在烧杯内
D、向容量瓶加水时眼睛一直仰视液面
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com