
1.下列词语中加点的字,每对读音都不相同的一组是(3分)
A.着陆/着手成春 提防/提纲挈领 效率/马虎草率
B.没收/没完没了 发行/高山景行 传记/传奇人生
C.埋怨/埋头苦干 暖和/随声附和 艾草/自怨自艾
D.澄清/澄清是非 疲沓/纷至沓来 省悟/不省人事
100.下列各组离子在溶液中能大量共存的是
A. 酸性溶液Na+、K+、MnO4-、Br- B. 酸性溶液Fe3+、NH4+、SCN-、NO3-
C. 碱性溶液Na+、K+、AlO2-、SO42- D. 碱性溶液Ba2+、Na+、CO32-、Cl-
99.在pH=1的溶液中,可以大量共存的离子是 ( B )
A. Na+ K+ HCO3- Cl- B. NH4+ Mg2+ SO42- Cl-
C. K+ Na+ SO42- S2O32- D. K+ Na+ AlO2- NO3-
98.下列化学方程式中,不能用离子方程式 Ba2+ +SO42―=BaSO4 ↓ ( C )
A.Ba(NO3)2+H2SO4=BaSO4↓+2HNO3 B.BaCl2+Na2SO4=BaSO4↓+2NaCl
C.BaCO3+H2SO4=BaSO4↓+H2O+CO2↑ D.BaCl2+H2SO4=BaSO4↓+2HCl
97.离子方程式CO32- + 2H+ = H2O + CO2↑中的CO32-代表的物质可以是( C )
A.CaCO3 B.NaHCO3 C.Na2CO3 D.BaCO3
96.下列电离方程式错误的是( A )
A.NaHCO3 =Na+ +H+ +CO32- B.NaHSO4=Na+ +H+ +SO42-
C.MgCl2 =Mg2+ +2Cl- D.Ba(OH)2 =Ba2+ +2OH-
95.写出下列化学方程式和离子方程式
㈠NaHSO4溶液中逐滴滴入Ba(OH)2溶液至
①恰好中和,溶液呈中性
离子方程式:
②沉淀完全
离子方程式:
㈡ 碳酸氢钠NaHCO3溶液与少量的氢氧化钙Ca(OH)2溶液反应
离子方程式:
㈢ 碳酸氢钠NaHCO3溶液与足量的氢氧化钙Ca(OH)2溶液反应
离子方程式:
答案:㈠2NaHSO4+Ba(0H)2 = BaSO4↓+Na2SO4+2H2O (每空1分)
2H++SO42-+Ba2++2OH- = BaSO4↓+2H2O
NaHSO4+Ba(0H)2 = BaSO4↓+NaOH+H2O
H++SO42-+Ba2++OH- = BaSO4↓+H2O
㈡ 2NaHCO3+Ca(0H)2 = CaCO3↓+Na2CO3+2H2O
2HCO3-+Ca2++20H- = CaCO3↓+CO32-+2H2O
㈢NaHCO3+Ca(0H)2 = CaCO3↓+NaOH+H2O
HCO3-+Ca2++0H- = CaCO3↓+H2O
94、有一瓶澄清溶液, 可能含有NH4+、K+、Mg2+、Ba2+、Al3+、Fe3+、SO 、CO
、CO 、NO
、NO 、Cl-、I-现进行如下实验:
、Cl-、I-现进行如下实验:
(1)测该溶液显强酸性;
(2)取样加少量四氯化碳和数滴新制氯水、CCl4层为紫红色;
(3)另取样滴加稀NaOH溶液, 使溶液变为碱性, 此过程无沉淀生成;
(4)取少量上述碱性溶液, 加Na2CO3溶液出现白色沉淀;
(5)将实验(3)中的碱性溶液加热, 有气体放出, 该气体能使湿红色石蕊试纸变蓝。
问:(1)原溶液中肯定存在的离子是 ;
(2)肯定不存在的离子是 ;
(3)不能确定是否存在的离子是 。
答案.(1)
(2)
(3)
93、有一瓶溶液只含Cl-、CO32-、SO42-、Na+、NH4+、K+、Mg2+ 七种离子中的某几种。经实验:
 ① 原溶液
① 原溶液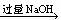 白色沉淀;
白色沉淀;
 ② 将①所得溶液
② 将①所得溶液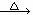 放出使湿润的红色石蕊试纸变蓝的气体;
放出使湿润的红色石蕊试纸变蓝的气体;
 ③ 原溶液中加BaCl2溶液不产生沉淀。
③ 原溶液中加BaCl2溶液不产生沉淀。
 ④ 原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
④ 原溶液中加AgNO3溶液产生白色沉淀,再加稀硝酸白色沉淀不溶解。
 回答下列问题:
回答下列问题:
 (1) 试分析原溶液中一定含有的离子是 ,一定不含有的离子是 ,
可能含有的离子是 。
(1) 试分析原溶液中一定含有的离子是 ,一定不含有的离子是 ,
可能含有的离子是 。
 (2) 有同学认为实验④可以省略,你认为呢?(填“可以”或“不可以”)
,
(2) 有同学认为实验④可以省略,你认为呢?(填“可以”或“不可以”)
,
 并说明理由
。
并说明理由
。
答案:
(1)Mg2+、NH4+、Cl-; CO32-、SO42-; Na+ 、 K+
 (2)可以、 溶液显电中性有阳离子存在必有阴离子存在
(2)可以、 溶液显电中性有阳离子存在必有阴离子存在
92、在反应:2MnO4-+5H2S+6H+=2Mn2++5S↓+8H2O中,电子转移的总数为 ,还原剂为 ,还原产物为 ,当反应中有80g S析出时,有 mol MnO4-被 ,同时有 g H2S被 。
答案:
10e-;H2S;Mn2+;1;还原;85;氧化。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com