
读图2,回答3-5题。

3.下列地区气候类型与甲地相同的是
A.德干高原 B.巴西高原 C.黄土高原 D.伊朗高原
4.乙气候类型区的地带性土壤是
A.棕壤 B.黑土 C.黄壤 D.红壤
5.甲、乙两地可能种植的主要经济作物分别是
 A.咖啡、甜菜
B.花生、咖啡
A.咖啡、甜菜
B.花生、咖啡
C.甜菜、亚麻 D.亚麻、花生
[解析]甲地月均温都在15°C以上,为热带气候类型,降水季节分配不均,为南半球的热带草原气候,对应的地区是巴西高原。乙地月均温在0°C以上,降水的分配比较均匀,为温带海洋性气候,对应的土壤是棕壤。
[答案]3.B 4.A 5.A
图1为地球公转轨道示意图。读图回答1-2题。

1.地球从甲运行到乙期间,重庆的正午太阳高度
A.逐渐减小 B.逐渐增大
C.先减小后增大 D.先增大后减小
[解析]甲处位于近日点附近,为冬至日,从甲运行到乙期间,太阳直射点逐渐北移,因此重庆的正午太阳高度逐渐增大。
[答案]B
2.当地球在甲位置时
A.黄河流域进入汛期 B.南极昆仑站正值极夜
C.三峡水库处于蓄清期 D.潘帕斯草原处于枯黄期
[解析]当地球在甲位置时,为北半球的冬至日,太阳直射在南回归线,黄河流域进入枯水期,南极昆仑站正值极昼,潘帕斯草原处于夏季。三峡水库在汛期6-9月“排浑”,讯末10月,开始蓄水,实现“蓄清”。
[答案]C
本部分共35题,每题4分,共140分。在每题给出的四个选项中,只有一项是最符合题目要求的。
11.(09年山东理综·31)(8分)(化学-化学与技术)
金属铝的生产是以Al2O,为原料,在熔融状态下进行电解:2Al2O3
 4Al+3O2↑
4Al+3O2↑
请回答下列问题:
(1)冰晶石(Na3AIF6)的作用是 。
(2)电解生成的金属铝是在熔融液的 (填“上层”或“下层”)。
(3)阴极和阳极均由 材料做成;电解时不断消耗的电极是 (填“阳极”或“阴极”)。
(4)铝是高耗能产品,废旧铝材的回收利用十分重要。在工业上,最能体现节能减排思想的是将回收铝做成 (填代号)。
a.冰晶石 b.氧化铝 c.铝锭 d.硫酸铝
答案:(1)降低Al2O3的熔化温度 (2)下层(3)碳素(或石墨) 阳极(4)c
 解析:Al2O3的熔点很高,熔化得需要较多能量,加入助熔剂就可节约能量,降低熔化温度
解析:Al2O3的熔点很高,熔化得需要较多能量,加入助熔剂就可节约能量,降低熔化温度
 (2)由于冰晶石(Na3AlF6)与氧化铝熔融物密度比铝的小,所以铝在熔融液的下层。
(2)由于冰晶石(Na3AlF6)与氧化铝熔融物密度比铝的小,所以铝在熔融液的下层。
 (3)电解时阳极的碳棒被生成的氧气氧化。
(3)电解时阳极的碳棒被生成的氧气氧化。
 (4)电解产生的铝要尽量以单质形式存在,所以将回收铝做成铝锭最好。
(4)电解产生的铝要尽量以单质形式存在,所以将回收铝做成铝锭最好。
 [考点分析]考查化学与生活、化学与技术、电解铝的有关问题
[考点分析]考查化学与生活、化学与技术、电解铝的有关问题
12 .(09年天津理综·9)(18分)海水是巨大的资源宝库,在海水淡化及综合利用方面,天津市位居全国前列。从海水中提取食盐和溴的过程如下:
.(09年天津理综·9)(18分)海水是巨大的资源宝库,在海水淡化及综合利用方面,天津市位居全国前列。从海水中提取食盐和溴的过程如下:

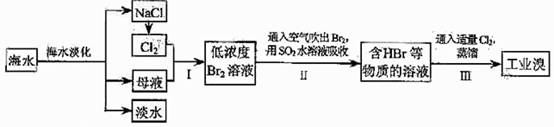
 (1)请列举海水淡化的两种方法: 、 。
(1)请列举海水淡化的两种方法: 、 。
 (2)将NaCl溶液进行电解,在电解槽中可直接得到的产品有H2、 、 、或H2、 。
(2)将NaCl溶液进行电解,在电解槽中可直接得到的产品有H2、 、 、或H2、 。
 (3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br,其目的为
。
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br,其目的为
。
 (4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为 ,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是
。
(4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为 ,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是
。
 (5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,了如下装置简图:
(5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,了如下装置简图:


 请你参与分析讨论:
请你参与分析讨论:
 ①图中仪器B的名称:
。
①图中仪器B的名称:
。
 ②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是
。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是
。
 ③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件:
。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件:
。
 ④C中液体产生颜色为 。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是
。
④C中液体产生颜色为 。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是
。
答案:(1)蒸馏法、电渗析法、离子交换法及其其他合理答案中的任意两种
(2)Cl2 NaOH NaClO
(3)富集溴元素
(4)Br2+SO2+2H2O=4H++SO42-+2Br- 强酸对设备的严重腐蚀
(5)①冷凝管 ②Br2腐蚀橡胶③控制温度计b的温度,并收集59℃的馏分④深红棕色 分液(或蒸馏)
解析:本题考查海水中提取溴的实验。电解NaCl溶液的方程式为:2NaCl + 2H2O  2NaOH+H2↑+Cl2↑,其中Cl2有可能与NaOH会生成NaClO。步骤I中的Br2的浓度很小,多次用SO2反复吸收,最终用Cl2处理,则可获得大量的工业溴。溴具有强氧化性可以氧化SO2,生成H2SO4,因此要注意酸对设备的腐蚀问题。溴具有腐蚀性,可以腐蚀橡胶。蒸馏的目的,就是通过沸点不同而提纯Br2,所以要通过温度计控制好Br2沸腾的温度,尽可能使Br2纯净。
2NaOH+H2↑+Cl2↑,其中Cl2有可能与NaOH会生成NaClO。步骤I中的Br2的浓度很小,多次用SO2反复吸收,最终用Cl2处理,则可获得大量的工业溴。溴具有强氧化性可以氧化SO2,生成H2SO4,因此要注意酸对设备的腐蚀问题。溴具有腐蚀性,可以腐蚀橡胶。蒸馏的目的,就是通过沸点不同而提纯Br2,所以要通过温度计控制好Br2沸腾的温度,尽可能使Br2纯净。
10.(09年宁夏理综·37)[化学-选修化学与技术](15分)
请回答氯碱的如下问题:
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k= (要求计算表达式和结果);
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)③BaCl2,这3种试剂添加的合理顺序是 (填序号)
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
 ①图中X、Y分别是
、 (填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小 ;
①图中X、Y分别是
、 (填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小 ;
②分别写出燃料电池B中正极、负极上发生的电极反应正极: ; 负极: ;
③这样设计的主要节(电)能之处在于(写出2处) 、 。
答案:(1)k=M(Cl2)/2 M(NaOH)=71/80=1:1.13或0.89(2)③①② (3)①Cl2 H2 a%小于b% ②O2+4e-+2H2O=4OH- H2-2e-+2OH-=2H2O ③燃料电池可以补充电解池消耗的电能;提高产出碱液的浓度;降低能耗(其他合理答案也给分)
解析:(1)只要了解电解饱和食盐水的化学方程式2NaCl+2H2O 2NaOH+H2↑+Cl2↑即可得到,k=M(Cl2)/2 M(NaOH)=71/80=1:1.13或0.89;(2)只要抓住除钡离子要放在除碳酸根离子前即可得到顺序关系:③①②;(3)本题突破口在于B燃料电池这边,通空气一边为正极(还原反应),那么左边必然通H2,这样Y即为H2 ;再转到左边依据电解饱和食盐水的化学方程式可知唯一未知的就是X,必然为Cl2了;A中的NaOH进入燃料电池正极再出来,依据O2+4e-+2H2O=4OH- 可知NaOH+浓度增大。
2NaOH+H2↑+Cl2↑即可得到,k=M(Cl2)/2 M(NaOH)=71/80=1:1.13或0.89;(2)只要抓住除钡离子要放在除碳酸根离子前即可得到顺序关系:③①②;(3)本题突破口在于B燃料电池这边,通空气一边为正极(还原反应),那么左边必然通H2,这样Y即为H2 ;再转到左边依据电解饱和食盐水的化学方程式可知唯一未知的就是X,必然为Cl2了;A中的NaOH进入燃料电池正极再出来,依据O2+4e-+2H2O=4OH- 可知NaOH+浓度增大。
[点评]本题前半部基本就是课本内容的再现,但后半部很有创意,可以很好的综合考查考生的原电池和电解的相关知识
9.
 (09年江苏化学·16)(8分)以氯化钾和钛白厂的副产品硫酸亚铁为原料生产硫酸钾、过二硫酸钠和氧化铁红颜料,原料的综合利用率较高。其主要流程如下:
(09年江苏化学·16)(8分)以氯化钾和钛白厂的副产品硫酸亚铁为原料生产硫酸钾、过二硫酸钠和氧化铁红颜料,原料的综合利用率较高。其主要流程如下:


 (1)反应I前需在FeSO4溶液中加入
(填字母),以除去溶液中的Fe3+。
(1)反应I前需在FeSO4溶液中加入
(填字母),以除去溶液中的Fe3+。
 A.锌粉 B.铁屑 C.KI溶液 D.H2
A.锌粉 B.铁屑 C.KI溶液 D.H2
 (2)反应Ⅰ需控制反应温度低于35℃,其目的是
。
(2)反应Ⅰ需控制反应温度低于35℃,其目的是
。
 (3)工业生产上常在反应Ⅲ的过程中加入一定量的醇类溶剂,其目的是
。
(3)工业生产上常在反应Ⅲ的过程中加入一定量的醇类溶剂,其目的是
。
 (4)反应Ⅳ常被用于电解生产(NH4)2S2O8(二硫酸铵)。电解时均用惰性电极,阳极发生地电极反应可表示为
。
(4)反应Ⅳ常被用于电解生产(NH4)2S2O8(二硫酸铵)。电解时均用惰性电极,阳极发生地电极反应可表示为
。
 答案:(1)B
答案:(1)B
 (2)防止NH4HCO3分解(或减少Fe2+的水解)
(2)防止NH4HCO3分解(或减少Fe2+的水解)
 (3)降低K2SO4
的溶解度,有利于K2SO4 析出。
(3)降低K2SO4
的溶解度,有利于K2SO4 析出。
 (4)2SO42-
-2e-
(4)2SO42-
-2e- 2S2O82-
2S2O82-
 解析:(1)在FeSO4溶液中除去溶液中的Fe3+,最好选用铁屑或铁粉,比较简单。(2)如果温度过高会导致NH4HCO3分解同样也会加快Fe2+的水解(温度越高水解速率越快)这样会使原料利用率降低。(3)由题目看出在III反应中生成的K2SO4
为固体,而K2SO4在无机溶剂中溶解度是比较大的,要想使K2SO4析出只能降低其溶解度所以加入醇类溶剂目的降低K2SO4的溶解度。
解析:(1)在FeSO4溶液中除去溶液中的Fe3+,最好选用铁屑或铁粉,比较简单。(2)如果温度过高会导致NH4HCO3分解同样也会加快Fe2+的水解(温度越高水解速率越快)这样会使原料利用率降低。(3)由题目看出在III反应中生成的K2SO4
为固体,而K2SO4在无机溶剂中溶解度是比较大的,要想使K2SO4析出只能降低其溶解度所以加入醇类溶剂目的降低K2SO4的溶解度。
 (4)根据阴阳极反应原理阳极失电子发生氧化反应,此题实质是电解硫酸铵溶液,在根据反应后的产物得出正确的答案。
(4)根据阴阳极反应原理阳极失电子发生氧化反应,此题实质是电解硫酸铵溶液,在根据反应后的产物得出正确的答案。
 [考点分析]此题为化工生产题型,主要考察了化合物性质,电极方程式书写。做此类题要分析清楚每一个环节目的和结果是什么。这样才能判断各反应后的产物分别是什么。
[考点分析]此题为化工生产题型,主要考察了化合物性质,电极方程式书写。做此类题要分析清楚每一个环节目的和结果是什么。这样才能判断各反应后的产物分别是什么。
8.(09年广东化学·24)(11分)
超细氧化铝是一种重要的功能陶瓷原料。
(1)实验室常以NH4Al(SO4)2和NH4HCO3为原料,在一定条件下先反应生成沉淀NH4AlO(OH)HCO3,该沉淀高温分解即得超Al2O3,NH4AlO(OH)HCO3热分解的化学反应方程式 。
(2)NH4Al(SO4)2·12H2O的相对分子质量为453。欲配制100mlPH为2浓度约为0.1mol-1的NH4Al(SO4)2溶液,配制过程为
①用托盘天平称量NH4Al(SO4)2·12H2O固体 g。
②将上述固体置于烧杯中 。
(3)在0.1mol·l-1NH4Al(SO4)2溶液中,铝各形态的浓度(以Al3+计)的对数(lgc)随溶液ph变化的关系见下图

①用NaOH溶液调节(2)中溶液pH至7,该过程中发生反应的离子方程式有 ②请在答题卡的框图中,画出0.01mol·l-1NH4Al(SO4)2溶液中铝各形态的浓度的对数lgc随溶液pH变化的关系图,并进行必要的标注。
答案:(1)2NH4AlO(OH)HCO3 2NH3↑+Al2O3+3H2O↑+2CO2↑(2)将4.5g固体置于烧杯中,边加蒸馏水溶解边用玻璃棒搅拌,待完全溶解后,用玻璃棒移液至100ml的容量瓶中,用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液转移到容量瓶中,加蒸馏水至刻度线2~3cm处应改用胶头滴管,上下振荡,静置,将配置好的溶液装入试剂瓶中,并贴上标签。
2NH3↑+Al2O3+3H2O↑+2CO2↑(2)将4.5g固体置于烧杯中,边加蒸馏水溶解边用玻璃棒搅拌,待完全溶解后,用玻璃棒移液至100ml的容量瓶中,用蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液转移到容量瓶中,加蒸馏水至刻度线2~3cm处应改用胶头滴管,上下振荡,静置,将配置好的溶液装入试剂瓶中,并贴上标签。
(3) 。作图要点:起始与最终数值为-2;刚开始产生沉淀时PH要增大;完全沉淀和沉淀溶解时的PH应与原图一样;氢氧化铝完全溶解时的PH也是不变的二纵座标发生改变,所以线要与原图有所区别。
。作图要点:起始与最终数值为-2;刚开始产生沉淀时PH要增大;完全沉淀和沉淀溶解时的PH应与原图一样;氢氧化铝完全溶解时的PH也是不变的二纵座标发生改变,所以线要与原图有所区别。
解析:(1)解答该题的关键是要判断出反应的产物,由题意NH4AlO(OH)HCO3热分解的产物应该有Al2O3,结合所学知识可知产物还应有NH3、CO2和H2O,配平化学方程式得:2NH4AlO(OH)HCO3 2NH3↑+Al2O3+3H2O↑+2CO2↑
2NH3↑+Al2O3+3H2O↑+2CO2↑
(2)注意配置一定物质的量浓度溶液的操作步骤地准确性,一般是计算、溶解、转移、洗涤、定容、装瓶。计算时要注意规范,同时要注意托盘天平的精确度是±0.1g,100ml 0.1mol/LNH4Al(SO4)2中,物质的量为0.01mol,M[NH4Al(SO4)2]=453g/mol ,所以m(NH4Al(SO4)2)=453g/mol×0.01mol=4.53g=4.5g;溶解时要注意玻璃棒搅拌,转移时注意用到玻璃棒引流,同时还要注意洗涤操作,定容时距刻度2~3cm处应改用胶头滴管,同时还要注意上下震荡,使之混合均匀,装瓶时要注意贴上标签。
(3)①从题给图示可以看出,pH至7时铝离子完全转化为氢氧化铝沉淀,没有出现沉淀的溶解,又因为铵根离子水解使溶液显酸性,所以中性溶液中必须是铵根离子和一水合氨的混合物,说明必需有铵根离子与氢氧根的反应。该过程中发生反应的离子方程式为:Al3+ +3OH-===Al(OH)3↓;NH4+ +OH-=NH3·H2O②作图时注意NH4Al(SO4)2浓度的变化,由于浓度变为0.01mol·l-1,所以起始与最终数值为-2,又因为Al3+浓度减少减少为0.01mol·l-1,而溶度积常数不变,所以刚开始产生沉淀时pH要增大。而完全沉淀和沉淀溶解时的PH应与原图一样不能改变,但注意氢氧化铝完全溶解时的PH也是不变的二纵座标发生改变,所以线要与原图有所区别。
7.


 (09年广东化学·22)(12分)
(09年广东化学·22)(12分)
某工厂生产硼砂过程中产生的固体废料,主要含有MgCO3、MgSiO3、 CaMg(CO3)2、Al2O3和Fe2O3等,回收其中镁的工艺流程如下:

|
沉淀物 |
Fe(OH)3 |
Al(OH)3 |
Mg(OH)2 |
|
pH |
3.4 |
5.2 |
12.4 |
部分阳离子以氢氧化物形式完全深沉时溶液的pH由见上表,请回答下列问题:
(1)“浸出”步骤中,为提高镁的浸出率,可采取的措施有 (要求写出两条)
(2)滤渣I的主要成分有 。
(3)从滤渣Ⅱ中可回收利用的主要物质有 。
(4)Mg(ClO3)2在农业上可用作脱叶剂、催熟剂,可采用复分解反应制备:
MgCl2+2NaClO3===Mg(ClO3)2+2NaCl
已知四种化合物的溶解度(S)随温度(T)变化曲线如下图所示:

①将反应物按化学反应方程式计量数比混合制备Mg(ClO3)2.简述可制备Mg(ClO3)2的原因: 。
②按①中条件进行制备实验。在冷却降温析出Mg(ClO3)2过程中,常伴有NaCl析出,原因是: 。除去产品中该杂质的方法是: 。
答案:(1)增大硫酸浓度;加热升高温度;边加硫酸边搅拌(要求写出两条)
(2)滤渣Ⅰ主要成分有Fe(OH)3、Al(OH)3
(3)从滤液Ⅱ中可回收利用的主要物质有CaSO4、Na2SO4
(4)①该反应的生成物为Mg(ClO3)2和NaCl的混合溶液,NaCl的溶解度随温度变化不大,Mg(ClO3)2的溶解度随温度升高而升高。利用两物的溶解度差异,通过加热蒸发浓缩,冷却结晶,过滤,将Mg(ClO3)2与NaCl分离,制得Mg(ClO3)2。
②因为在相同温度向下NaCl的溶解度最小,所以在冷却结晶过程中,会有少量NaCl随Mg(ClO3)2析出;重结晶。
解析:(1)固体溶解及反应完全的措施一般是加热、振荡或搅拌,或是增大硫酸的浓度,所以答案应该从这些方面分析回答。
(2)从题给信息可以看出pH调到5.5应该Fe3+和Al3+沉淀完全,所以沉淀应该是氢氧化铁和氢氧化铝。
(3)从流程变化,因为废料浸出用到硫酸,可知滤液中应该含有硫酸根离子;从废料成分中含有CaMg(CO3)2和两次调节PH均用到氢氧化钠,可知滤液中阳离子应该有钠离子和钙离子,所以从滤渣Ⅱ中可回收利用的主要物质是硫酸钠和硫酸钙。
(4)①分析该题可以结合硝酸钾与氯化钠的分离方法思考,同时要注意题给图示,从图示上我们不难得到下列信息,一是相同温度时氯酸镁的溶解度最大氯化钠溶解度最小,二是氯酸镁溶解度随温度变化最大,氯化钠溶解度随温度变化最小。所以控制反应温度的变化,可以控制可溶性物质的分离。
②从题给图示不难看出相同温度时氯化钠的溶解度最小,因此在冷却降温析出Mg(ClO3)2过程中一定会析出氯化钠。由于氯酸镁和氯化钠均溶于水,溶于水的可溶性物质一般用结晶和重结晶的方法分离。
6. (09年海南化学·20.4)(11分)
(09年海南化学·20.4)(11分)
 工业上常用氨氧化法生产硝酸,其过程包括氨的催化氧化(催化剂为铂铑合金丝网)、一氧化氮的氧化和水吸收二氧化氮生成硝酸。请回答下列问题:
工业上常用氨氧化法生产硝酸,其过程包括氨的催化氧化(催化剂为铂铑合金丝网)、一氧化氮的氧化和水吸收二氧化氮生成硝酸。请回答下列问题:
 (1)氨催化氧化的化学方程式为
:
(1)氨催化氧化的化学方程式为
:
 (2)原料气中空气必须过量,其主要原因是
;
(2)原料气中空气必须过量,其主要原因是
;
 (3)将铂铑合金做成薄丝网的主要原因是
;
(3)将铂铑合金做成薄丝网的主要原因是
;
 (4)水吸收二氧化氮生成硝酸为放热反应,其化学方程式为
,为了提高水对二氧化氮的吸收率,可采取的措施为
(答2项)。
(4)水吸收二氧化氮生成硝酸为放热反应,其化学方程式为
,为了提高水对二氧化氮的吸收率,可采取的措施为
(答2项)。
答案:(11分)
(1)4NH3+5O2 4NO+6H2O
4NO+6H2O (3分)
(3分)
 (2)提高氨的转化率和一氧化氮的转化率(2分)
(2)提高氨的转化率和一氧化氮的转化率(2分)
 (3)增大单位质量的催化剂与反应物的接触面积(2分)
(3)增大单位质量的催化剂与反应物的接触面积(2分)
 (4)3NO2+H2O=2HNO3+NO 加压 降温(4分)
(4)3NO2+H2O=2HNO3+NO 加压 降温(4分)
解析:(1)

(2)根据平衡原理,增大反应物的浓度,平衡向正反应方向移动,以提高原料的转化率;
(3)这是为了增大铂铑合金的表面积,使接触面积增大,提升催化的效果;
(4)为了提高吸收率,可根据溶解过程放热采用降温处理,且气体的吸收可用加压的方式。
5.(10分)(08年江苏化学·15)金矿开采、冶炼和电镀工业会产生大量含氰化合物的污水,其中含氰化合物以HCN、CN -和金属离子的配离子M(CN)nm-的形式存在于水中。测定污水中含氰化合物含量的实验步骤如下:
①水样预处理:水样中加入磷酸和EDTA,在pH<2的条件下加热蒸馏,蒸出所有的HCN,并用NaOH溶液吸收。
②滴定:将吸收液调节至pH>11,以试银灵作指示剂,用AgNO3标准溶液滴定
 Ag++2CN - == [Ag(CN)2]
-
Ag++2CN - == [Ag(CN)2]
-
终点时,溶液由黄色变成橙红色。
根据以上知识回答下列问题:
(1)水样预处理的目的是 。
(2)水样预处理的装置如右图,细导管插入吸收液中是为了
。
(3)蒸馏瓶比吸收液面要高出很多,其目的是 。
(4)如果用盐酸代替磷酸进行预处理,实验结果将
(填“偏高”、“无影响”或“偏低”)。
(5)准确移取某工厂污水100 mL,经处理后用浓度为0.01000 mol·L-1的硝酸银标准溶液滴定,终点时消耗了21.00 mL。此水样中含氰化合物的含量为 mg·L-1的(以计,计算结果保留一位小数)。
答案:(10分)(1)将含氰化合物全部转化为CN - (2)完全吸收HCN,防止气体放空 (3)防止倒吸 (4)偏高 (5)109.2
解析:水样预处理的目的是,将污水中含的氰化合物HCN、CN -和金属离子的配离子M(CN)nm-的形式全部转化成HCN,然后用NaOH溶液吸收将HCN全部转化为CN -,很明显将细导管插入吸收液中是为了充分吸收HCN,防止气体排到空气中,引起大气污染,但同时可能产生倒吸现象,为防止倒吸,可以将蒸馏瓶升至比吸收液面要高出很多。如果用盐酸代替磷酸进行预处理,用AgNO3标准溶液滴定时,氯离子也消耗银离子,实验结果将偏高。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com