
28.(1995年全国,35)取50.0 mL Na2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后得到14.51 g白色沉淀,用过量稀硝酸处理后沉淀量减少到4.66 g,并有气体放出。试计算:
(1)原混合液中Na2CO3和Na2SO4的物质的量浓度;
(2)产生的气体在标准状况下的体积。
27.(1996年全国,36)将a mol H2S和1 mol O2置于一个容积可变的容器内进行反应。维持容器内气体的压强不变(101 kPa),在120 ℃下测得反应前后容器内气体的密度分别为d1和d2。若a的取值不同,则H2S的氧化产物可能有如下三种情况:
(1)全部是SO2,此时a的取值范围是________。
(2)全部是S,此时a的取值范围是________,并且d1________d2(填“小于”“大于”或“等于”)。
(3)部分是SO2,部分是S,此时a的取值范围是________。
反应所生成的SO2的物质的量为________ mol。
容器内气体的物质的量之和为________ mol。(以含a的代数式表示)
26.(1997年上海,36)接触法制硫酸排放的尾气中含少量的SO2,为防止污染大气,在排放前设法进行综合利用。
(1)某硫酸厂每天排放的10000 m3尾气中含0.2%(体积分数)的SO2,问用NaOH溶液、石灰及O2处理后,假设硫元素不损失,理论上可得到多少千克石膏(CaSO4·2H2O)?
(2)如果将一定体积的尾气通入100 mL 2 mol·L-1的NaOH溶液中使其完全反应,经测定所得溶液含16.7 g溶质。试分析该溶液的成分,并计算确定各成分的物质的量。
(3)工厂在尾气处理制石膏的过程中,中间产物是NaHSO3。调节尾气排放的流量,以取得SO2与NaOH间物质的量的最佳比值,从而提高亚硫酸氢钠的产量。现设n(SO2)、n(NaOH)、n(NaHSO3)分别表示SO2、NaOH和NaHSO3的物质的量,且 =x,试写出x在不同取值范围时,n(NaHSO3)的值或n(NaHSO3)与n(SO2)、n(NaOH)间的关系式。
=x,试写出x在不同取值范围时,n(NaHSO3)的值或n(NaHSO3)与n(SO2)、n(NaOH)间的关系式。

25.(1997年全国,35)8.8 g FeS固体置于200 mL 2.0 mol·L-1的盐酸中,以制备H2S气体。反应完全后,若溶液中H2S的浓度为0.10 mol·L-1,假定溶液体积不变,试计算:
(1)收集到的H2S气体的体积(标准状况)。
(2)溶液中Fe2+和H+的物质的量浓度(摩尔浓度)。
24.(1997年全国,31)某无色溶液可能含有下列钠盐中的几种:A.氯化钠 B.硫化钠 C.亚硫酸钠 D.硫代硫酸钠 E.硫酸钠 F.碳酸钠。向此溶液中加入适量稀H2SO4,有浅黄色沉淀析出,同时有气体产生,此气体有臭鸡蛋气味,可使澄清的石灰水变浑浊,不能使品红试液褪色。根据上述实验现象回答下列问题。
(1)不能使品红试液褪色,说明该气体不含 (填分子式)。
(2)此无色溶液中至少存在哪几种钠盐?请写出全部可能的情况(填写相应的字母)。第一种情况 ,第二种情况 ,第三种情况 ,第四种情况 (可不填满,也可补充)。
23.(1998年上海,28)汽车尾气(含有烃类、CO、SO2与NO等物质)是城市空气的污染源,治理的方法之一是在汽车的排气管上装一个“催化剂转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及SO2的转化。
(1)写出CO与NO反应的化学方程式 。
(2)“催化剂转换器”的缺点是在一定程度上提高空气的酸度。其原因是 。
(3)控制城市污染源的方法可以有 (多选扣分)。
a.开发氢能源 b.使用电动车
c.植树造林 d.戴上呼吸面具
22. (2000年全国,23)某学生课外活动小组利用右图所示装置分别做如下实验:
(2000年全国,23)某学生课外活动小组利用右图所示装置分别做如下实验:
(1)在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是_________溶液;加热时溶液由红色逐渐变浅的原因是: 。
(2)在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是_________溶液;加热时溶液由无色变为红色的原因是: 。
21.(2002年上海,31)硫铁矿高温下空气氧化产物二氧化硫,4FeS2+11O2===8SO2+2Fe2O3设空气中N2、O2的含量分别为0.800和0.200(体积分数,以下气体含量均用体积分数表示),试完成下列各题:
(1)1.00 mol FeS2完全氧化,需要空气的体积(标准状况)为________L。
(2)55 L空气和足量FeS2完全反应后,气体体积(同温同压)变为________L。
(3)用空气氧化FeS2产生的气体混合物中,O2含量为0.0800,计算SO2的含量。
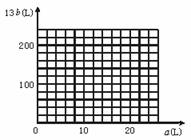
(4)设FeS2氧化产物的气体混合物为100 L,其中O2为a L,SO2为b L。
①写出a和b的关系式
②在图中画出a和b的关系曲线(FeS2氧化时,空气过量20%)
说明:为方便作图,纵坐标用13b表示。
20.(1995年上海,24)为方便某些化学计算,有人将98%浓硫酸表示成下列形式,其中合理的是
A.H2SO4·1/9H2O B.H2SO4·H2O
C.H2SO4·SO3 D.SO3·10/9H2O
19.(1995年全国,26)某温度下,在100 g水中加入m g CuSO4或加入n g CuSO4·5H2O,均可使溶液恰好达到饱和,则m与n的关系符合
A.m= n B.m=
n B.m=
C.m= D.m=
D.m=
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com