
27. (8·Ö)ÔÚĂܱƠÈƯÆ÷ÖĐ£¬Ê¹2molN2ºÍ6molH2»́ºÏ·¢ÉúÏÂÁĐ·´Ó¦£º
¡¡¡¡ N2(g)+3H2(g)===2NH3(g)(Ơư·´Ó¦Îª·ÅÈÈ·´Ó¦)
(1)µ±·´Ó¦´ïµ½Æ½ºâʱ£¬N2ºÍH2µÄŨ¶È±ÈÊÇ_______£»N2ºÍH2µÄת»¯ÂʱÈÊÇ_________¡£
(2)Éư¸ßƽºầåϵµÄζÈ(±£³Ö̀å»ư²»±ä)£¬»́ºÍÆø̀åµÄƽ¾ùÏà¶Ô·Ö×ÓÖÊÁ¿_______£¬ĂܶÈ________¡£(̀î¡°±ä´ó¡±¡¢¡°±äĐ¡¡±»̣¡°²»±ä¡± )
(3)µ±´ïµ½Æ½ºâʱ£¬½«C(N2)¡¢C(H2)¡¢C(NH3)ͬʱ¼ơĐ¡̉»±¶£¬Æ½ºâ½«Ị̈______̉ƶ¯¡£
(4)µ±´ïµ½Æ½ºâʱ£¬³äÈëë²Æø£¬²¢±£³Öѹǿ²»±ä£¬Æ½ºâ½«Ị̈_________̉ƶ¯¡£
(5)ÈôÈƯÆ÷ºăÈƯ£¬¾øÈÈ¡¢¼ÓÈÈʹÈƯÆ÷ÄÚζÈѸËÙÉưÖÁÔÀ´µÄ2±¶£¬Æ½ºâ½«_______
(̀î¡°Ị̈×ó̉ƶ¯¡±¡°Ị̈Ó̉̉ƶ¯¡±»̣¡°²»̉ƶ¯¡±)¡£´ïµ½ĐÂƽºâºó£¬ÈƯÆ÷ÄÚζÈ_______(̀î¡°´óÓÚ¡±¡°Đ¡ÓÚ¡±»̣¡°µÈÓÚ¡±)ÔÀ´µÄ2±¶¡£
26.(6·Ö)ÔÚ̉»¶῭ơ¼₫Ï·´Ó¦2SO2(g)+O2(g)===2SO3(g)´ïµ½Æ½ºâ×´̀¬µÄ±êÖ¾ÊÇ_______________________________¡£
¢ÙijÎïÖʺ¬Á¿²»±ä¡¡ ¢ÚijÎïÖÊת»¯Âʲ»±ä¡¡ ¢ÛijÎïÖÊŨ¶È²»±ä¡¡ ¢ÜºăÈƯѹǿ²»±ä¢Ưºăѹ̀å»ư²»±ä¡¡ ¢̃ v(Ơư)= v(Äæ)¢ß̀ơ¼₫̉»¶¨£¬Æ½¾ùÏà¶Ô·Ö×ÓÖÊÁ¿²»±ä¡¡ ¢à̀å»ử»¶¨£¬Æø̀åĂܶȲ»±ä
ÉÏÊö̀ơ¼₫·ûºÏ£ºH2(g)+ I2(g)===2HI(g)·´Ó¦´ïƽºâµÄÓĐ_____________£»ÉÏÊö̀ơ¼₫·ûºÏ£ºA(g)+B(l)===C(g)·´Ó¦´ïƽºâµÄÓĐ_____________________¡£
25.(6·Ö)ĂܱỜåϵÖĐ·¢ÉúÏÂÁĐ·´Ó¦£ºN2 + 3H2 ==== 2NH3(Ơư·´Ó¦Îª·ÅÈÈ·´Ó¦)£¬
ÈçͼÊÇij̉»Ê±¼ä¶Î·´Ó¦ËÙÂÊÓë·´Ó¦½ø³̀µÄÇúÏß¹Øϵͼ¡£¡¡¡¡ ¡¡
 »Ø´đÏÂÁĐÎỀ⣺¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
v
»Ø´đÏÂÁĐÎỀ⣺¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
v
(1)´¦ÓÚƽºâ×´̀¬µÄʱ¼ä¶ÎÊÇ_______________¡¡¡¡¡¡¡¡¡¡¡¡ v(Äæ)


 __________________________________________¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡v(Äæ)¡¡
__________________________________________¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡v(Äæ)¡¡


 (2)t1¡¢t3¡¢t4ʱ¿̀£¬̀åϵÖĐ·Ö±đÊÇÊ²Ă´̀ơ¼₫·¢ÉúÁ˱仯£¿ ¡¡¡¡¡¡V(Ơư)
(2)t1¡¢t3¡¢t4ʱ¿̀£¬̀åϵÖĐ·Ö±đÊÇÊ²Ă´̀ơ¼₫·¢ÉúÁ˱仯£¿ ¡¡¡¡¡¡V(Ơư)
 ¡¡ t1£º_______ ¡¡t3£º_______¡¡ t4£º_________¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡V(Ơư)¡¡¡¡¡¡¡¡
¡¡ t1£º_______ ¡¡t3£º_______¡¡ t4£º_________¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡V(Ơư)¡¡¡¡¡¡¡¡
 ¡¡ (3)ÏÂÁĐʱ¼ä¶ÎÖĐ£¬°±µÄ°Ù·Öº¬Á¿×î¸ßµÄÊÇ________¡¡ ¡¡¡¡t 0¡¡ t1¡¡ t2¡¡ t3 ¡¡t4 ¡¡t5¡¡ t6¡¡
¡¡ (3)ÏÂÁĐʱ¼ä¶ÎÖĐ£¬°±µÄ°Ù·Öº¬Á¿×î¸ßµÄÊÇ________¡¡ ¡¡¡¡t 0¡¡ t1¡¡ t2¡¡ t3 ¡¡t4 ¡¡t5¡¡ t6¡¡
¡¡ A¡¢t 0~t1¡¢¡¡¡¡ B¡¢t2~t3¡¡¡¡¡¡¡¡ C¡¢t3~t4¡¡ ¡¡¡¡ ¡¡¡¡D¡¢t5~t6
24£®(8·Ö)»¯Ñ§Æ½ºẩƶ¯ÔÀíͬÑù̉²ÊÊÓĂÓÚÆäËûƽºâ£¬̉ÑÖªÔÚ°±Ë®ÖĐ´æÔÚÏÂÁĐƽºâ£º
NH3+H2O===NH3.H2O===NH4++OH-
(1)Ị̈°±Ë®ÖĐ¼ÓÈëMgCl2¹̀̀åʱ£¬Æ½ºâỊ̈______________̉ƶ¯£¬OH-µÄŨ¶È_______£¬
NH4+µÄŨ¶È_______¡£
(2)Ị̈°±Ë®ÖĐ¼ÓÈëŨÑÎËᣬ´ËʱÈÜ̉ºÖĐŨ¶È¼ơĐ¡µÄ΢Á£ÓĐ_______¡¢_______¡¢_______¡£
(3)Ị̈Ũ°±Ë®ÖĐ¼ÓÈëÉÙÁ¿µÄNaOH¹̀̀壬ƽºâỊ̈_______̉ƶ¯£¬´Ëʱ·¢ÉúµÄÏÖÏóÊÇ______________
______________¡£
23.(3·Ö)¶ÔÓÚÈÜ̉ºÖĐ½øĐеķ´Ó¦£ºFeCl3+3KSCN===Fe(SCN)3+3KCl,µ±ÆäËû̀ơ¼₫̉»¶¨Ê±£º
(1)Ị̈ÈÜ̉ºÖĐ¼ÓÈëÉÙÁ¿µÄKCl¹̀̀壬ÈÜ̉ºµÄÑƠÉ«_______
(2)Ị̈ÈÜ̉ºÖĐ¼ÓÈëÉÙÁ¿KSCN¹̀̀壬ÈÜ̉ºµÄÑƠÉ«_______
(3)¼ÓˮϡÊÍʱ£¬»¯Ñ§Æ½ºâỊ̈_______̉ƶ¯
22.(5·Ö)ÔÚĂܱƠÈƯÆ÷ÖĐ£¬µ±ºÏ³É°±µÄ·´Ó¦N2+3H2===2NH3(Ơư·´Ó¦ÊÇ·ÅÈÈ·´Ó¦)´ïµ½Æ½ºâʱ£¬¸Ä±äÈçϵÄ̉»Đ©̀ơ¼₫£º
(A)ÉưΣ¬(B)¼Óѹ£¬(C)¼ơѹ£¬(D)Ôö´óc(H2)£¬(E)¼ơĐ¡c(NH3)£¬(F)Ôö´óc(NH3)£¬ÈôƽºâỊ̈Ó̉̉ƶ¯ÓĂ¡° ¡ú¡±£¬ÈôƽºâỊ̈×ó̉ƶ¯ÓĂ¡°¡û¡±±íʾ£»ÈôÖµÔö¼ÓÓĂ¡°¡ü¡±±íʾ£¬ÈôÖµ¼ơĐ¡ÓĂ¡°¡ư¡±±íʾ£¬Çë¸ù¾ƯϱíÖи÷ÏîµÄ±ä»¯Çé¿ö£¬Ôڸıä̀ơ¼₫À¸Ä¿ÖĐ̀îÉÏÏàÓ¦µÄ±àºÅ(Ă¿ÏîÖ»¸Ä±ä̉»¸ö̀ơ¼₫)¡£
|
񅧏 |
¸Ä±ä̀ơ¼₫ |
ƽºẩƶ¯·½Ị̈ |
N2µÄת»¯ÂÊ |
C(NH3) |
C(N2) |
C(H2) |
|
¢Ù |
¡¡ |
¡ú |
¡ü |
¡ư |
¡ư |
¡ư |
|
¢Ú |
¡¡ |
¡û |
¡ư |
¡ư |
¡ü |
¡ü |
|
¢Û |
¡¡ |
¡ú |
¡ü |
¡ü |
¡ư |
¡ü |
|
¢Ü |
¡¡ |
¡û |
¡ư |
¡ư |
¡ư |
¡ư |
|
¢Ư |
¡¡ |
¡ú |
¡ü |
¡ü |
¡ü |
¡ü |
21.(3·Ö)¶ÔÓÚ·´Ó¦£º2SO2+O2===2SO3£¬µ±ÆäËû̀ơ¼₫²»±äʱ£¬Ö»¸Ä±ä̉»¸ö·´Ó¦̀ơ¼₫£¬½«Éú³ÉSO3µÄ·´Ó¦ËÙÂʵı仯̀îÈëϱí¿Ơ¸ñÀï(̀î¡°Ôö´ó¡±¡¢¡°¼ơĐ¡¡±»̣¡°²»±ä¡±)
|
񅧏 |
¸Ä ±ä µÄ ̀ơ ¼₫ |
Éú³ÉSO3µÄËÙÂÊ |
|
¢Ù |
Éư¸ßÎÂ¶È |
¡¡ |
|
¢Ú |
ºăѹϳäÈëNe |
¡¡ |
|
¢Û |
Ôö´óO2µÄŨ¶È |
¡¡ |
|
¢Ü |
ʹÓĂ´ß»¯¼Á |
¡¡ |
|
¢Ư |
ѹËờå»ư |
¡¡ |
|
¢̃ |
ºăÈƯϳäÈëNe |
¡¡ |
20. ¶ÔÓÚ¿ÉÄæ·´Ó¦£ºmA(s)+ nB(g)=== eC(g)+ f D(g)£¬·´Ó¦¹ư³̀ÖĐ£¬²»Í¬Î¶È(T1¡¢T2)»̣²»Í¬Ñ¹Ç¿(P1¡¢P2)ʱ£¬·´Ó¦»́ºÏÎïÖĐBµÄ̀å»ư·ÖÊư[¦×(B)]Óëʱ¼ä(t)µÄ¹ØϵÇúÏßÈçÏÂͼËùʾ(¼ÙÉè·´Ó¦¿ªÊ¼Ê±Ö»ÓĐAºÍB)£º
¡¡¡¡¡¡ ¦×(B)¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¦×(B)




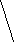 ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
 ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡P1
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡P1

 ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
T1¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡P2
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
T1¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡P2
 ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
T2
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
T2

 ¡¡¡¡¡¡ O¡¡¡¡¡¡¡¡¡¡¡¡¡¡
t(s)¡¡¡¡¡¡¡¡¡¡¡¡
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡O¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡t(s)¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¼×¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ̉̉
¡¡¡¡¡¡ O¡¡¡¡¡¡¡¡¡¡¡¡¡¡
t(s)¡¡¡¡¡¡¡¡¡¡¡¡
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡O¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡t(s)¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡
¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¼×¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ̉̉
ÏÂÁĐÓĐ¹ØĐđÊöÖĐƠưÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
¡¡A. ʹÓĂÊỂ˵Ĵ߻¯¼Á£¬CµÄ̀å»ư·ÖÊư½«Ôö´ó
¡¡B. ·´Ó¦·½³̀ʽÖĐ»¯Ñ§¼ÆÁ¿ÊưµÄ¹ØϵÊÇm + n ¡µe + f
¡¡C. Éư¸ßζȣ¬Æ½ºâ½«Ị̈Äæ·´Ó¦·½Ị̈̉ƶ¯
¡¡D. AµÄ¿ÅÁ£Ô½Đ¡£¬Ô½ÓĐÀûÓÚƽºâỊ̈Ơư·´Ó¦·½Ị̈̉ƶ¯
ÑÅ°²ÖĐѧ2010-2011ѧÄê(ÉÏÆÚ)¸ß¶₫Ä꼶Ô¿¼(9ÔÂ)
»¯¡¡ ѧ¡¡ ÊÔ¡¡ ̀â
µÚ¢̣¾í¡¡ ·ÇÑ¡Ôñ̀â(50·Ö)
19. ÔÚ̉»¶῭ơ¼₫Ï£¬¿ÉÄæ·´Ó¦£ºX(g)+ 3Y(g)===2Z(g)£¬´ïµ½Æ½ºâʱÓĐ37.5%µÄYת»¯ÎªZ£¬ÓĐ25%µÄXת»¯ÎªZ¡£ỘÆđʼʱ£¬³äÈëÈƯÆ÷ÖеÄXºÍYµÄÎïÖʵÄÁ¿±ÈΪ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
¡¡ A. 1 : 3¡¡¡¡ B. 3 : 1¡¡¡¡¡¡ C. 3 : 2¡¡¡¡¡¡ D. 1 : 2
18. ¶ÔÓÚ¿ÉÄæ·´Ó¦£º2A(g)+ 3B(g)===3C(g)£¬ÔÚ̉»¶῭ơ¼₫Ï£¬Ê¹̉»¶¨Á¿AºÍB·´Ó¦´ïµ½Æ½ºâ×´̀¬Ê±£¬¾ßÓеÄĐÔÖÊÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
¡¡ A. ¸÷ÎïÖÊŨ¶È±ÈΪc(A) : c(C) = 2 : 3 : 3¡¡
¡¡ B. ÔÚζȡ¢Ñ¹Ç¿²»±äʱ£¬Æ½ºâ»́ºÏÎïµÄ̀å»ưÊÇ·´Ó¦¿ªÊ¼Ç°µÄ
¡¡ C. ƽºâ»́ºÏÎïÖи÷ÎïÖʵÄŨ¶ÈÏàµÈ¡£
¡¡ D. µ¥Î»Ê±¼äÄÚ£¬ÈôÏûºÄÁËa mol AÎïÖÊ£¬Í¬Ê±̉²ÏûºÄÁË1.5a mol CÎïÖÊ
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com