
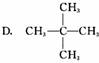
5.某烷烃相对分子质量为72,与Cl2起反应生成的一氯取代物只有一种,其结构简式是( )
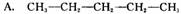
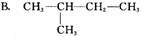
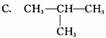
4.按系统命名法下列名称不正确的是 ( )
A.1一甲基丙烷 B.2一甲基丙烷 C.2,2一二甲基丙烷 D.3一乙基庚烷
3.已知二氯苯的同分异构体有3种,从而推知四氯苯的同分异构体数目是 ( )
A.2种 B.3种 C.4种 D.5种
2.下列各组物质,两者互为同分异构体的是 ( )
A.NH4CNO和CO(NH2)2 B.CuSO4·3H2O和CuSO4·5H2O
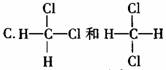 D.H2O和D2O(重水)
D.H2O和D2O(重水)
1.某有机物在氧气中充分燃烧,生成等物质的量的二氧化碳和水。则该有机物的组成必须满足的条件是 ( )
A.分子中C、H、O的个数比为1:2:3 B.分子中C、H的个数比为1:2
C.该有机物的相对分子质量为14 D.该分子中肯定不含氧
1、下列说法正确的是
A、需要加热方能发生的反应一定是吸热反应
B、放热的反应在常温下一定很易发生
C、反应是放热的还是吸热的必须看反应物和生成物所具有的总能量的相对大小
D、吸热反应在一定的条件下也能发生
•2、反应C(石墨) → C(金刚石)是吸热反应,由此可知
•A、石墨比金刚石更稳定
•B、金刚石和石墨可以相互转化
•C、金刚石比石墨稳定
•D、金刚石和石墨不能相互转化
3、H2 + F2 = 2HF H2 + Cl2 = 2HCl 预测当生成2 mol HF和2 mol HCl时,哪个反应放出的热量多?

若干化学键的键能( kJ/mol,25 ℃ )
2、你所知道的化学反应中有哪些是吸热反应?能作一个简单的总结吗?
多数的分解反应、氯化铵固体与氢氧化钡晶体的反应、水煤气的生成反应、炭与二氧化碳生成一氧化碳
反应物具有的总能量 < 生成物具有的总能量
当能量变化以热能的形式表现时:
我们知道:一个化学反应同时遵守质量守恒定律和能量守恒,那么一个反应中的质量与能量有没有关系呢?
有能量的释放或吸收是以发生变化的物质为基础,二者密不可分,但以物质为主。
能量的多少则以反应物和产物的质量为基础。那么化学反应中能量到底怎样变化
2:反应热,焓变
化学反应过程中为什么会有能量的变化?(用学过的知识回答)
化学反应的实质就是反应物分子中化学键断裂,形成新的化学键,从新组合成生成物的分子的过程。旧键断裂需要吸收能量,新键形成需要放出能量。而一般化学反应中,旧键的断裂所吸收的总能量与新键形成所放出的总能量是不相等的,而这个差值就是反应中能量的变化。所以化学反应过程中会有能量的变化。
反应热 焓变
化学反应过程中所释放或吸收的能量,都可以热量(或换算成相应的热量)来表述,叫做反应热,又称为“焓变”。符号: ΔH ,单位:kJ/mol 或 kJ•mol-1
∆H为“-” 为放热反应∆H为“+” 为吸热反应
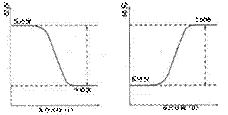 思考:能量如何转换的?能量从哪里转移到哪里?体系的能量如何变化?升高是降低?环境的能量如何变化?升高还是降低?规定放热反应的ΔH
为“-”,是站在谁的角度?体系还是环境
思考:能量如何转换的?能量从哪里转移到哪里?体系的能量如何变化?升高是降低?环境的能量如何变化?升高还是降低?规定放热反应的ΔH
为“-”,是站在谁的角度?体系还是环境
放热反应ΔH为“-”或ΔH〈 0 吸热反应ΔH为“+”或ΔH 〉0
∆H=E(生成物的总能量)- E(反应物的总能量)
∆H=E(反应物的键能)- E(生成物的键能)
3:练习1)1molC与1molH2O(g)反应失成lmol CO(g)和1mol H2(g),需要吸收131.5kJ的热量,该反应的反应热为△H= kJ/mol。
2)拆开 lmol H-H键、lmol N-H键、lmolN≡N键分别需要的能量是436kJ、391kJ、946kJ,则1mol N2生成NH3的反应热为 ,1mol H2生成NH3的反应热为 。
1、你所知道的化学反应中有哪些是放热反应?能作一个简单的总结吗?
活泼金属与水或酸的反应、酸碱中和反应、燃烧反应、多数化合反应
反应物具有的总能量 > 生成物具有的总能量
27.室温下,某密闭容器中盛有甲烷与氧气的混合气体。已知混合气体中碳元素的质量分数为12.5%,将此混合气体点燃引爆后,冷却至原温度,求反应容器中的混合气体对氢气的相对密度。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com