
3.乙醇结构与性质方面的说法中正确的是( )
A.乙醇结构中有-OH,所以乙醇溶解于水,可以电离出OH-而显碱性
B.乙醇中的羟基可以和钠反应,同样也可以和氢氧化钠溶液反应
C.乙醇与钠反应可以产生氢气,所以乙醇显酸性
D.乙醇与钠反应非常平缓,所以乙醇羟基上的氢原子不如水中的氢原子活泼
2.能证明乙醇分子中含有一个羟基的事实是( )
A.乙醇完全燃烧生成水 B.0.1mol乙醇与足量金属钠反应生成0.05molH2
C.乙醇能与水以任意比例互溶 D.乙醇容易挥发
1.下列有关乙醇的物理性质的应用中不正确的是 ( ) A.由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去
B.由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中药的有效成分
C.由于乙醇能够以任意比溶解于水,所以酒厂可以勾兑各种浓度的酒
D.由于乙醇容易挥发,所以才有熟语“酒香不怕巷子深”的说法
3、在有机化学中常用反应物的得氧或得氢来判断氧化还原反应。有机物得氧或失氢的反应叫做氧化反应;有机物得氢或失氧的反应叫做还原反应。
[思考与交流]铜丝放在酒精灯外焰灼烧,慢慢移向内焰,上下几次。观察铜丝的变化。
红-黑-红
[讲]乙醇能使酸性高锰酸钾和重铬酸钾褪色,乙醇被直接氧化生成乙酸
[板书](3) 直接氧化-生成乙酸
[知识拓展]醇催化氧化的规律:
①与羟基(-OH)相连碳原子上有两个氢原子的醇(-OH在碳链末端的醇),被氧化生成醛。
2R-CH2-CH2OH+O2
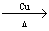 2R-CH2-CHO+2H2O
2R-CH2-CHO+2H2O
②与羟基(-OH)相连碳原子上有一个氢原子的醇(-OH在碳链中间的醇),被氧化生成酮。
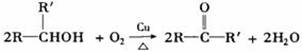
③与羟基(-OH)相连碳原子上没有氢原子的醇不能被催化氧化。
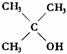 不能形成
不能形成 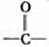 双键,不能被氧化成醛或酮。
双键,不能被氧化成醛或酮。
[过]请大家回忆实验室制乙烯的方法,我们知道,乙醇在浓H2SO4作催化剂和脱水剂的条件下,加热到170℃即生成乙烯,该反应属于消去反应。因此乙醇还可以发生消去反应。
[板书]3、脱水
(1) 分子内脱水---消去反应-实验室制乙烯
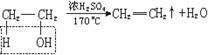
[注意]①分子中至少有两个C原子,如CH3OH就不能发生消去反应;
②羟基所连C原子的相邻C上要有H原子,否则不能发生消去反应。
[讲]消去反应是从一个分子内脱去一个小分子而形成不饱和化合物的反应。如将该反应的温度控制在140℃,则发生分子间脱水生成乙醚
[板书](2) 分子间脱水-取代反应
CH3CH2OH+HOCH2CH3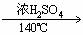 C2H5-O-C2H5
+H2O
C2H5-O-C2H5
+H2O
[讲]乙醚是醚类中最重要的一种。凡是两个烃基通过一个氧原子连结起来的化合物叫做醚。醚的通式是R-O-R',R和R'都是烃基,可以相同,也可以不同。乙醚是一种无色易挥发的液体,沸点是4.51 ℃,有特殊的气味。吸入一定量的乙醚蒸气,会引起全身麻醉,所以纯乙醚可用作外科手术时的麻醉剂。乙醚微溶于水,易溶于有机溶剂,它本身是一种优良溶剂,能溶解许多有机物。乙醚蒸气很容易着火,空气中如果混有一定比的乙醚蒸气,遇火就会发生爆炸,所以使用乙醚时要特别小心。
[知识拓展]实验室常用固体NaBr、浓H2SO4和乙醇共热来制取溴乙烷,这利用的是乙醇与卤代烃的取代反应。该反应中断的是C-OH键。
[板书]4、与氢卤酸反应--- 取代反应
C2H5OH+HBr
 C2H5Br+H2O
C2H5Br+H2O
[投影小结]乙醇结构与性质关系

[过]乙醇在生产、生活中的用途十分广泛,用量也很大,下面让我们来一起研究一下乙醇的工业制法
[板书]四、乙醇的工业制法
[讲]我国劳动人民早在几千年前就掌握了发酵酿酒术,至今,发酵法仍是制备乙醇的重要方法。发酵法以富含淀粉的各种谷物和野生果实为原料,经下列过程成为发酵液:

发酵液内含乙醇10%-15%,发酵液经蒸馏可得含95.6%的乙醇和4.4%水的恒沸液液,称为工业酒精。
[板书]

[知识拓展]

[总结]

[自我评价]
2、Cu在这里起催化剂作用。
3、CH3CH2ONa的水溶液是碱性的?酸性的?还是中性的?
CH3CH2ONa 是强碱
[讲]乙醇和水都有羟基,羟基中氢原子与氧原子之间的共用电子对由于氧原子吸引电子的能力强(非金属性强),电子对很大程度偏离氢原子,这就可能使氢原子以离子形式脱离,产生氢离子,故乙醇和水能与金属钠反应生成氢气。但乙醇中的乙基(烷基)是斥电子基,使乙醇的羟基中氢原子的离子化倾向减弱,故乙醇与钠的反应比水与钠的反应要缓和得多,乙醇比水难电离,故乙醇属非电解质
[过]燃料乙醇的使用不仅可节省能源,而且可以减少环境污染。巴西等国是推广汽车燃烧乙醇的最早的国家,我国燃料乙醇刚起步,2003年投产的吉林60万吨燃料乙醇项目,是国内乙醇生产规模之最。
[板书]2、氧化反应
(1) 燃烧:现象:产生淡蓝色火焰,同时放出大量热

[讲]乙醇在人体内在酶的作用下,也能发生氧化还原反应,将乙醇代谢成乙酸排出体外,因此,一个人的酒量好坏是根其体内含酶多少来划分的,这就是为什么有的人“千杯万盏皆不醉”,而有的人则“洒不醉人人自醉”。
[过]通过乙醇与钠的反应我们知道乙醇中的O-H键最易断裂,那么其C-H键和C-O键能否断裂吗?
[探究实验]
实验操作:把一端弯成螺旋状的铜丝放在酒精灯外焰中加热,使铜丝表面生成一薄层黑色的CuO,立即把它插入盛有乙醇的试管里,这样反复操作几次。
实验现象:加热变黑的铜丝伸入乙醇后又变为光亮的红色,有大量的气泡,有刺激性气味气体生成
[投影]乙醇氧化机理:

[板书](2) 催化氧化
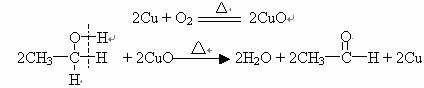
总反应: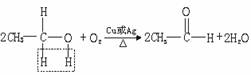
[注意]1、生成物叫乙醛,特征基团是-CHO,乙醛是无色、具有刺激性气味的液体;密度比水小;易挥发;易燃烧;能与水、乙醇等互溶。易被氧化制乙酸,也可以被还原制乙醇。
2、水和钠、水和乙醇,钠个反应更剧烈呢?为什么?
水与钠反应更剧烈,因为H2O中的H比CH3CH2OH 中的H更活泼。
1、CH3CH2OH的水溶液是碱性的?酸性的?还是中性的?它还能与哪些金属反应?
CH3CH2OH 是非电解质,既无碱性,也无酸性;钾、镁、铝等亦能和乙醇反应。
1、与活泼金属反应(如Na、K、Mg、Al等)
2CH3CH2OH+2Na 2CH3CH2ONa+H2↑
2CH3CH2ONa+H2↑
2CH3CH2OH+Ca (CH3CH2O)2Ca
+H2↑
(CH3CH2O)2Ca
+H2↑
[投影]

[思考与交流]
4、球棍模型和比例模型
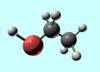

[讲]CH3CH2-部分可以简单写成C2H5-,因为它没有同分异构体。所以,可以看成乙烷中一个氢被-OH取代,或水中的氢被乙基取代后所得。
[板书]5、特征基团:-OH 羟基
[讨论]羟基与氢氧根离子间的区别
[投影]

[讲]乙醇羟基上的氢不如水中的氢活泼,乙醇分子中的--OH键比H2O分子中的O-H键更稳定。同样的键在不同的环境中,其稳定性会有所不同,因为它不是孤立。综合乙醇与Na反应和金属活动性顺序便知,K、Ca等很活泼的金属也能与乙醇发生反应,请同学们试着写出方程式
[板书]三、化学性质
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com