
24.答案:A
解析:应选择极易与NaOH反应(或说极易被NaOH吸收)的物质。其中只有A符合。B中的CH4,C中的CO,D中的NO本身都不与NaOH反应,故不选。
注:如是混合气,则NO2与NO又为等摩尔混合时也可进行喷泉实验。因NO2+NO+2NaOH===2NaNO2+H2O。
23.答案:B
解析:SO2、CO、NO都是污染大气的主要有害物质。SO2能使人发生呼吸道疾病,CO和NO能引起血红蛋白中毒,不会造成大气污染的是N2。
38.4×10-3 g/64 g·mol-1=0.6×10-3 mol,与浓硝酸反应若全部生成NO2气体,V(NO2)=0.6×10-3mol×2×22.4 L·mol-1/1=1.2×10-3×22.4 L。消耗n(HNO3)=(0.6×2+0.6×2)×10-3 mol=2.4×10-3 mol;
若全部生成NO气体,
V(NO)=(0.6×10-3mol×2×22.4 L·mol-1)/3=0.4×10-3×22.4 L,消耗n(HNO3)=(0.6×2+0.6/3×2)×10-3 mol=1.6×10-3 mol。已知生成22.4 mL气体,介于二者之间,所以生成的是NO、NO2的混合气体,消耗的HNO3的物质的量也应介于2.4×10-3 mol和1.6×
10-3 mol之间,所以选C。
解法二:仍然用上述方法判断22.4 mL气体的成分为NO、NO2混合气体。然后根据氮的物质的量反应前后守恒得出如下关系:
n(HNO3)=n[Cu(NO3)2]×2+n(NO2)+n(NO)
=n(Cu)×2+n(总气体)
=38.4×10-3 g/64 g·mol-1×2+22.4×10-3 L/22.4 L·mol-1
=2.2×10-3 mol
22.答案:C
解析:解法一:根据电子守恒Cu:
21.答案:BD
解析:选择b溶液极易吸收a气体且无其他气体生成的。NO2易与水反应但又生成NO,溶液不能充满烧瓶,Cl2在饱和NaCl中溶解度很小基本不被吸收。
20.答案:C
解析:由质量守恒定律知反应前后原子的个数与种类不变,所以可按反应前两种原子数目计算,又原子的物质的量之比等于原子个数之比,所以n(N)∶n(O)=a∶(a+2b),故选C。
19.答案:AD
解析:白磷有毒,红磷无毒,白磷着火点很低,在空气中加热极易燃烧,被氧化。
18.答案:C
解析:设烧瓶的容积为V L,V L NH3全部溶于水,形成溶液的体积为V L,V L的NO2完全反应后,生成了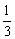 V L的NO气体,形成的溶液的体积为
V L的NO气体,形成的溶液的体积为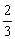 V L,从N原子守恒角度分析,也有
V L,从N原子守恒角度分析,也有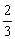 V L的NO2转化生成溶质HNO3。所以两溶液的物质的量浓度相等。
V L的NO2转化生成溶质HNO3。所以两溶液的物质的量浓度相等。
17.答案:A
16.答案:D
解析:铜锌合金也称黄铜,其外观与黄金相似,但其密度比黄金小,因其含有锌元素,放入硝酸、盐酸中都能反应,而黄金却不与硝酸、盐酸反应。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com