
14.T ℃时,A气体与B气体反应生成C气体。反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1 ℃和T2 ℃时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是
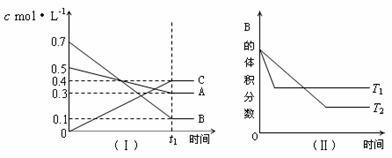
A.该平衡体系的化学反应方程式为:A(g) + B(g) 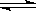 C(g)
C(g)
B.(t1+10)min时,保持容器总压强不变,通入稀有气体,平衡向逆反应方向移动
C.T1<T2
D.其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大
13.下列各组离子在碱性条件下能大量共存,且在强酸性条件下能发生氧化还原反应的是
A.K+、Na+、SO32-、NO3- B.Ca2+、Al3+、SO42-、Cl-
C.Na+、K+、NO3-、SO42- D.NH4+、Na+、Cl-、CO32-
12.制印刷电路时常用氯化铁溶液作为“腐蚀液”,发生的反应为2FeCl3+Cu=2FeCl2+CuCl2,向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是
A.烧杯中有铁无铜 B.烧杯中有铜无铁 C.烧杯中铁、铜都有 D.烧杯中铁、铜都无
11.在a L Al2(SO4)3和(NH4)2SO4的混合溶液中加入b mol BaCl2,恰好使溶液中的SO42-离子完全沉淀;如加入足量NaOH并加热可得到c mol NH3,则原溶液中的Al2(SO4)3离子浓度(mol/L)为
A.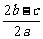 B.
B.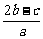 C.
C.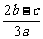 D.
D.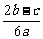
10.下列离子方程式中正确的是
A.H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42- = BaSO4↓+H2O
B.AgNO3溶液中加入过量氨水:Ag+ + NH3·H2O = AgOH↓ + NH4+
C.氧化铝溶于NaOH溶液:Al2O3+2OH-+3H2O = 2 Al(OH)4-
D.CH3COOH溶液与NaOH溶液反应: H++OH- = H2O
9.下列各组物质的分类正确的是
①混合物:氯水、氨水、水玻璃、水银、福尔马林、聚乙烯
②电解质:硫酸铝钾、冰醋酸、氯化氢气体、纯碱
③非极性分子:CO2、CC14、CH2C12、对二甲苯
④同位素:1H+、2H2、3H
⑤同素异形体:C60、石墨、金刚石、石墨烯
⑥同系物:CH2O2、C2H4O2、C3H6O2、C4H8O2
⑦同分异构体:乙二酸二乙酯、乙二酸乙二酯,二乙酸乙二酯
A.②⑤ B.②④⑤⑦ C.②⑤⑥⑦ D.全部正确
8.将磁性氧化铁放入稀HNO3中可发生如下反应:3Fe3O4+ 28HNO3=9Fe(NO3)x+ NO↑+14H2O 。下列判断合理的是
A.Fe(NO3)x中的x为2
B.反应中每生成0.2 mol 还原产物,就有0.6 mol 电子转移
C.稀HNO3 在反应中只作氧化剂
D.磁性氧化铁中的所有铁元素全部被氧化
7.NA为阿伏加德罗常数,下列叙述正确的是
A.25℃时,1 L pH=13的NaOH溶液中含有NA氢氧根离子
B.1L 1 mol·L-1的盐酸中,所含氯化氢分子数为NA
C.1 mol羟基(-OH)所含的电子数为10NA
D.68gCaSO4和KHSO4的混合固体,所含氧原子数为2NA
6.用生物热解气(主要成分CO、CH4、H2)可将SO2高温下还原为硫单质,主要反应如下:
2CO(g) + SO2(g) =S(g) + 2CO2(g) △H = + 8.0kJ/mol
2H2(g) + SO2(g) = S(g) + 2H2O(g) △H = + 90.4kJ/mol
2CO(g) +O2(g) = 2CO2(g) △H = -566.0kJ/mol
2H2(g) + O2(g) = 2H2O(g) △H = -483.6kJ/mol
则S(g)与O2(g)反应生成SO2(g)的热化学方程式正确的是
A.S(g) + O2(g) = SO2(g) ;△H = -1148.0 kJ/mol
B.S(g) + O2(g) = SO2(g) ;△H = -1148.0 kJ
C.S+ O2 = SO2;△H = -574.0 kJ/mol
D.S(g) + O2(g) = SO2(g);△H = -574.0 kJ/mol
5.关于下列各装置图的叙述中,正确的是
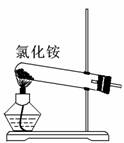

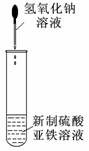
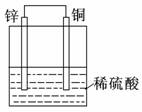
① ② ③ ④
A.实验室用装置①制取氨气
B.装置②中X若为四氯化碳,可用于吸收氨气,并防止倒吸
C.装置③可用于制备氢氧化亚铁并观察其颜色
D.装置④是原电池,锌电极为负极,发生还原反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com