
0.3 mol·L-1,则vb=0.075 mol·L-1·s-1,故B项正确;平衡后,增大压强平衡正移,A的转化率增大,故C项错误;平衡后,升温平衡逆移,C的浓度减小,故D项错误。
11(2010·潍坊模拟)关于下列各图的叙述正确的是( )


A.甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6kJ·mol-1
B.乙表示恒温恒容条件下发生的可逆反应2NO2(g) N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
C.丙表示A、B两物质的溶解度随温度变化情况,将A、B饱和溶液分别由T1℃升温至T2℃时,溶质的质量分数B>A
D.丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液
[答案]选D。
10、(2010·连云港模拟)将 4 mol A 气体和 2 mol B 气体在 2 L
的密闭容器中混合并在一定条件下发生如下反应 2A(g)+B(g)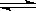 2C(g);△H <0。4 s(秒)后反应达到平衡状态,此时测得 C 的浓度为0.6 mol·L-1 。下列说法中正确的是 ( )
2C(g);△H <0。4 s(秒)后反应达到平衡状态,此时测得 C 的浓度为0.6 mol·L-1 。下列说法中正确的是 ( )
A.当A 、B、C物质的量浓度之比为 2:1:2时,反应即达到平衡状态
B.4s内用物质B表示的反应速率为0.075 mol·L-1·s-1
C.达平衡后若通入一定量氦气,A的转化率降低
D.达平衡后若升高温度,C的浓度将增大
[解析]选B。各物质浓度是否满足方程式计量数比,与反应是否平衡无关,故A项错;4 s内消耗c(B)=
0.075 mol·L-1;则下列关于C物质状态的推测正确的是( )
①C为非气态;②C为气态;③第二次达到平衡时C为气态;④第三次达到平衡时C为非气态A.② B.③④ C.②④ D.①④
[解析]选C.第一次平衡与第二次平衡相比,c(A)增加的浓度大于压强的增加,故增压时平衡向逆反应方向移动,从而可确定第二次达到平衡时C为气态;第二次平衡与第三次平衡相比,c(A)浓度的增加程度小于压强的增加程度,故增压平衡向正反应方向移动,从而确定第三次达到平衡时C为非气态,故选C项。
9、(2010·合肥模拟)温度为T℃,压强为1.01×106Pa条件下,某密闭容器下列反应达到化学平衡A(g)+ B(g)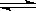 3C(?),测得此时c(A)=0.022 mol·L-1;压缩容器使压强增大到2.02×106Pa,第二次达到平衡时,测得c(A)=0.05 mol·L-1;若继续压缩容器,使压强增大到4.04×107Pa,第三次达到平衡时,测得c(A)=
3C(?),测得此时c(A)=0.022 mol·L-1;压缩容器使压强增大到2.02×106Pa,第二次达到平衡时,测得c(A)=0.05 mol·L-1;若继续压缩容器,使压强增大到4.04×107Pa,第三次达到平衡时,测得c(A)=
0.2-a)÷a=3:2,解得:a=0.08
A项,反应放出的热量为0.08a kJ; B项,平衡时H2O的转化率为0.08÷0.2=40%; C项,该反应前后气体系数相等,压强改变,该平衡不移动;D项, CO、H2O、CO2、H2的浓度都相等时,不一定是平衡状态。
8、(2010·临沂模拟)已知在一定条件下有CO(g)+H2O(g) CO2(g)+H2(g)在某一容积为2L的密闭容器内,加入0.2mol的CO和0.2mol的H2O,在催化剂存在的条件下,高温加热,发生如下反应:CO(g)+H2O(g)=CO2(g)+H2(g);△H=a kJ/mol反应达平衡后,测得c(CO):c(CO2)=3:2,下列说法正确的
是( )
A.反应放出的热量为0.04a kJ
B.平衡时H2O的转化率为40%
C.若将容器的体积压缩为1L,有利于该反应平衡正向移动
D.判断该反应达到平衡的依据是CO、H2O、CO2、H2的浓度都相等
[解析]选B。A项,CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
开始(mol): 0.2 0.2
反应(mol): a a a a
平衡(mol) 0.2-a 0.2-a a a
7、(2010·长沙模拟)某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)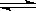 2AB3(g)化学平衡状态的影响,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),根据如图可得出的判断结论正确的是( )
2AB3(g)化学平衡状态的影响,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),根据如图可得出的判断结论正确的是( )

A.正反应一定是放热反应
B.达到平衡时A2的转化率大小为:b>a>c
C.正反应一定是吸热反应,且T2>T1
D.b点时,平衡体系中A、B原子数之比接近1∶3
 [答案]选D。
[答案]选D。
6、(2010·金华模拟)在一个密闭容器中用等物质的量的A和B发生反应:
A(g)+3B(g)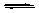 2C(g),该反应达到平衡时,平衡混和气中A的体积分数为( )
2C(g),该反应达到平衡时,平衡混和气中A的体积分数为( )
A.50% B.60% C.70% D.无法计算
[解析]选A。 A(g)+3B(g)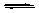 2C(g) △=2
2C(g) △=2
开始(mol): 1 1
反应(mol): a 3a 2a
平衡(mol): 1-a
混和气中A的体积分数为(1-a)÷(2- 2a)=50%
5、(2010·厦门模拟)已知某可逆反应:mA(g)+nB(g)
 xC(g),在密闭容器中进行,右图表示反应在不同时间t、温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则正确的是( )
xC(g),在密闭容器中进行,右图表示反应在不同时间t、温度T和压强P与C在混合气体中的百分含量(C%)的关系曲线,则正确的是( )

A.T1>T2 ,P1>P2 ,m+n>x ,正反应放热
B.T1<T2 ,P1<P2 ,m+n<x ,正反应吸热
C.T1>T2 ,P1<P2 ,m+n<x ,正反应放热
D.T1<T2 ,P1>P2 ,m+n>x ,正反应吸热
[解析]选C。由相同温度T1 ,不同压强下两条曲线比较知,速率快的压强大,P1<P2,由P1到P2,压强增大时,C百分含量下降,平衡逆向移动,所以,m+n<x;由相同压强T1 ,不同温度下两条曲线比较知,速率快的温度高,T1>T2,由T1到T2,温度降低时,C百分含量升高,平衡正向移动,所以,正反应放热。
4、(2010·延边模拟)高温下,某反应达到平衡,平衡常数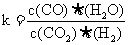 ,恒容时,温度升高,H2
,恒容时,温度升高,H2
浓度减小,下列说法正确的是( )
A.该反应的焓变为正值
B.恒温恒容下,增大压强,H2浓度一定减小
C.升高温度,逆反应速率减小

D.该反应化学方程式为CO+H2O CO2+H2

[解析]选A。由平衡常数的表达式知,该反应化学方程式为CO2+H2 CO+H2O,D错;
项。A项,温度升高,H2浓度减小,说明平衡正向移动,该反应为吸热反应,焓变为正值;B项,恒温恒容下,增大压强,相当于体积缩小,H2浓度一定增大;C项,升高温度,正、逆反应速率都会增大。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com