
16、(2010·南京模拟)常温下将c1 mol/L V1 mL的氨水滴加到c2 mol/L V2 mL的盐酸中,下列结论正确的是( )
A.若混合溶液的pH=7,则c1V1>c2V2
B.若V1=V2,c1=c2,则混合液中c(NH4+)=c(Cl-)
C.若混合溶液的pH=7,则混合液中c(NH4+)>c(Cl-)
D.若V1=V2,且混合溶液的pH<7,则一定有c1<c2
[解析]选A。A项,若混合溶液的pH=7,则氨水稍过量,c1V1>c2V2;B项,若V1=V2,c1=c2则氨
水与盐酸恰好完全反应,混合液中溶质为NH4Cl, c(Cl-)>c(NH4+);C项,若混合溶液的pH=7,由
电荷守恒知,c(NH4+)=c(Cl-);D项,混合溶液的pH<7,溶质可能是NH4Cl或NH4Cl和HCl,可能
c1=c2或 c1<c2。
15、(2010·厦门模拟)用酸碱中和滴定的方法测定NaOH和Na2CO3的混合液中的NaOH含量时,可先在混合液中加过量的BaCl2溶液,使Na2CO3完全变成BaCO3沉淀,然后用标准盐酸滴定(用酚酞作指示剂),下列有关实验的说法正确的是( )
A.向混有BaCO3沉淀的NaOH溶液中滴入盐酸,不会影响NaOH含量的测定
B.滴定时,若滴定管中滴定液一直下降到活塞处才达到滴定终点,则不会影响计算结果
C.若用甲基橙作指示剂,则测定结果偏小
D.可以不用将Na2CO3完全变成BaCO3沉淀,直接滴加标准盐酸,至不再有气泡产生
[解析]选A。A项,酚酞作指示剂,滴定终点显弱碱性,盐酸不会与BaCO3反应,不会影响NaOH含量的测定;B项若滴定管中滴定液一直下降到活塞处,则无法读取数据;C项,若用甲基橙作指示剂,滴定终点显酸性,部分盐酸与BaCO3反应,则测定结果偏大
14、(2010·巢湖模拟)莫尔盐[(NH4)2Fe(SO4)2·6H2O]常作氧化还原滴定法的基准物质,下列有关该盐溶液比较不正确的是( )
A.c (SO42-) > c (NH4+)>c (Fe2+)>c (H+)>c (OH-)
B.c (SO42-) = c (NH4+)>c (Fe2+)>c (H+)>c (OH-)
C.2c (SO42-)+ c (OH-) = c (NH4+) + 2c (Fe2+)+ c (H+)
D.c(H+) = c(OH-) + c(NH3· H2O) + 2c( Fe(OH)2 )
[解析]选B。A项,NH4+、 Fe2+水解显酸性,c (SO42-) > c (NH4+),A项正确,B项错误;C项符合电荷守恒;D项符合质子守恒。
13、(2010·济南模拟)已知某溶液中只存在OH-、Cl-、NH4+、H+四种离子,下列说法不正确的是( )
A.若溶液中c(NH4+)=c(Cl-),则该溶液一定显中性
B.若溶液中c(NH4+)>c(Cl-)>c(OH-)>c(H+),则溶液中一定含有NH4Cl和NH3·H2O
C.若溶液中c(Cl-)>c(NH4+)>c(H+)>c(OH-),则溶液中可能含有NH4Cl或可能含有NH4Cl和HCl
D.若溶液中c(Cl-)>c(H+)>c(NH4+)>c(OH-),则溶液中含有大量的NH4Cl和少量的HCl
[解析]选D。A项,若溶液中c(NH4+)=c(Cl-),由电荷守恒知c(OH-)=c(H+),则该溶液一定显中性。B项,溶液呈碱性,溶质只能是NH4Cl和NH3·H2O;C项,溶液呈酸性,溶质可能含有NH4Cl或可能含有NH4Cl和HCl;但若溶质是大量的NH4Cl和少量的HCl,则c(Cl-)>c(NH4+)>c(H+)>c(OH-),D项错误。
12、(2010·广州模拟)将足量的CO2慢慢通入一定体积某浓度的NaOH溶液中,溶液的pH随CO2体积(已换算成标准状况)的变化曲线如图所示(不考虑过量的CO2在水中的溶解和反应过程中溶液体积的变化),则下列说法中不正确的是( )
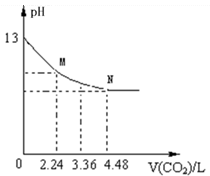
A.NaOH溶液的物质的量浓度为0.1mol/L
B.NaOH溶液的体积为2L
C.M点粒子浓度的大小关系满足c(HCO3-)>c(CO32-)
D.M、N点对应的纵坐标均大于7
[解析]选C。A项,NaOH溶液的pH为13,c(OH-)为0.1mol/L;B项,4.48L CO2物质的量为0.2mol,0.2mol CO2可与NaOH恰好完全反应生成NaHCO3 ,所以NaOH溶液的体积为0.2mol÷ 0.1mol/L﹦2L。C项,M点对应 CO2物质的量为0.1mol,0.1 mol CO2可与NaOH恰好完全反应生成Na2CO3,溶液中粒子浓度的大小关系c(CO32-)>c(HCO3-);D项,M、N点对应的溶液中的溶质分别为 Na2CO3 、NaHCO3,两者水解都显碱性,pH大于7。
11、(2010·沈阳模拟)欲使0.1mol/LNaHCO3溶液中c(H+)、c(CO32-)、c(HCO3-)都减小,方法是( )
A.通入CO2气体 B.加入NaOH固体
C.通入HCl气体 D.加入饱和石灰水
[解析]选D。A项,通入CO2气体c(H+)、c(CO32-)、c(HCO3-)都增大;B项,NaOH可与NaHCO3反应生成Na2CO3,c(H+)、 c(HCO3-)减小,c(CO32-)增大;C项,HCl可与NaHCO3反应生成Na Cl、H2O 和CO2气体 ,c(H+)增大,c(CO32-)、c(HCO3-)都减小;D.饱和石灰水可与NaHCO3反应生成CaCO3,
c(H+)、c(CO32-)、c(HCO3-)都减小。
10、(2010·青岛模拟)下列各组比较中,前者比后者大的是( )
A.25℃时,pH均为2的H2SO4溶液和盐酸中氢离子的物质的量浓度
B.25℃时,pH均为2的盐酸和CH3COOH溶液中溶质的物质的量浓度
C.同温度、同浓度的NaCl溶液和氨水的导电能力
D.25℃时,pH均为3的HCl和FeCl3溶液中水的电离程度
[解析]选C。A项,同温度pH相等的H2SO4溶液和盐酸中氢离子的物质的量浓度相等;B项,同温度pH相等的盐酸和CH3COOH溶液中溶质的物质的量浓度相比,后者大;C.导电能力与溶液中的离子浓度有关,同温度、同浓度的NaCl溶液和氨水的导电能力,前者大;D项,HCl电离出的H+能抑制水的电离, FeCl3水解能促进水的电离,同温度pH相等的HCl和FeCl3溶液中水的电离程度,后者大。
9、(2010·延边模拟)对水的电离平衡不产生影响的粒子是( )
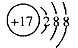
 B.
C. 26M3+ D.
HCO3-
B.
C. 26M3+ D.
HCO3-
[解析]选B。A项,NaOH能抑制水的电离;B项,Cl-对水的电离平衡不产生影响; C项,Fe3+水解能促进水的电离;D项, HCO3-水解能促进水的电离。
8、(2010·昆明模拟)下图表示的是某离子X的水解过程示意图,则离子X可能是( )

A.CO32- B.HCO3- C.Na+ D.NH4+
[解析]选D。离子X水解显酸性所以只能是NH4+。
7、(2010·曲靖模拟)已知NaHSO3溶液呈酸性,NaHCO3溶液呈碱性。现有浓度均为0. 2 mol·L-1的NaHSO3溶液和NaHCO3,溶液中各粒子的物质的量浓度存在下列关系(R表示S或C),其中正确的是( )
A.两溶液中c(Na+),c(HRO3-),c(RO32-),分别相等
B. c(Na+)﹥c(HRO3-)﹥c(H+)﹥c(RO32-)﹥c(OH -)
C. c(H+)+ c(H2RO3)= c(RO32-)+ c(OH-)
D. c(Na+)+ c(H+)= c(HRO3-)+ c(RO32-)+ c(OH-)
[解析]选C。NaHSO3溶液呈酸性,说明HSO3-的电离能力大于水解能力,NaHCO3溶液呈碱性,说明HCO3-的水解能力大于电离能力。A项,两溶液中c(Na+)相等,NaHSO3中c(RO32-)大;B项,NaHSO3溶液中c(Na+)﹥c(HRO3-)﹥c(H+)﹥c(RO32-)﹥c(OH -),而NaHCO3溶液中c(Na+)﹥c(HRO3-)﹥c(OH -)﹥c(RO32-)﹥c(H+)。C项,符合质子守恒;D项,电荷守恒应为c(Na+)+ c(H+)=
c(HRO3-)+ 2c(RO32-)+ c(OH-)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com