
3. 
其中 表示当
表示当 从左侧趋近于
从左侧趋近于 时的左极限,
时的左极限,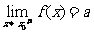 表示当
表示当 从右侧趋近于
从右侧趋近于 时的右极限
时的右极限 
2. 趋向于定值的函数极限概念:当自变量 无限趋近于
无限趋近于 (
(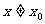 )时,如果函数
)时,如果函数 无限趋近于一个常数
无限趋近于一个常数 ,就说当
,就说当 趋向
趋向 时,函数
时,函数 的极限是
的极限是 ,记作
,记作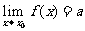

特别地,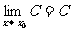 ;
;

1.研究实例
(1)探讨函数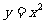 ,当
,当 无限趋近于2时的变化趋势.
无限趋近于2时的变化趋势.
当 从左侧趋近于2时,记为:
从左侧趋近于2时,记为: .
.
 |
1.1 |
1.3 |
1.5 |
1.7 |
1.9 |
1.99 |
1.999 |
1.9999 |
 |
2 |
|
y=x2 |
1.21 |
1.69 |
2.25 |
2.89 |
3.61 |
3.9601 |
3.996 |
3.9996 |
 |
4 |
当 从右侧趋近于2时, 记为:
从右侧趋近于2时, 记为: .
.
 |
2.9 |
2.7 |
2.5 |
2.3 |
2.1 |
2.01 |
2.001 |
2.0001 |
 |
2 |
|
y=x2 |
8.41. |
7.29 |
6.25 |
5.25 |
4.41 |
4.04 |
4.004 |
4.0004 |
 |
4 |
发现(左极限)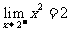 ,(右极限)
,(右极限)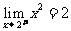 ,因此有
,因此有 .
.
(2)我们再继续看
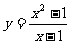 ,当
,当 无限趋近于1(
无限趋近于1( )时的变化趋势:
)时的变化趋势:
 ,当
,当 从左侧趋近于1时,即
从左侧趋近于1时,即 时,
时, .
.
当 从右侧趋近于1时, 即
从右侧趋近于1时, 即 时,
时, .
.
即(左极限)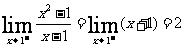 ,
,
(右极限)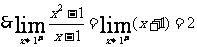

(3)分段函数 当x→0的变化趋势.
当x→0的变化趋势.
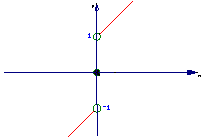
①x从0的左边无限趋近于0,则 的值无限趋近于-1.即
的值无限趋近于-1.即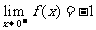
②x从0的右边无限趋近于0,则 的值无限趋近于1. 即
的值无限趋近于1. 即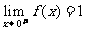
可以看出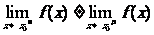 ,并且都不等于
,并且都不等于 .象这种情况,就称当
.象这种情况,就称当 时,
时, 的极限不存在.
的极限不存在.
4.常数函数f(x)=c.(x∈R),有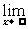 f(x)=c.
f(x)=c.
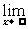 f(x)存在,表示
f(x)存在,表示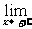 f(x)和
f(x)和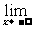 f(x)都存在,且两者相等.所以
f(x)都存在,且两者相等.所以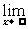 f(x)中的∞既有+∞,又有-∞的意义,而数列极限
f(x)中的∞既有+∞,又有-∞的意义,而数列极限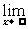 an中的∞仅有+∞的意义
an中的∞仅有+∞的意义

3.函数极限的定义:
(1)当自变量x取正值并且无限增大时,如果函数f(x)无限趋近于一个常数a,就说当x趋向于正无穷大时,函数f(x)的极限是a.
记作: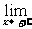 f(x)=a,或者当x→+∞时,f(x)→a.
f(x)=a,或者当x→+∞时,f(x)→a.
(2)当自变量x取负值并且绝对值无限增大时,如果函数f(x)无限趋近于一个常数a,就说当x趋向于负无穷大时,函数f(x)的极限是a.
记作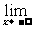 f(x)=a或者当x→-∞时,f(x)→a.
f(x)=a或者当x→-∞时,f(x)→a.
(3)如果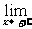 f(x)=a且
f(x)=a且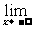 f(x)=a,那么就说当x趋向于无穷大时,函数f(x)的极限是a,
f(x)=a,那么就说当x趋向于无穷大时,函数f(x)的极限是a,
记作: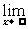 f(x)=a或者当x→∞时,f(x)→a.
f(x)=a或者当x→∞时,f(x)→a.
2.几个重要极限:
(1) (2)
(2) (C是常数)
(C是常数)
(3)无穷等比数列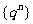 (
(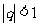 )的极限是0,即
)的极限是0,即 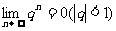

1.数列极限的定义:
一般地,如果当项数 无限增大时,无穷数列
无限增大时,无穷数列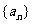 的项
的项 无限趋近于某个常数
无限趋近于某个常数 (即
(即 无限趋近于0),那么就说数列
无限趋近于0),那么就说数列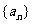 以
以 为极限,或者说
为极限,或者说 是数列
是数列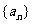 的极限.记作
的极限.记作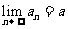 ,读作“当
,读作“当 趋向于无穷大时,
趋向于无穷大时, 的极限等于
的极限等于 ”
” “
“
 ∞”表示“
∞”表示“ 趋向于无穷大”,即
趋向于无穷大”,即 无限增大的意思
无限增大的意思
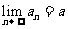 有时也记作:当
有时也记作:当
 ∞时,
∞时,

 .
.
19、(2010·哈尔滨模拟)A、B、C、D、E是位于短周期的主族元素,其中A、B为金属元素。已知:①热稳定性:HmD>HmC;②Cm-、E(m-1)-具有相同的电子层结构;③B与E在同一周期,在该周期中,E的原子半径最小,B的离子半径最小;④A、B所形成的单核离子具有相同的电子层结构,B的最高价氧化物对应的水化物与A、E的最高价氧化物对应的水化物都能反应。依据上述信息用相应的化学用语回答下列问题:
(1)HmD的电子式:___________________。
(2)Cm-、E(m-1)-的还原性强弱为___________>___________,能证明其还原性强弱的离子方程式为_________________________________________________________。
(3)写出B的最高价氧化物对应的水化物和A的最高价氧化物对应的水化物反应的离子方程式_________________________________________________________。
(4)常温下,将等物质的量浓度的HmC溶液和A的最高价氧化物对应的水化物溶液等体积混合,所得溶液显碱性,溶液中离子浓度由大到小的顺序为___________________。
(5)在B、C、E单质中,符合下列转化关系的是___________________。

[解析]根据题意,B的最高价氧化物对应的水化物与A、E的最高价氧化物对应的水化物都能反应,所以B为Al元素,又因为A、B所形成的单核离子具有相同的电子层结构,所以A为Na元素;根据B与E在同一周期,在该周期中,E的原子半径最小,所以E为Cl元素;根据Cm-、E(m-1)-具有相同的电子层结构,所以C为S元素;根据热稳定性:HmD>HmC,所以D为O元素。
[答案](1)H: O :H
(2)S2->Cl- Cl2+S2-=2Cl-+S↓
(3)Al(OH)3 + OH- = AlO2- +2H2O
(4)c(Na+)>c(HS-)>c(OH-)>c(H+)>c(S2-)
(5)S
()
18、(2010·南阳模拟)以酚酞试剂为指示剂,对某新制的NaOH溶液进行中和滴定实验,数据记录如下表:
|
|
待测液 |
消耗标准盐酸(0.1mol/L)的体积 |
|
① |
20.00mLNaOH溶液 |
V1 mL |
|
② |
20.00mLNaOH溶液+10.00mL水 |
V2 mL |
|
③ |
敞口隔夜放置的20.00mLNaOH溶液 |
V3 mL |
该新制的NaOH溶液的浓度合理的是( )
A.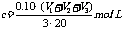 B.
B. 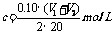 C.
C. 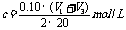 D.
D. 
[解析]选A。向20.00mLNaOH溶液加入10.00mL水,再用盐酸滴定,对消耗盐酸的体积无影响。敞口隔夜放置的20.00mLNaOH溶液会吸收空气中的CO2,但以酚酞试剂为指示剂,用盐酸来滴定时 ,最终产物仍然是NaCl,对消耗盐酸的体积无影响。所以合理的是A。
17、(2010·杭州模拟)下列叙述正确的是( )
A.pH=3的酸溶液稀释100倍后pH=5
B.在相同温度下,pH=3的溶液和pH=5的溶液相比,前者氢离子浓度是后者的100倍
C.相同温度相同浓度的钾盐溶液中,酸式盐的pH一定等于正盐的pH
D.碳酸钠溶液在室温时的pH一定大于60℃时的pH
[解析]选B。A项,pH=3的酸溶液稀释100倍后,若为强酸,则pH=5,若为弱酸pH<5。B项,pH=3的溶液,c (H+)=10-3mol/L,pH=5的溶液c (H+)=10-5,前者氢离子浓度是后者的100倍。C项酸式盐的pH一定小于正盐的pH。D项,温度升高能促进水解,同浓度的碳酸钠溶液的pH,60℃时大于室温时。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com