
6.对文中有关联想江南采莲风俗的文字,理解最贴切、最准确的一项是( )
A.作者在夜晚闲居无事,沿着荷塘漫步而浮想联翩,这一段文字没有太大的意义,可以删去。
B.作者触景生情,表达了他对祖国美好河山的无限热爱,由眼前的荷塘联想到故乡的荷塘,流露出热爱家乡的情感。
C.对古代采莲盛况的向往,对故乡的惦念,是想把自己从“颇不宁静”的心情中解脱出来。
D.为了充实作品内容而附加的,没有什么特别的意义。
5.对“白天里一定要做的事,一定要说的话,现在都可不理。这是独处的妙处,我且受用这无边的荷香月色好了”这段话理解最准确的一项是 ( )
A.白天的应酬太多,交际太多,夜晚终于可以安闲了,所以就放下心来欣赏荷塘月色。
B.在黑暗笼罩下的社会,人与人之间勾心斗角,白天必须说些违心的话,做些违心的事,感到很累;只有到了夜晚漫步的时候,才觉得轻松了些。
C.白天在压抑的心情与环境中工作、生活,在晚上终于暂得宽余,独自欣赏荷塘月色,从那些令人厌倦的人与事中解脱出来,感到淡淡的喜悦。
D.白天从事地下工作,必须加倍小心地同周围的敌人周旋,到了晚上才可以放松一下,感到淡淡的喜悦。
4.对“像今晚上,一个人在这苍茫的月下,什么都可以想,什么都可以不想,便觉是个自由的人”这段话的理解最恰当的一项是 ( )
A.作者用比喻的手法,描写宁静的月夜,这时的“我”与白天的“我”判若两人。
B.在宁静的月夜中,作者可摆脱白天人世的羁绊,得到自己追求的一时的自由。
C.在宁静的月夜下,作者可以任凭自己的性格,想说就说,想做就做。
D.作者用白描手法,描写月夜的美丽,自己也进入了一个美妙的、神秘的世界。
3.下列各句中与其他三句修辞方法不同的一项是 ( )
A.微风过处,送来缕缕清香,仿佛远处高楼上渺茫的歌声似的。
B.光与影有着和谐的旋律,如梵婀玲上奏着的名曲。
C.突然是绿茸茸的草坂,像一支充满幽情的乐曲。
D.树色一例是阴阴的,乍看像一团烟雾。
2.下列加点的词语解释有错误的一项是 ( )
A.树梢上隐隐约约的是一带远山,只有些大意罢了。(大致的轮廓)
B.但杨柳的丰姿,便在烟雾里也辨得出。(指美好的姿态)
C.树色一律是阴阴的,乍看像一团烟雾。(远远看去)
D.叶子底下是脉脉的流水,遮住了,不能见一些颜色,而叶子却更见风致了。(情态、样子)
1.下列加点字的注音完全正确的一项是 ( )
A.脉脉(mò) 颤动(zhàn) 乘凉(chéng) 独处(chǔ)的妙处(chù)
B.酣睡(hān) 参差(cī) 袅娜(nuó) 蓊蓊郁郁(wěng)
C.点缀(zhuì) 倩影(qiàn) 皱缬(xié) 梵婀玲(fán)
D.惦着(diàn) 羞涩(sè) 宛然(wǎn) 踱着步(dù)
朱自清,原名________,字佩弦,号秋实,他的长诗是________,诗集是________,第一本散文集是________。我们还学过他的散文如: 、 等。
21. (2010·临沂模拟)由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、Cl-、NH、Mg2+、CO、Ba2+、SO.将该混合物溶于水后得澄清溶液,现取3份100 mL该溶液分别进行如下实验:
|
实验 序号 |
实验内容 |
实验结果 |
|
1 |
加AgNO3溶液 |
有白色沉淀生成 |
|
2 |
加足量NaOH溶液并加热 |
收集到气体1.12 L(已折算成标准状况下的体积) |
|
3 |
加足量BaCl2溶液时,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 |
第一次称量读数为6.27 g,第二次称量读数为2.33 g |
试回答下列问题:
(1)根据实验1对Cl-是否存在的判断是____________(填“一定存在”“一定不存在”或“不能确定”);根据实验1-3判断混合物中一定不存在的离子是________.
(2)试确定溶液中一定存在的阴离子及其物质的量浓度(可不填满):
|
阴离子符号 |
物质的量浓度(mol/L) |
|
|
|
|
|
|
|
|
|
(3)试确定K+是否存在?________,判断的理由是________________________________
______________________________________________________________.
20.常温下,将20.0 g 14%的NaCl溶液跟30.0 g 24%的NaCl溶液混合,得到密度为1.17 g/cm3的混合溶液.
(1)该混合溶液中NaCl的质量分数为 .
(2)该混合溶液中NaCl的物质的量浓度 mol/L.
(3)在1000 g水中需加入 mol氯化钠,才能使其浓度恰好与上述混合溶液浓度相等(保留1位小数).
19.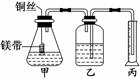 某研究性学习小组为证明在同温同压下,相同浓度、
某研究性学习小组为证明在同温同压下,相同浓度、
相同体积酸性不同的两种二元酸与足量镁带反应时,生成氢气
的体积相同而反应速率不同,同时测定实验室条件下的气体摩
尔体积.设计的简易实验装置如图所示.该实验的主要操作步骤
如下:
Ⅰ.①配制浓度均为0.5 mol/L 的H2SO4和H2C2O4溶液.
②用 量取10.00 mL 0.5 mol/L H2SO4和H2C2O4溶液分别于两个锥形瓶中.
③分别称取除去表面氧化膜的镁带并系于铜丝末端.
④检查装置的气密性,在广口瓶中装满水,按图连接好装置.
⑤将铜丝向下移动,使足量镁带浸入酸中(铜丝不与酸接触)至反应完全后,记录 .
⑥反应结束后,读取量筒内水的体积为 y mL.
Ⅱ.请将上述步骤补充完整并回答下列问题:
(1)用密度为1.84 g/cm3 98%的浓H2SO4,配制浓度为250 mL 0.5 mol/L的H2SO4溶液,所需要的主要仪器有 、 、烧杯、玻璃棒、酸式滴定管.
(2)以下是读取量筒内水的体积时,必须包括的几个步骤:①使乙、丙中液面相平;②将装置冷却至室温;③读取量筒内水的体积.这三步操作的正确顺序是 .
(3)读取量筒内水的体积时,若丙中液面高于乙中液面,使乙、丙中液面相平的操作是 .
(4)简述速率不等的原因 ,铜丝不与酸接触的原因 .
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com