
1.集合A={0,2,a},B={1,a2}.若A∪B={0,1,2,4,16},则a的值为 ( )
A.0 B.1 C.2 D.4
1.在作者的眼中,刘和珍是怎样的人?请整合文中的信息,简要回答。
解析:本题考查的是概括和整合信息的能力。要正确答出刘和珍是怎样的人,就需要我们从文中找出作者对刘和珍评价性的语言,“她们怎能不痛哭战斗正殷中失去了首领”,“然而我永远敬佩你做事的毅力和任劳任怨的精神,尤其是你那微笑中给与我的热力和温情”,把这些评价性语言进行整合即可得出答案。
1.读音
长歌当哭(dàng) 祭品菲薄(bó) 赁屋上课(lìn) 攒射(cuán)
惩创学生(chàng) 浸渍(zì) 干练坚决(gàn) 山阿(ē)
殒身不恤(yǔn xù) 桀骜(ào) 黯然(àn) 喋血(dié)
立仆(pū)
烃的衍生物知识是高考有机化学知识中的重要部分。其命题特点是:一是已知有机物的结构简式写其分子式或由有机物的分子式确定其结构简式,即确定有机物的结构和组成的关系,此类题在近几年高考题中经常出现,有时与书写同分异构体结合在一起。二是根据烃的衍生物的性质,结合生活、生产中常见的物质设计成选择题、推断题来考查学生认识、理解烃的衍生物的主要官能团的性质。三是根据有机物的衍变关系,以新药、新的染料中间体、新型材料的合成为情境,通过引入一些新信息,设计成框图的形式来设问,组合多个化合物的化学反应,合成具有指定结构的产物仍是今后高考命题的方向。
[例题](2002年上海,29)某有机物J(C19H20O4)不溶于水,毒性低,与聚氯乙烯、聚乙烯等树脂具有良好相容性,是塑料工业主要增塑剂,可以用下列方法合成之:
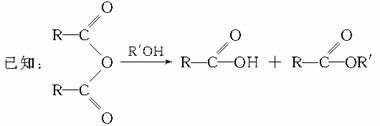
合成路线:
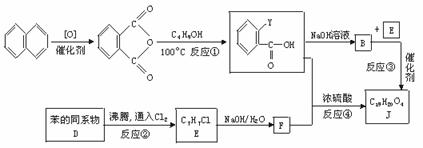
流程中:(Ⅰ)反应A→B仅发生中和反应,(Ⅱ)F与浓溴水混合不产生白色沉淀。
(1)指出反应类型:反应② 反应④ 。
(2)写出结构简式:Y F 。
(3)写出B+E→J的化学方程式 。
(4)写出E的属于芳香烃衍生物的同分异构体的结构简式:
、 、 。
解析:此题为一有机推断题。一要注意反应条件的利用,如由D与氯气反应生成E,没有催化剂的参与,应是苯的同系物侧链上的氢被氯取代,由E到F应是卤代烃的水解,F是醇,则F与A发生的是酯化反应。二要注意分子组成的变化,如碳原子数、氢原子数、氧原子数等的变化,F与A发生酯化反应生成J,由J和F的分子组成,就可推知A的分子组成,进一步再推出Y的组成和结构;另外,注意题给信息的利用,如F与浓溴水混合不产生白色沉淀,说明F不是酚类物质,更进一步说明了前面推导的正确性。
答案:(1)取代 酯化
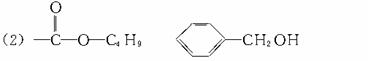
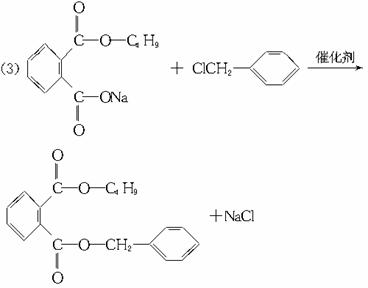
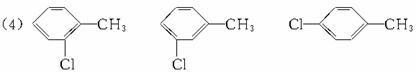
5.有机物中一些经验公式和规律
(1)由烃含氧衍生物(一元)相对分子质量推断类别和分子式:
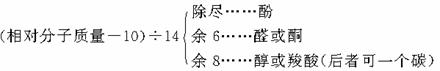
(2)有机物完全燃烧生成CO2和H2O的物质的量比等于原有机物中碳与2倍氢的物质的量比,每增1 mol CH2,耗O2量多1.5 mol。
(3)1 mol有机物完全燃烧的耗氧量,烃为:碳数+氢数/4;一元醇为:碳数+氢数/4-0.5;一元醛或酮为:碳数+氢数/4-0.5;一元羧酸或酯为:碳数+氢数/4-1。
4.系列异构的规律
(1)同数碳的饱和一元醇和醚CnH2n+2O互为同分异构体。
(2)同数碳的一元酚和芳香醇及芳香醚CnH2n-6O互为同分异构体。
(3)同数碳的饱和一元醛和酮CnH2nO互为同分异构体。
(4)同数碳的饱和一元羧酸和酯CnH2nO2互为同分异构体。
(5)同数碳的氨基酸和硝基化合物互为同分异构体。
3.有机化学反应类型
重要有机反应类型和涉及的主要有机物类别
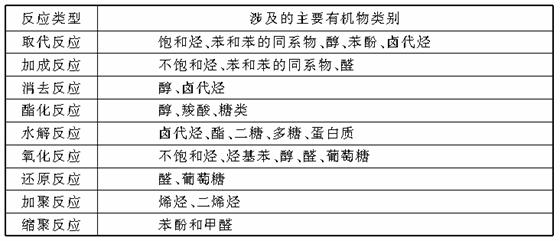
2.烃的衍生物的分类及相互转化关系
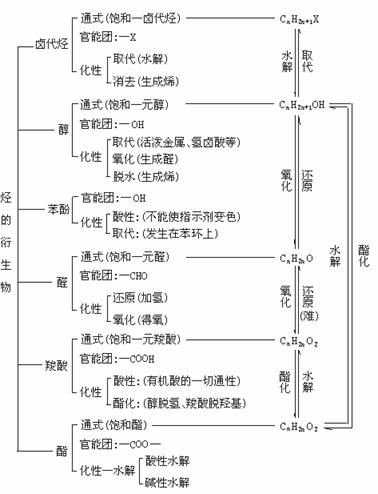
(1)烃的衍生物的化学性质取决于官能团。但官能团相同,其有机物的化学性质不一定完全相同。如苯酚和乙醇官能团同为羟基,化学性质却不完全相同:苯酚显酸性,能与溴水发生取代反应,与Fe3+发生显色反应;而乙醇没有酸性,只与氢卤酸发生取代反应,还能发生消去反应、酯化反应等。
(2)含有多个官能团,具有多个官能团的性质,但官能团之间相互有影响:如甲酸
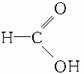
有醛基、羧基,因此能发生氧化反应、中和反应。
(3)有机物间的相互衍变关系
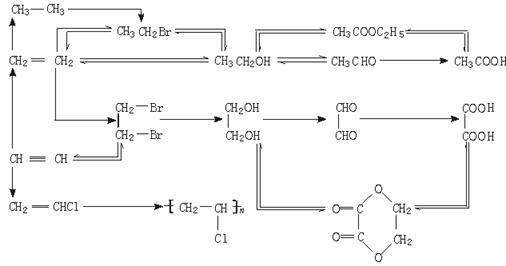
1.有机物重要物理性质的规律
(1)有关密度的规律。物质的密度是指单位体积里所含物质的质量,它与该物质的相对分子质量、分子半径等因素有关。一般讲,有机物的密度与分子中相对原子质量大的原子所占质量分数成正比。例如,烷、烯、炔及苯和苯的同系物等物质的密度均小于水的密度(即ρ烃<1),并且它们的密度均随着分子中碳原子数的增加和碳元素的质量分数的增大而增大;而一卤代烷、饱和一元醇随分子中碳原子数的增加,氯元素、氧元素的质量分数降低,密度逐渐减小。
(2)水溶性规律。有机物是否溶于水与组成该有机物的原子团(包括官能团)有密切关系。在有机物分子常见的官能团中,-OH、-CHO、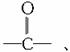 -COOH、-SO3H等,皆为亲水基,-R、-NO2、-X、
-COOH、-SO3H等,皆为亲水基,-R、-NO2、-X、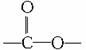 等皆为憎水基。一般来讲,有机物分子中当亲水基占主导地位时,该有机物溶于水;当憎水基占主导地位时,则难溶于水。由此可推知:
等皆为憎水基。一般来讲,有机物分子中当亲水基占主导地位时,该有机物溶于水;当憎水基占主导地位时,则难溶于水。由此可推知:
①烃类均难溶于水,因其分子内不含极性基团。
②含有-OH、-CHO、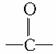 及-COOH的各类有机物(如醇、醛、酮、羧酸),其烃基部分碳原子数小于等于3时可溶于水。
及-COOH的各类有机物(如醇、醛、酮、羧酸),其烃基部分碳原子数小于等于3时可溶于水。
③当活泼金属原子取代有机物分子中的氢原子后所得的产物可溶于水。如CH3CH2ONa、CH3COONa、C6H5ONa等。
(3)熔、沸点规律。熔、沸点是物质状态变化的标志,有机物溶、沸点的高低与分子间相互作用、分子的几何形状等因素有关。
①结构相似的有机物,相对分子质量越大,分子间力越大,其熔、沸点越高。如链烃同系物的沸点,随着相对分子质量的增大而升高,状态由气态(分子中碳原子数小于等于4者及新戊烷通常为气态)到液态,最后变为固态。
②在同分异构体中,一般支链越多,分子间接触越困难,分子间力越小,其熔、沸点越低。如沸点:正戊烷>异戊烷>新戊烷。但熔点有例外,如新戊烷>正戊烷>异戊烷。
③分子的极性越强,分子间引力越大,故相对分子质量相近的有机物,其分子的极性越强,沸点就越高。如沸点:CH3CH2OH>CH3CH2Cl>CH3CH3。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com