
2、Cu(OH)2
(1)难溶性碱,可与酸反应:。
(2)受热易分解:
(3)有弱氧化性,用于醛基化合物的检验:
(4)制备:
1、氧化物
CuO是不溶于水的碱性氧化物,具有较强的氧化性,在加热时能被CO、H2、C等还原,可与酸反应,Cu2O呈砖红色,可用于制红色玻璃,本身较稳定,但在酸液中易发生歧化反应.
、 、
3、化学性质:
(1)与非金属单质(O2、S、Cl2)反应
[思考]如何除去混在H2、CO中的少量O2?
(2)与O2、CO2、H2O的作用(在潮湿的空气中铜可生成铜绿)
(3)与酸的反应
①与稀盐酸、稀硫酸不反应
②与浓硫酸反应:
③与硝酸反应:
(4)与盐溶液反应(FeCl3溶液)
2、物理性质:纯铜呈 色,属有色金属,导电导热性、延展性良好,焰色反应呈 色。
1、原子结构:原子序数为 ,简化电子排布式为 位于元素周期表中第 周期、第 族,最外层有 个电子,常见化合价有 、 价。
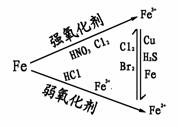 [思考]请写出离子反应式(没离子反应式的写化学方程式):
[思考]请写出离子反应式(没离子反应式的写化学方程式):
(1)FeO与稀HNO3
FeCl2与H2O2/H+
(2)Fe(OH)3、与氢碘酸
FeCl3与H2S
用FeCl3溶液制Fe(OH)3胶体
3.Fe2+ 与Fe3+ 的检验方法
|
|
Fe2+ |
Fe3+ |
|
|
物理方法(观察颜色) |
|
|
|
|
化学方法 |
加碱溶液 |
|
|
|
加KSCN |
|
|
|
|
还有那些方法? |
|
|
[思考] (1)配制FeSO4溶液时,需加入 和 ,其作用分别是 、 。
(2)制取Fe(OH)2时,为什么要用新制的FeSO4溶液?为什么要将吸有NaOH溶液的胶头滴管插入液面以下?
(3)烧过菜的铁锅未及时洗干净(残液中含NaCl),第二天便出现红棕色锈斑[Fe(OH)3失水的产物],试用有关的电极反应式和化学方程式表示Fe(OH)3的生成过程。
2.铁的氢氧化物
|
名称 |
氢氧化亚铁 |
氢氧化铁 |
|
化学式 |
|
|
|
色态 |
白色固体 |
红褐色固体 |
|
溶解性 |
难溶于水 |
难溶于水 |
|
与HCl反应 |
|
|
|
热稳定性 |
无O2条件下,生成FeO 色→ 色→ 色 |
|
|
制备 |
|
|
1.铁的氧化物
|
名称 |
氧化亚铁 |
氧化铁 |
四氧化三铁 |
|
化学式 |
|
|
|
|
价态 |
|
|
|
|
俗名 |
|
铁红 |
磁性氧化铁 |
|
色态 |
黑色粉末 |
红棕色粉末 |
黑色晶体 |
|
溶解性 |
|
||
|
与HCl反应 |
① |
② |
③ |
|
与HNO3反应 |
④ |
⑤ |
⑥ |
|
与HI反应 |
⑦ |
⑧ |
⑨ |
|
特性 |
不稳定。在空气中加热,易被氧化成
。 |
用作油漆的颜料等 |
具有磁性 |
4、铁的冶炼和用途:
[思考] ①将Cu片放入0.1mol·L-1FeCl3溶液中,反应一定时间后取出Cu片,溶液中c(Fe3+)∶c(Fe2+)为2∶3,则Cu2+与Fe3+的物质的量之比为________________。
②mgFe与含有ngHNO3的硝酸溶液恰好完全反应,若m∶n=1∶3,则起氧化剂作用的硝酸的质量是多少克? A、m B、3/4m C、1/2n D、1/4n
③在氯化铁、氯化铜和盐酸的混合溶液中加入铁粉,待反应结束,所剩余的固体滤出后溶液中存在较多的阳离子是( ) A.Cu2+ B.Fe3+ C. Fe2+ D. H+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com