
 1.Cl-的电子式为:
1.Cl-的电子式为:
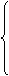 同位素(相同的中子数,不同的质子数,是微观微粒)
同位素(相同的中子数,不同的质子数,是微观微粒)
同素异形体(同一种元素不同的单质,是宏观物质)
同分异构体(相同的分子式,不同的结构)
同系物(组成的元素相同,同一类的有机物,相差一个或若干个的CH2)
同一种的物质(氯仿和三氯甲烷,异丁烷和2-甲基丙烷等)
看图像:一看面(即横纵坐标的意义); 二看线(即看线的走向和变化趋势);
三看点(即曲线的起点、折点、交点、终点),先出现拐点的则先达到平衡,说明该曲线表示的温度较高或压强较大,“先拐先平”。 四看辅助线(如等温线、等压线、平衡线等);五看量的变化(如温度变化、浓度变化等),“定一议二”。
CH3COOH+H18OC2H5
 CH3CO18OC2H5+H2O
CH3CO18OC2H5+H2O
三十九、氧化还原反应配平
标价态、列变化、求总数、定系数、后检查
一标出有变的元素化合价;
二列出化合价升降变化
三找出化合价升降的最小公倍数,使化合价升高和降低的数目相等;
四定出氧化剂、还原剂、氧化产物、还原产物的系数;
五平:观察配平其它物质的系数;
六查:检查是否原子守恒、电荷守恒(通常通过检查氧元素的原子数),画上等号。
四十、"五同的区别"
 ②编号位,定支链
②编号位,定支链
③取代基,写在前,注位置,短线连
④不同基,简到繁,相同基,合并算
烷烃的系统命名法使用时应遵循两个基本原则:①最简化原则,②明确化原则,主要表现在一长一近一多一小,即“一长”是主链要长,“一近”是编号起点离支链要近,“一多”是支链数目要多,“一小”是支链位置号码之和要小,这些原则在命名时或判断命名的正误时均有重要的指导意义。
三十八、酯化反应的反应机理(酸提供羟基,醇提供氢原子)
所以羧酸分子里的羟基与醇分子中羟基上的氢原了结合成水,其余部分互相结合成酯。
浓硫酸
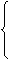 化合价不变只显酸性
化合价不变只显酸性
化合价半变既显酸性又显强氧化性
化合价全变只显强氧化性
三十七、烷烃系统命名法的步骤
①选主链,称某烷
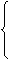 化合价不变只显酸性
化合价不变只显酸性
化合价半变既显酸性又显强氧化性
化合价全变只显强氧化性
三十六、浓硝酸“四性”
酸性、强氧化性、不稳定性、挥发性
注意:⑴要注明反应温度和压强,若反应在298K和1.013×105Pa条件下进行,可不予注明;
⑵要注明反应物和生成物的聚集状态,常用s、l、g分别表示固体、液体和气体;
⑶△H与化学计量系数有关,注意不要弄错。方程式与△H应用分号隔开,一定要写明“+”、“-”数值和单位。计量系数以“mol”为单位,可以是小数或分数。
⑷一定要区别比较“反应热”、“中和热”、“燃烧热”等概念的异同。
三十五、浓硫酸“五性”
酸性、强氧化性、吸水性、脱水性、难挥发性
3.检查△H的数值是否与反应物或生成物的物质的量相匹配(成比例)
2.检查△H的“+”“-”是否与吸热、放热一致。(注意△H的“+”与“-”,放热反应为“-”,吸热反应为“+”)
1.检查是否标明聚集状态:固(s)、液(l)、气(g)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com