
4.氯气的制法
<1>工业制法:
(1) 电解饱和食盐水法:(写出反应的化学方程式和离子方程式)
;
(2)电解熔融的氯化钠:化学方程式
<2> 实验室制法
(1)药品:浓盐酸+强氧化剂 如:(KMnO4,K2MnO4,MnO2,KCIO3等)
写出用MnO2和浓盐酸制取Cl2的化学方程式和离子方程式)
;
[例4]实验室制取Cl2通常利用下图装置:A是氯气发生装置,C.D为气体的净化装置,C中装有饱和食盐水,D中有浓H2SO4,E是硬质玻璃管中装有细铁丝网;F为干燥的广口瓶,烧杯G为尾气吸收装置. 试回答:
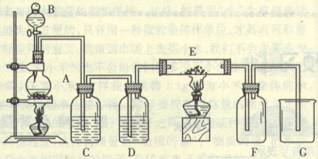
(1)A.B.G中各装有什么药品:A ;B ;G .(写化学式)
(2) 为什么从A中生成的气体一定要通过C.D两个装置? .
(3) 写出G中和E中反应的化学方程式 、
3. 强氧化性a. 漂白性 b.与还原性物质(Fe2+、SO2、I-等反应)
[例2]为了增大氯水中HCIO的浓度应采取的措施是( )
A 加入NaOH固体 B 加入食盐固体 C 加入CaCO3 D 加入Na2SO3固体
[例3]下列事实能证明HCIO是弱酸的是 ( )
A. HCIO不稳定,易分解 B. HCIO有强氧化性
C. HCIO能使有机色质褪色 D.Ca(CIO)2与CO2及H2O反应生成HCIO
(4)跟碱反应:
①与烧碱反应:
用途:制漂白液和氯气的尾气吸收
②制取漂白粉
[思考]漂白粉(精)的组成、性质和用途
①有效成份 、主要成份 。
②与CO2的反应:
与盐酸的反应:
③漂白粉要密封保存,防止与空气接触而变质,失效的原因是(用方程式表示为:)
(5)跟其它物质的反应:(如:KI、FeCl2、SO2、Na2SO3、CH4、CH2=CH2、C6H6等)
1.不稳定性: HClO 2. 弱酸性:
2. 弱酸性:
3.化学性质:活泼的非金属,具有很强的 性,电负性仅次于 、 。
(1)跟金属反应:(与Na、Fe、Cu反应,描述现象)
(2)跟非金属反应:
①与H2反应(点燃时火焰呈____色,同时集气瓶口有____,混合光照,发生______)
[思考]燃烧一定要氧气参与?你对燃烧有何新的认识?
②与P反应
(3)跟水反应(溶于水的部分Cl2与水反应):
氯水中的成份有:分子 离子 。
[例1]在氯水中分别加入下列溶液:①紫色石蕊试液;②氯化亚铁溶液;③碳酸钠溶液;④氢硫酸;⑤硝酸银溶液。观察有何现象?写出相关离子方程式。
[思考]液氯和氯水有什么区别? 氯水久置后会变成什么溶液?
氯水如何保存? 干燥氯气能漂白?
[思考]次氯酸性质:
2.物理性质:
通常情况下,Cl2是______色_________气味气体。密度比空气_____,____溶于水,易液化。
[思考]闻有毒气体及未知气体气味的方法是
1.组成和结构:位于第 周期第 族,只以 态存在。常见价态 。
[对比]氯原子结构;氯分子结构;氯离子结构。写出它们的电子式及结构简图
12.一质点沿直线Ox轴做变速运动,它离开O点的距离x随时间t变化的关系式为x=5+2t3(m),它的速度随时间t的变化关系为v=6t2(m/s).求:
(1)该质点在t1=0至t2=2 s时间内的平均速度 1和在t2=2 s至t3=3 s时间内的平均速度 2.
(2)该质点在t2=2 s的瞬时速度v2和t3=3 s的瞬时速度v3.
[解析]
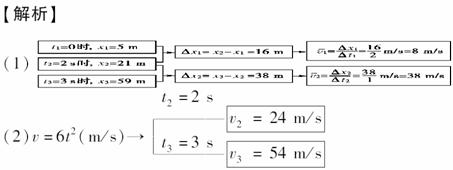
[答案] (1)8 m/s 38 m/s (2)24 m/s 54 m/s
11.

如右图所示,一列火车在甲、乙两站之间匀速行驶,一位乘客根据铁路旁电杆的标号观察火车的运动情况.在5 min时间内,他看见电杆的标号从100增到200.如果已知两根电杆之间的距离是50 m.甲、乙两站相距x=72 km那么火车从甲站到乙站需时间多少?
[解析] 先分析求出5 min内火车的位移,求出火车速度,再根据两站之间的距离,求所用时间,在5 min的时间里,火车运动的位移
Δx=50×100 m=5 000 m,Δt=5 min=300 s,
故火车的速度为v== m/s= m/s.
从甲站到乙站所需时间为t==4 320 s=72 min.
[答案] 72 min
10.

用接在50 Hz交流电源上的打点计时器,测定小车的运动情况.某次实验中得到一条纸带如右图所示,从比较清晰的点起,每五个打印点取一个计数点,分别标明0、1、2、3…,量得0与1两点间距离x1=30 mm,2与3两点间的距离x2=48 mm,则小车在0与1两点间的平均速度为v1=________m/s,在2与3两点间的平均速度v2=________m/s,据此可判定小车做________.
[解析] 由平均速度的定义式=得v1==m/s=0.3 m/s,v2== m/s=0.48 m/s.可见,小车的速度变大,故判定小车做加速运动.
[答案] 0.3 0.48 加速运动
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com