
13.下列实验基本操作正确的是 ( )
A.用碱式滴定管量取0.10 mol·L-1的Na2CO3溶液22.10 mL;
B.配制一定浓度的氢氧化钠溶液时,将氢氧化钠固体放在纸片上称量
C.将滴管垂直伸进试管内滴加液体。
D.用玻璃棒蘸取溶液滴到湿润的pH试纸上,测其pH
12.下列描述违背化学原理的是( )
A.“冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高
B.反应A(g)+3B(g) 2C(g)达平衡后,温度不变,增大压强,平衡正向移动,平衡常数K值增大
2C(g)达平衡后,温度不变,增大压强,平衡正向移动,平衡常数K值增大
C.SO2的催化氧化是一个放热的反应,升高温度,反应速率加快
D.在KI溶液中加入氯化银固体,一段时间后沉淀变成黄色,说明同温度下Ksp(AgI)< Ksp(AgCl)
11.常温下,0.1mol·L-1某一元酸(HA)溶液中=1×10-8,下列叙述正确的是( )
A.该一元酸溶液的pH=1
B.该溶液中HA的电离度为 1% C.该溶液中水的离子积常数为1×10-22 D.若加水稀释,则C(OH-)/C(H+)将减小
10.用铜片、银片、Cu (NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U型管)构成一个原电池。以下有关该原电池的叙述正确的是( )
①在外电路中,电流由铜电极流向银电极 ②正极反应为:Ag++e - =Ag ③实验过程中取出盐桥,原电池仍继续工作 ④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同 A.②④ B.②③ C.①② D.③④
9.某温度下,反应N2
(g)+3H2 (g) 2NH3(g);△H <0,在密闭容器中达到平衡,平衡时改变外界条件,使反应再次平衡,新平衡时,c(H2)/c(NH3)与原平衡相比变小了,则改变条件的可能有( )
2NH3(g);△H <0,在密闭容器中达到平衡,平衡时改变外界条件,使反应再次平衡,新平衡时,c(H2)/c(NH3)与原平衡相比变小了,则改变条件的可能有( )
A.保持容器的容积不变,升高了温度
B. 保持容器压强和温度不变,向容器内补充了Ar(g)
C.保持容器容积和温度不变,向容器内补充了N2
D.保持容器容积和温度不变,液化分离走部分NH3
8.化学与社会、生活、环境保护密切相关,下列现象或事实与解释一致的是( )
|
编号 |
现象或事实 |
解释 |
|
A |
用热的纯碱溶液洗去油污 |
纯碱可以直接与油污反应 |
|
B |
在农田施肥时,草木灰(主要成分K2CO3)不能与氯化铵混合使用 |
一定条件下,K2CO3与NH4Cl会发生反应,有“跑氨”现象 |
|
C |
漂白粉因在空气中放置时间过久而变质 |
漂白粉中的CaCl2与空气中的CO2反应生成碳酸钙 |
|
D |
利用氯化铁溶液可以制作铜质印刷线路板 |
FeCl3溶液置换出铜单质 |
7.在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中大量共存的( ) A. 滴加酚酞试液显红色的溶液 Fe3+、NH4+、Cl-、SCN- B. 水电离出来的c(H+)=10-13mol/L的溶液 K+、HCO3-、Br-、Ba2+ C. 所含溶质为Na2SO4的溶液 K+、CO32-、NO3-、Al3+ D. pH=1的溶液 Cu2+、Na+、Mg2+、NO3-
6.能正确表示下列反应的离子方程式是( )
A.用醋酸除去水垢:CaCO3 + 2H+==Ca2+ + H2O + CO2↑
B.氯气与水反应:Cl2+H2O=2H++Cl-+ClO-
C.氨水中滴加盐酸:H+ + NH3·H2O = NH4+ + H2O
D.向Ba(OH)2溶液中加入H2SO4溶液: Ba2++ OH-+ H+ +SO42-= BaSO4↓+ H2O
5.下列情况下,反应速率相同的是 ( )
A.等质量锌粒和锌粉分别与等量1 mol/L HCl反应
B.等体积等浓度盐酸和醋酸分别与等质量的Na2CO3粉末反应
C.等体积0.1 mol/L HCl和0.05 mol/L H2SO4分别与等体积0.2 mol/L NaOH液反应
D.等体积0.2 mol/L HCl和0.1 mol/L H2SO4与等质量、等品质的石灰石反应
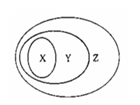
4.右图用交叉分类法表示了一些物质或概念之间的从属或包含关系,其中不正确的是( )
|
|
X |
Y |
Z |
|
例 |
氧化物 |
化合物 |
纯净物 |
|
A |
硫酸铜 |
盐 |
纯净物 |
|
B |
盐酸 |
电解质溶液 |
分散系 |
|
C |
碱性氧化物 |
氧化物 |
化合物 |
|
D |
置换反应 |
氧化还原反应 |
离子反应 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com