
9.将2LN2和6 LH2充入密闭容器里反应,达到平衡时,混合气体的体积为7.2L,计算:
(1)平衡时,混合气体里各气体物质的质量分数。
(2)N2转化为NH3的转化率。
(3)混合气体中NH3全部被0.005L水吸收,所得氨水的物质的量浓度是多少?(氨水的密度为0.96g/mL,气体在标况下)质量分数是多少?
8.总压强为3.0×107Pa时,氮氢混合气体(体积比为1:3)通入合成塔,反应达平衡时的压强降为2.5×107Pa。则平衡时混合气体中氨的体积分数为( )。
(A)35% (B)30% (C)25% (D)20%
7.在3H2 + N2 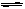 2NH3反应中,使用催化剂的理由是( )。
2NH3反应中,使用催化剂的理由是( )。
(A)使平衡向正反应方向移动 (B)没有催化剂该反应不能发生
(C)使化学反应速率增大 (D)遏止逆反应的发生
6.在一定条件下,合成氨反应达到平衡后,混合气体中NH3的体积分数为25%。若反应前后条件保持不变,则反应后缩小的气体体积与原反应物体积之比是( )。
(A)1:5 (B)1:4 (C)1:3 (D)1:2
5.工业上用氨和二氧化碳反应合成尿素。已知下列物质在一定条件下均能与水反应产生H2和CO2,H2是合成氨的原料,CO2供合成尿素用。若从充分利用原料的角度考虑,选用____物质作原料较好。
(A)CO (B)石油脑(C5H12、C6H14) (C)CH4 (D)焦炭
4.下面是合成氨的简要流程示意图(如图2-4-1):
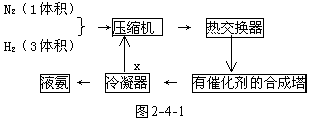
沿x路线回去的物质的是( )。
(A)N2和H2 (B)催化剂 (C)N2 (D)H2
3.在某合成氨厂合成氨的反应中,测得合成塔入口处气体N2、H2、NH3的体积比为6:18:1,出口处气体N2、H2、NH3的体积比为9:27:8,则氮的转化率为( )。
(A)5% (B)50% (C)25% (D)20%
2.将V1L的H2和V2L的N2在一定条件下发生反应,达到平衡后,混合气体总体积为V3L(气体体积均在相同条件下测定),则生成NH3的体积是( )。
(A)(V1+V2-V3)L (B)(V1+V2+V3)L
(C)(V1+V2-2V3)L (D)[V3-(V1+V2)]L
1.在现代无机化工、有机化工、生物化工等生产中,大多数产品的合成往往需要使用的主要化学反应条件是( )。
(A)高温 (B)高压 (C)催化剂 (D)高温、高压、催化剂
2.能力和方法目标
(1)通过合成氨生产条件的分析和选择,使学生了解应化学原理选择化工生产条件的思路和方法。
(2)通过用化学反应速率理论、化学平衡理论选择合成氨反应条件,培养知识的综合应用和归纳能力。
(3)通过合成氨对工业、农业等领域的重要作用的教育,让学生理解化学对于改善人类生活的重要意义。
[教学过程]
课堂练习:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com