

分析数据,观察实验装置图,回答下列问题:
(1)组装完成后,某同学发现该装置在设计上存在明显缺陷:根本无法完成实验,甚至存在危险,其缺陷在于 ,经小组研究后,稍作改进就可继续实验了;
(2)改进装置后,如何检查一侧装置的气密性?
方法是:__________________________________________________________________;
(3)欲配制100mL实验所需浓度的盐酸,除烧杯、酸式滴定管、胶头滴管之外,还需用到的主要玻璃仪器是 ;
(4)在实验数据中
①t(a1)远远大于t(b1)的原因为: ;
②由 [用 含t(b1)、 t(b2)、 t(b3)代数式表示]说明盐酸是强酸不存在电离平衡;由 [用 含t(a1)、 t(a2)、 t(a3)代数式表示]说明醋酸中存在电离平衡。
(5)该实验能得到什么结论?(回答出两点即可)
① ;
② 。
(6)通过实验判断,实验室用过量锌与稀盐酸制取氢气时,若要减慢反应速率而不影响产生氢气的量,可以加入 (填写两种不同作用原理的物质)。
【选做部分】
共8题,考生必须从中选择2个物理题、1个化学题和1个生物题在答题纸规定的区域作答。
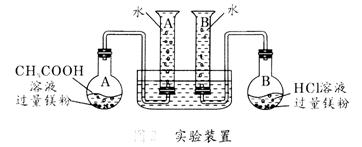 30.(15分)某校科技活动小组用镁粉、盐酸、醋酸设计以下实验,对两种酸分别与镁反应的速率和电离平衡理论进行研究,设计的实验装置如图所示(夹持固定装置已略去)。
30.(15分)某校科技活动小组用镁粉、盐酸、醋酸设计以下实验,对两种酸分别与镁反应的速率和电离平衡理论进行研究,设计的实验装置如图所示(夹持固定装置已略去)。
正确操作,记录得到下表中的部分实验数据。
 ①高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压,高铁电池的总反应为:
①高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压,高铁电池的总反应为:
则放电时正极材料是__________,负极电极反应式为____________________________,放电时___________极附近溶液的碱性增强。
②高铁酸钾(K2FeO4)是一种强氧化剂,工业上可先制得高铁酸钠,制备高铁酸钠的两种方法的主要反应原理如下:
湿法制备――2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O;
干法制备――2FeSO4 +6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。
然后在低温下向高铁酸钠溶液中加入一定量的KOH,可析出高铁酸钾。
由以上信息可知:高铁酸钠溶解度比高铁酸钾____________(填“大”或“小”),每生成l mol Na2FeO4湿法和干法转移的电子数比为_____________,K2FeO4可以和水反应生成铁的氢氧化物和氧气,则该反应的离子方程式为___________________________(不必配平)。
已知: N2(g) + 2O2(g) = 2NO2(g); △H = + 67.7kJ/mol
N2H4(g) + O2(g) = N2(g) + 2H2O(g); △H = ? 534kJ/mol
则肼和NO2反应的热化学方程式为__________________________________________
(3)化学能与电能
29.(13分)化学能的利用是化学研究的重要方面,化学能的利用包括化学能与热能、光能、电能的转化。
(1) 化学能与光能
下列关于化学能与光能的说法不正确的是___________(填编号)。
A.化石能源是远古太阳能转化为化学能而储存下来的
B.光能转化为化学能最重要的是植物的光合作用
C.利用太阳能分解水制取氢气是光能转化为化学能的过程
D.灯泡通电发光就是化学能转化为光能的过程
(2)化学能与热能
肼(N2H4)又称联氨,是一种可燃性的液体。发射“神六”时用肼(N2H4)作为火箭发动机的燃料,NO2为氧化剂,反应生成N2和水蒸气。
 电解结束时,消耗水的质量为__________;溶液的pH为______________(体积的变化忽 略不计)。
电解结束时,消耗水的质量为__________;溶液的pH为______________(体积的变化忽 略不计)。
III. 某含0.02molNaCl与0.02molCuSO4的混合溶液200 mL,
常温下在恒定电压和电流的情况下进行电解,当40s时,阴极开始产生气体,100s时电解结束,此时两极产生的气体体积理论上相同,请在下图中画出阴阳两极产生气体的体积(已换算成标准状况下的体积)与时间的关系图。
2SO2 (g) + O2 (g)  2SO3(g) ,其△H<0。当反应达
2SO3(g) ,其△H<0。当反应达
到平衡时,活塞位置如图2所示,则达到平衡时,SO2的转化
率为__________;该条件下反应的平衡常数为____________。
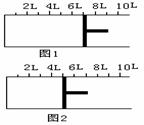 II.如右图所示,一定条件下将1mol O2气体和2mol
SO2气体充入一容积可变的密闭容器中,可滑动的活塞的位置如图1
II.如右图所示,一定条件下将1mol O2气体和2mol
SO2气体充入一容积可变的密闭容器中,可滑动的活塞的位置如图1
所示。在恒温恒压下发生如下反应:
 请回答下列问题:
请回答下列问题:
(1)下列关于PAFC的说法正确的是____________(填编号);
A.PAFC是一种无机高分子化合物
B.PAFC中Fe显+2价
C.PAFC溶于水能电离出OH-,是一种碱
D.PAFC在强酸性和强碱性溶液中均不能稳定存在
(2)写出上述流程中酸性溶液加入NaClO3时,发生反应的离子方程式:
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com