
19. (2010天津卷7).X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。
回答下列问题:
⑴ L的元素符号为________ ;M在元素周期表中的位置为________________;五种元素的原子半径从大到小的顺序是____________________(用元素符号表示)。
⑵ Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为___,B的结构式为____________。
⑶ 硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为_______,其最高价氧化物对应的水化物化学式为_______。该族2 ~ 5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1 mol硒化氢反应热的是__________(填字母代号)。
a.+99.7 mol·L-1 b.+29.7 mol·L-1 c.-20.6 mol·L-1 d.-241.8 kJ·mol-1
⑷ 用M单质作阳极,石墨作阴极,NaHCO3溶液作电解液进行电解,生成难溶物R,R受热分解生成化合物Q 。写出阳极生成R的电极反应式:______________;由R生成Q的化学方程式:_______________________________________________。
18. X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:① 元素周期表中,Z与Y相邻,Z与W也相邻; ② Y、Z和W三种元素的原子最外层电子数之和为17。 请填空:
⑴.Y、Z和W三种元素是否位于同一周期(填“是”或“否”) ,理由是
。
⑵.Y是 、Z是 、W是 (填元素符号)。
⑶.X、Y、Z和W可组成一种化合物,其原子个数之比为8:2:4:1。写出该化合物的名称及化学式 。
17. (09天津卷)下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
(09天津卷)下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
族 周期 周期 |
IA |
|
0 |
|||||
|
1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
|
2 |
|
|
|
② |
③ |
④ |
|
|
|
3 |
⑤ |
|
⑥ |
⑦ |
|
|
⑧ |
|
(1)④、⑤、⑥的原子半径由大到小的顺序为_________________________。
 (2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是_________________________。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是_________________________。
 (3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
 (4)由表中两种元素的原子按1:1组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号)_________________。
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号)_________________。
 a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
 (5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:


 X溶液与Y溶液反应的离子方程式为_____________________,
X溶液与Y溶液反应的离子方程式为_____________________,
 N→⑥的单质的化学方程式为________________。
N→⑥的单质的化学方程式为________________。
 常温下,为使0.1 mol/L M 溶液中由M电离的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至_________________。
常温下,为使0.1 mol/L M 溶液中由M电离的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至_________________。
16. (09上海卷).海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等。
(09上海卷).海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等。
 (1)在光照条件下,氯气和氢气反应过程如下:
(1)在光照条件下,氯气和氢气反应过程如下:
 ①
① ②
② ③
③ ……
……
 反应②中形成的化合物的电子式为
;反应③中被破坏的化学键属
反应②中形成的化合物的电子式为
;反应③中被破坏的化学键属
 于
键(填“极性”或“非极性”)。
于
键(填“极性”或“非极性”)。
 (2)在短周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是
(2)在短周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是
 (用元素符号表示)。与氯元素同周期且金属性最强的元素位于周期表的第 周期
族。
(用元素符号表示)。与氯元素同周期且金属性最强的元素位于周期表的第 周期
族。
 (3)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是 。
(3)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是 。
 a.卤化银的颜色按AgCl、AgBr、AgI 的顺序依次加深
a.卤化银的颜色按AgCl、AgBr、AgI 的顺序依次加深
 b.卤化氢的键长按H-F、H-C1、H-Br、H-I的顺序依次减小
b.卤化氢的键长按H-F、H-C1、H-Br、H-I的顺序依次减小
 c.卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
c.卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
 d.卤素单质与氢气化合按
d.卤素单质与氢气化合按 、
、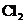 、
、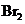 、
、 的顺序由难变易
的顺序由难变易

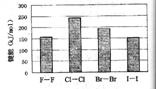 (4)卤素单质的键能大小如右图。由图推断:
(4)卤素单质的键能大小如右图。由图推断:
 ①非金属性强的卤素,其单质分子的化学键
①非金属性强的卤素,其单质分子的化学键
 断裂(填“容易”或“不容易”或“不一定容易”)。
断裂(填“容易”或“不容易”或“不一定容易”)。
 ②卤素单质键能大小与键长的关系为:
②卤素单质键能大小与键长的关系为:

14.(2004江苏理综,16)X、Y、Z均为短周期元素,它们的原子核外最外层电子数分别为1、6、6。Z位于Y的上一周期,则这三种元素形成的某种化合物的化学式可能为
A.X2YZ4 B.XY2Z3 C.X3YZ4 D.X2YZ5
 15(09上海卷).根据以下事实得出的判断一定正确的是
15(09上海卷).根据以下事实得出的判断一定正确的是

 A.HA的酸性比HB的强,则HA溶液 pH比HB溶液的小
A.HA的酸性比HB的强,则HA溶液 pH比HB溶液的小
 B.
B. 和
和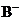 的电子层结构相同,则A原子的核电荷数比B原子的大
的电子层结构相同,则A原子的核电荷数比B原子的大
 C.A盐的溶解度在同温下比B盐的大,则A盐溶液的溶质质量分数比B盐溶液的大
C.A盐的溶解度在同温下比B盐的大,则A盐溶液的溶质质量分数比B盐溶液的大
 D.A原子失去的电子比B原子的多,则A单质的还原性比B单质的强
D.A原子失去的电子比B原子的多,则A单质的还原性比B单质的强
13.有两种短周期元素X和Y,可组成化合物XY3,当Y的原子序数为m时,X的原子序数为 ① m-4 ② m+4 ③ m+8 ④ m-2 ⑤ m+6。其中正确的组合是
A.只有①②④ B.只有①②⑤ C.①②③⑤ D.①②③④⑤
12.据国外有关资料报道,在独居石(一种共生矿,化学成分为Ge, La, Nb,…的磷酸盐)中,查明尚有未命名的116、124、126号元素。试判断,116号元素应位于周期表中的
A.第6周期ⅣA族 B.第7周期ⅥA族 C.第7周期Ⅷ族 D.第8周期ⅥA族
10.短周期元素X、Y的原子序数相差2,下列有关叙述正确的是
A.X与Y不可能位于同一主族 B.X与Y一定位于同一周期
C.X与Y可能形成共价化合物XY D.X与Y不可能形成离子化合物XY
11(09海南卷).门捷列夫在描述元素周期表时,许多元素尚未发现,但他为第四周期的三种元素留下了空位,并对它们的一些性质做了预测,X是其中的一种“类硅”元素,后来被德国化学家文克勒发现,并证实门捷列夫当时的预测相当准确。根据元素周期律,下列有关X性质的描述中错误的是
A.X单质不易与水反应
B.XO2可被碳或氢还原为X C . XCl4的沸点比SiCl4的高 D.XH4的稳定性比SiH4的高
C . XCl4的沸点比SiCl4的高 D.XH4的稳定性比SiH4的高
8.下列叙述正确的是
A.同一主族的元素,原子半径越大,其单质的熔点一定越高
B.同一周期元素的原子,半径越小越容易失去电子
C.同一主族元素的氢化物,相对分子质量越大,它的沸点一定越高
D.稀有气体元素的原子序数越大,其单质的沸点一定越高
 9(09四川).X、Y、Z、M是元素周期表中前20号元素,其原子序数依次增大,且X、Y、Z相邻。X的核电荷数是Y是核外电子数的一半,Y与M可形成化合物
9(09四川).X、Y、Z、M是元素周期表中前20号元素,其原子序数依次增大,且X、Y、Z相邻。X的核电荷数是Y是核外电子数的一半,Y与M可形成化合物 。下列说法正确的是
。下列说法正确的是
A.  还原性:X的氧化物>Y的氧化物>Z的氢化物
还原性:X的氧化物>Y的氧化物>Z的氢化物
B.  简单离子的半径:M的离子>Z的离子>Y的离子>X的离子
简单离子的半径:M的离子>Z的离子>Y的离子>X的离子
C.  YX
YX 、M
、M Y都是含有极性键的极性分子
Y都是含有极性键的极性分子
D.  Z元素的最高价氧化物的水化物的化学式为HZO4
Z元素的最高价氧化物的水化物的化学式为HZO4
5. R、W、X、Y、Z为原子序数依次递增的同一短周期的元素,下列说法一定正确的是(m、n均为正整数)
A.若R(OH)n为强碱,则W(OH)n+1也为强碱
B.若HnXOm为强酸,则Y是活泼非金属元素
C.若Y的最低化合价为-2,则Z的最高正化合价为+6
D.若X的最高正化合价为+5,则五种元素都是非金属元素
6(09山东卷). 元素在周期表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是高考资
元素在周期表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是高考资
A.同一元素不可能既表现金属性,又表现非金属性
 B.第三周期元素的最高正化合价等于它所处的主族序数
B.第三周期元素的最高正化合价等于它所处的主族序数
 C.短周期元素形成离子后,最外层电子都达到8电子稳定结构
C.短周期元素形成离子后,最外层电子都达到8电子稳定结构
 D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同
D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同
 7(09江苏卷). X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是
7(09江苏卷). X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是
 A.元素Y、Z、W具有相同电子层结构的离子,其半径依次增大
A.元素Y、Z、W具有相同电子层结构的离子,其半径依次增大
 B.元素X不能与元素Y形成化合物
B.元素X不能与元素Y形成化合物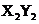
 C.元素Y、R分别与元素X形成的化合物的热稳定性:
C.元素Y、R分别与元素X形成的化合物的热稳定性:
 D.元素W、R的最高价氧化物的水化物都是强酸
D.元素W、R的最高价氧化物的水化物都是强酸
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com