
17.设NA表示阿伏加德罗常数,下列叙述中正确的是
A.常温常压下,20g
D2O跟足量钠反应产生气体的分子数为0.1NA
B.1
mol Cu跟足量浓硫酸反应,被还原的硫酸分子数为2NA
 C.标准状况下, 密闭容器中22.4L NO2气体含有的分子数为NA
C.标准状况下, 密闭容器中22.4L NO2气体含有的分子数为NA
D.常温常压下,62g白磷分子( )中的共价键数为3NA
16.相同状况下,将氮气、氯化氢的混和气体(体积比1:1)和纯净的氨气,分别充满两个干燥的烧瓶做喷泉实验。实验结束后两个烧瓶中所得溶液的物质的量浓度之比为
A.1:1 B.1:2 C.2:1 D.无法确定
15.可用于区别Na2SO3、Na2SO4、Na2CO3、Na2SiO3四种溶液的一种试剂是
A.NaOH B.盐酸
C.酚酞试液
D.BaCl2
14.向2 L密闭容器里充入2 mol M和一定量的N,发生如下反应:M(g)+2N(g) E(g),当反应进行到4 min时,测知M的浓度为0.2 mol/L,则化学反应的平均速率为
E(g),当反应进行到4 min时,测知M的浓度为0.2 mol/L,则化学反应的平均速率为
A.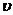 (M)=0.4 mol/(L·min) B.
(M)=0.4 mol/(L·min) B.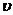 (N)=0.4 mol/(L·min)
(N)=0.4 mol/(L·min)
C.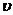 (M)=0.8 mol/(L·min) D.
(M)=0.8 mol/(L·min) D.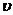 (E)=0.45 mol/(L·min)
(E)=0.45 mol/(L·min)
13.一定温度下,反应N2(g)+3H2(g) 2NH3(g)达到化学平衡状态的标志是
2NH3(g)达到化学平衡状态的标志是
A.N2、H2和NH3的质量分数不再改变

B.c(N2):c(H2):c(NH3)=1:3:2 
C.N2与H2的物质的量之和是NH3的物质的量2倍
D.单位时间里每增加1 mol N2,同时增加3 mol H2
12.下列物质中既含有离子键又含有非极性共价键的是
A.NH4Cl B.H2O C.Na2O2 D.H2O2
11.某混合气体中可能含有Cl2、O2、SO2、NO、NO2中的两种或多种。现将此无色透明的混合气体通过品红溶液,品红溶液褪色,剩余气体与空气接触,很快变为红棕色。对于原混合气体成分判断正确的是
A.肯定有SO2和NO B.肯定没有Cl2、O2和NO
C.可能有Cl2和O2 D.肯定有Cl2和NO
10.日常生活中我们经常接触到一些材料,表中对应关系错误的是
|
|
材料 |
主要化学成分 |
|
A |
刚玉、金刚石 |
三氧化二铝 |
|
B |
大理石、石灰石 |
碳酸钙 |
|
C |
普通水泥、普通玻璃 |
硅酸盐 |
|
D |
沙子、石英 |
二氧化硅 |
9.下列反应的离子方程式正确的是
A.铜与稀硝酸反应
Cu+2NO3-+4H+ = Cu2++2NO2↑+2H2O
B.碳酸钠溶液中通入二氧化碳 CO32-
+ CO2 + H2O = HCO3- 
C.在氯化铝溶液中滴入氨水 Al3++3NH3·H2O = Al(OH)3↓+3NH4+
D.向次氯酸钙溶液中通入SO2 Ca2++2ClO-+H2O+SO2 = CaSO3↓+2HClO
8.下列离子在溶液中能大量共存并且加入(NH4)2Fe(SO4)2·6H2O晶体后,仍能大量共存的是
A.Na+ H+ Cl- NO3- B.K+
Na+ OH- I-
C.Na+ Mg2+ Cl- NO3- D.Ba2+ Na+ Cl- ClO-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com