
15、(2010·成都模拟)某核素R原子核内中子数比质子数多43,由它组成的固体单质A,在一定条件下密度为6.88g·cm-3,用X射线研究其固体表明,在边长为1.0×10-7cm3的立方体中含有20个原子。R的+4价化合物在溶液中具有强氧化性,可将NO2氧化为HNO3。请回答:
(1)R原子的摩尔质量为 (取整数)。
(2)R元素的核电荷数为 ,处于周期表中第 周期 族,其元素符号为 。
(3)溶液中不存在R4+,假若能使少量R4+加到FeCl2溶液中,是否会发生反应?
若“否”,其原因为: 。(若“是”,则不答)
若“是”,其离子反应方程式为: 。(若“否”,则不答)
(4)R3O4因具有氧化性,被大量用于油漆涂料,涂在钢铁表面,有利于形成耐腐蚀的钝化层。已知R3O4与足量的HNO3反应,生成R的氧化物、R的硝酸盐和水三种物质,此反应的离子方程式为:
[答案](1)207g/mol (2)82 6 ⅣA Pb
(3)Pb4++2Fe2+= Pb2++2Fe3+ (4)Pb3O4+4H+=PbO2+2Pb2++2H2O
()
14、(2010·上海徐汇区模拟)已知20℃时,CO2密度为1.83g/L,Ca(OH)2的溶解度为0.165g/100g H2O。20℃时,将NaOH和Ca(OH)2的混合物2.02 g全部溶于897g水中配制成稀溶液,再缓缓通入CO2气体(不考虑溶解过程中溶质之间溶解性的相互影响)。
计算:(计算结果精确到0.01)
(1)20℃时,CO2的气体摩尔体积为____________________L/mol;
(2)若消耗369mL CO2气体时,生成沉淀的质量刚好达到最大,求原混合物中NaOH的质量。
(3)若在上述溶液中缓缓通入CO2气体,使其充分反应,理论上消耗CO2的总体积为VmL,则V的取值范围为 。
[答案](1)24.04; (2)1.28g
(3)1214.02<V<1286.14
13、(2010·惠州模拟)(1)有一包白色固体粉末,可能由Na2CO3 和NaHCO3,请设计实验确定该白色粉末的成分(用化学方程式表示): 。
(2)现有纯碱溶液、酚酞溶液、氯化钙溶液,请设计一个探究纯碱溶液呈碱性是由CO32-引起的实验方案,写出主要实验步骤及实验现象:
。
[解析] 第一问比较简单,只需要根据CO3 2-和HCO3-的区别选择不同的方法即可检验出结果;第二问中探究实验的关键在于设计有无CO3 2-的对比实验,根据实验现象的对比即可确认纯碱溶液呈碱性是由CO32-引起的,而除去CO3 2-的方法通常有两种,即沉淀法和生成气体法,结合题目所给出的试剂,显然只能采取沉淀法。
[答案](1)Na2CO3+BaCl2=BaCO3↓+2NaCl(合理答案即可)
(2)用试管取少量纯碱溶液,向纯碱溶液中滴加酚酞溶液,溶液显红色;若再向该溶液中滴入过量氯化钙溶液,产生白色沉淀,且溶液红色褪去。说明纯碱溶液呈碱性是由CO32-引起的。
12、(2010·邵阳模拟)已知A、B、C、D组成的元素都属于短周期,它们之间的简单转化关系如图所示。请按要求写出有关反应的化学方程式:
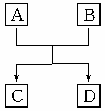
(1)若其中A、D为单质且同主族,B、C为氧化物: (该反应在工业上有重要用途) 。
(2)若A、D为常态下的气体单质且不同主族,B、C为化合物且B为水: 。
(3)若A、B、C均为化合物且C为水,单质D常态下为固体: 。
(4)若A、B、C均为氧化物,D为单质,反应是在高温下进行: 。
(5)若A、D为固体单质且不同主族,B、C为氧化物: 。
[解析]无机框图题是历年高考化学试题的重要组成部分,这类题涉及知识面广,要求学生有较高的逻辑思维能力。以短周期元素为重点。本题较综合地考查了学生对中学化学中常见的置换反应类型,中学化学阶段所涉及的置换反应类型通常有非金属置换非金属、金属置换金属、金属置换非金属、非金属置换金属四种类型,常见的有Fe2O3+2Al2Fe+Al2O3、4H2O(g)+ 3FeFe3O4+4H2、2Mg+CO2 2MgO+C、H2O(g)+ C CO+H2、SiO2+2C 2CO↑+Si、2F2+2H2O4HF+ O2、2H2O+ 2Na2NaOH+H2↑、H2(或C或CO)+CuO Cu+ H2O等;
Cu+ H2O等;
[答案](1)2C+SiO22CO+Si
(2)2F2+2H2O===4HF+O2或2Cl2+2H2O4HCl+O2
(3)SO2+2H2S===3S+2H2O
(4)CO+H2O(g)CO2+H2
(5)2Mg+CO22MgO+C
11、(2010·苏州模拟)已知25℃、101kPa下,石墨、金刚石燃烧的热化学方程式分别为:
C(石墨)+O2(g) =CO2(g);△H=-393.51kJ·mol-1
C(金刚石)+O2(g) =CO2(g);△H=-395.41kJ·mol-1”,则下列结论正确的是 ( )
A.在该条件下金刚石比石墨稳定,等质量时金刚石的能量大于石墨
B.金刚石转化为石墨为放热反应
C.石墨转化为金刚石为物理变化
D.由于石墨转化为金刚石为吸热反应,因此石墨在任何条件下都不可能转化为金刚石
[解析]选B。本题考查化学反应中的能量规律及其应用。用下一反应减去上一反应可得:C(金刚石) =C(石墨) △H=-1.9kJ·mol-1”,说明等质量时金刚石的能量大于石墨,A项错误;金刚石转化为石墨为放热反应,B项正确;石墨转化为金刚石为化学变化,C项错误;石墨在一定条件下可能转化为金刚石,D项错误。
10、(2010·临沂模拟)向饱和Na2CO3溶液中通入足量CO2,结果有晶体析出,对析出晶体的原因分析错误的是 ( )
A.相同温度下,Na2CO3的溶解度大于NaHCO3 B.溶液中溶剂减少了 C.溶质质量增加了 D.反应过程放热
[解析]选D。产生沉淀的原因不是产生的碳酸氢钠不溶于水,而是因为碳酸氢钠溶液达到了饱和,不能溶解的碳酸氢钠沉淀了下来。从化学方程式中可以算出,如果有106克碳酸钠参加反应的话,可以生成168克碳酸氢钠.因为原溶液是"饱和"的碳酸钠,反应过程中又消耗了一部分的水。且同温度下,碳酸钠的溶解度要大于碳酸氢钠,所以产生的碳酸氢钠无法全部溶解.就产生了沉淀,D项不正确。
9、(2010·长沙模拟)20世纪80年代后,人们发现和证实了碳的另一类单质,它们是由一系列偶数个碳原子组成的分子,其中C60(足球烯,分子中含有30个双键)最具代表性。下图所示为n个C60连接而成的物质X。下列有关说法不正确的是( )
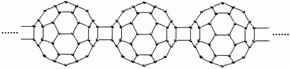
A.X难溶于水 B.一定条件下X可与H2发生加成反应
C.X是碳的一种同素异形体 D.X的摩尔质量为720g
[答案]选D。碳的单质均难溶于水,A项正确;因为该物质含有双键,一定条件下X可与H2发生加成反应,B项正确;C60是碳元素的一种单质,与金刚石、石墨互为同素异形体,C项正确;C60的摩尔质量应为720g/mol,D项错误。
8、(2010·郑州模拟)一种新型材料B4C,它可用于制作切削工具和高温热交换器。关于B4C的推断正确的是 ( )
A.B4C是一种分子晶体 B.B4C是一种离子晶体
C.B4C是一种原子晶体 D.该分子是有4个硼原子和1个碳原子构成
[解析]选C。由题意可得该物质硬度大、耐高温符合原晶体的性质,C项正确。
7、(2010·重庆模拟)已知(OCN)2的电子式为 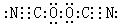 ,则SCN– 的电子式正确的是( )
,则SCN– 的电子式正确的是( )
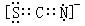
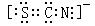 A.
B.
A.
B.
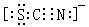
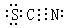 C.
D.
C.
D.
[解析]选D。
6、(2010·郑州模拟)碳与它非相邻的短周期元素以极性键形成的化合物中,各原子最外层都达到了8电子稳定结构。满足这种关系的元素共有( )
A.3种 B.4种 C.5种 D.6种
[解析]选B。CO2,CF4,CS2,CCl4均符合题意,B项正确。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com