
28、(15分)
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放100 g 5.00%的NaOH溶液、足量的CuSO4溶液和100 g 10.00%的K2SO4溶液,电极均为石墨电极。

(1)接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。据此回答问题:
①电源的N端为______极;
②电极b上发生的电极反应为_________________________;
③列式计算电极b上生成的气体在标准状况下的体积:
_________________________________
④电极c的质量变化是_________g;
⑤电解前后各溶液的酸、碱性大小是否发生变化,简述其原因:
甲溶液______________________________;
乙溶液______________________________;
丙溶液______________________________;
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么?
______________________________________。
答案. (1)①正极 ②4OH--4e-=2H2O + O2↑。③2.8L ④16g ⑤甲增大,因为相当于电解水;乙减小,OH-放电, H+增多。丙不变,相当于电解水。(2)可以
[解析](1)①乙中C电极质量增加,则c处发生的反应为:Cu2++2e-=Cu,即C处为阴极,由此可推出b为阳极,a为阴极,M为负极,N为正极。丙中为K2SO4,相当于电解水,设电解的水的质量为xg。由电解前后溶质质量相等有,100×10%=(100-x)×10.47%,得x=4.5g,故为0.25mol。由方程式2H2+O2  2H2O可知,生成2molH2O,转移4mol电子,所以整个反应中转化0.5mol电子,而整个电路是串联的,故每个烧杯中的电极上转移电子数是相等的。②甲中为NaOH,相当于电解H2O,阳极b处为阴离子OH-放电,即4OH--4e-=2H2O + O2↑。③转移0.5mol电子,则生成O2为0.5/4=0.125mol,标况下的体积为0.125×22.4=2.8L。④Cu2++2e-=Cu,转移0.5mol电子,则生成的m(Cu)=0.5/2 ×64 =16g。⑤甲中相当于电解水,故NaOH的浓度增大,pH变大。乙中阴极为Cu2+放电,阳极为OH-放电,所以H+增多,故pH减小。丙中为电解水,对于K2SO4而言,其pH几乎不变。(2)铜全部析出,可以继续电解H2SO4,有电解液即可电解。
2H2O可知,生成2molH2O,转移4mol电子,所以整个反应中转化0.5mol电子,而整个电路是串联的,故每个烧杯中的电极上转移电子数是相等的。②甲中为NaOH,相当于电解H2O,阳极b处为阴离子OH-放电,即4OH--4e-=2H2O + O2↑。③转移0.5mol电子,则生成O2为0.5/4=0.125mol,标况下的体积为0.125×22.4=2.8L。④Cu2++2e-=Cu,转移0.5mol电子,则生成的m(Cu)=0.5/2 ×64 =16g。⑤甲中相当于电解水,故NaOH的浓度增大,pH变大。乙中阴极为Cu2+放电,阳极为OH-放电,所以H+增多,故pH减小。丙中为电解水,对于K2SO4而言,其pH几乎不变。(2)铜全部析出,可以继续电解H2SO4,有电解液即可电解。
27、(15分)
浓H2SO4和木炭在加热时发生反应的化学方程式是
2H2SO4(浓)+C  CO2↑+2H2O+2SO2↑
CO2↑+2H2O+2SO2↑
请从下图中选用所需的仪器(可重复选用)组成一套进行该反应并要检出反应产物的装置。现提供浓H2SO4、木炭和酸性KMnO4溶液,其他固、液试剂自选。(连接和固定仪器所用的玻璃管、胶管、铁夹、铁架台及加热装置等均略去)

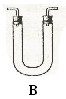

将所选的仪器连接顺序由上至下依次填入下表,并写出该仪器中应加试剂的名称及其作用。
|
选用的仪器 (填字母) |
加入的试剂 |
作用 |
|
|
|
|
答案. C 浓硫硫和木炭 产生反应物
B 无水硫酸铜 检验是否有水
A 品红 检验SO2
A 酸性KMnO4 除去SO2
A 品红 检验SO2是否除尽
A 澄清石灰水 检验CO2的存在。
[解析]成套装置包括反应装置,检验装置和尾气处理装置。C中加入浓硫硫和木炭作为反应物的发生器,产物中必须先检验水,因为在检验其他物质时会在其它试剂中混入水,可选用装置B,放入无水硫酸铜,若变蓝则说明有水。接着检验SO2气体,用装置A,放入品红检验,若品红褪色,则说明有SO2气体产生,再用装置A,放入酸性KMnO4溶液以除去SO2,然后再用装置A,放入品红,检验品红是否除尽,因为CO2是用澄清石灰水来检验的,而SO2也可以使澄清石灰水变浑,故先要除去SO2。
13、下图表示反应X(g) 4Y(g)+Z(g),△H<0,在某温度时X的浓度随时间变化的曲线:
4Y(g)+Z(g),△H<0,在某温度时X的浓度随时间变化的曲线:
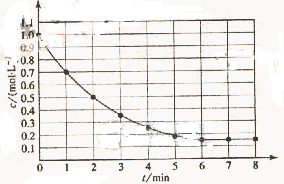
下列有关该反应的描述正确的是
A.第6 min 后,反应就终止了
B.X的平衡转化率为85%
C.若升高温度,X的平衡转化率将大于85%
D.若降低温度,v正和v逆将以同样倍数减小
答案.B
[解析]A项,6min时反应达平衡,但未停止,故错;B项,X的变化量为1-0.15=0.85mol,转化率为0.85/1=85%,正确。H<0,反应为放热,故升高温度,平衡将逆向移动,则X的转化率减小,C项错;D项,降温,正、逆反应速率同时减小,但是降温平衡正向移动,故V正>V逆,即逆反应减小的倍数大,错误。
12、有关下图所示化合物的说法不正确的是
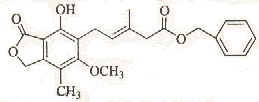
A.既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应
B.1 mol 该化合物最多可以与3 mol NaOH反应
C.既可以催化加氢,又可以使酸性KMnO4溶液褪色
D.既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体
答案.D
[解析]有机物含有碳碳双键,故可以与Br2发生加成反应,又含有甲基,故可以与Br2光照发生取代反应,A项正确;B项,酚羟要消耗一个NaOH,两个酯基要消耗两个NaOH,正确;C项,苯环可以催化加氢,碳碳双键可以使KMnO4褪色,正确;该有机物中不存在羧基,故不能与NaHCO3放出CO2气体,D项错。
11、为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将w1 g 样品加热,其质量变为w2 g ,则该样品的纯度(质量分数)是
A.  B.
B.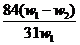 C.
C.  D.
D.
答案.A
[解析]2NaHCO3  Na2CO3 + CO2↑ + H2O m (减少)
Na2CO3 + CO2↑ + H2O m (减少)
2×84 106 62
x (W1- w2)
解得x= ,将其带入下式可得: w(Na2CO3)= (w1- x )/W1 =
,将其带入下式可得: w(Na2CO3)= (w1- x )/W1 =  ,A项正确。
,A项正确。
10、用0.10 mol·L-1的盐酸滴定0.10 mol·L-1的氨水,滴定过程中不可能出现的结果是
A.c(NH4+)>c(Cl-),c(OH-)>c(H+)
B.c(NH4+)=c(Cl-),c(OH-)=c(H+)
C.c(Cl-)> c(NH4+), c(OH-)>c(H+)
D.c(Cl-)> c(NH4+),c(H+)> c(OH-)
答案.C
[解析]溶液中不可能出现阴离子均大于阳离子的情况,不遵循电荷守恒,故C项错。
9、现有乙酸和两种链状单烯烃的混合物,若其中氧的质量分数为a,则碳的质量分数是
A.  B.
B. a C.
a C. 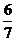 (1-a) D.
(1-a) D. (1-a)
(1-a)
答案.C
[解析]乙酸的化学式为C2H4O2,而单烯烃的通式为CnH2n,从化学式可以发现两者中,C与H之间的数目比为1:2,质量比为6:1,碳氢的质量分数一共为1-a,其中碳占 。
。
8、下列表示溶液中发生反应的化学方程式错误的是
A.2Al+2NaOH+2H2O=2NaAlO2+3H2↑
B.KMnO4+HCOOK+KOH=2K2MnO4+CO2↑+H2O
C.MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
D.K2Cr2O7+6FeSO4+7H2SO4=Cr2(SO4)3+3Fe2(SO4)3+K2SO4+7H2O
答案.B
[解析]在碱性条件下,可能产生CO2气体,而应是CO32 -,故B项错。
7、将15 mL 2 mol·L-1 Na2CO3溶液逐滴加入到40 mL 0.5 mol·L-1 MCln盐溶液中,恰好将溶液中的Mn+离子完全沉淀为碳酸盐,则MCln中n值是
A.4 B.3 C.2 D.1
答案.B
[解析]M的化合价为+n,Na2CO3与MCln反应对应的关系式为:2Mn+ ~ nCO32 -
2 n
15×10-3×2 40×10-3×0.5
可得n=3,故选B。
6、下列各组离子,在溶液中能大量共存、加入NaOH溶液后加热既有气体放出又有沉淀生成的一组是
A.Ba2+、NO3-、NH4+、Cl-
B.Ca2+、HCO3-、NH4+、AlO2-
C.K+、Ba2+、Cl-、HSO3-
D.Mg2+、NH4+、SO42-、K+
答案.D
[解析]A项,加入NaOH会与NH4+ 产生NH3,但没有沉淀;B项HCO3- 与AlO2- 不能共存,会生成Al(OH)3 沉淀。C项,OH-与HSO3- 生成SO32 -,与Ba2+可生成BaSO3沉淀,但无气体。D项,OH-与NH4+ 产生NH3,与Mg2+会产生Mg(OH)2沉淀,正确。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com