
5. 科学家利用精密的仪器把石墨拆成只有一个或几个原子层厚的“碳片”(示意图如下),碳片是世界上最薄的材料。下列说洪错误的是[ ]
科学家利用精密的仪器把石墨拆成只有一个或几个原子层厚的“碳片”(示意图如下),碳片是世界上最薄的材料。下列说洪错误的是[ ]
A.碳片是一种单质
B.碳片和C60是同一种物质
C.在一定条件下,碳片可还原氧化铁
D.碳片在氧气中完全燃烧的产物是CO2
6.下图是两种气体发生反应的微观示意图,其中相同的球代表同种原子。下列说法正确的是[ ]

A.分子在化学变化中不可分 B.反应后生成了两种新的化合物
C.原子在化学反应中可分 D.化学反应前后原子的种类不变
4.下列实验操作或装置正确的是[ ]
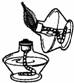
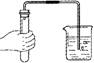
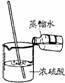

A.点燃酒精灯 B.检验气密性 C.稀释浓硫酸 D.收集氢气
3.我省的祁门红茶是“世界四大红茶”之一,由于香叶醇(C10H18O)的含量高于普通茶叶的几十倍,因而具有独特的玫瑰花香。下列关于香叶醇的说法错误的是[ ]
A.由C、H、O三种元素组成 B.闻到玫瑰花香说明分子在不断运动
C.属于有机化合物 D.组成元素中,氢元素的质量分数最大
2.下列各组食品中蛋白质含量最丰富的是[ ]
A.黄瓜、西红柿B.鸡蛋、牛肉C.米饭、大摸D.苹果、梨子
1.材料是人类文明进步的标志。下列不同时代物品的材料在加工、制取过程中只发生物理变化的是[ ]




A.石器 B.青铜器 C.铁器 D.高分子材料
36.(09年山东理综·31)(8分)(化学-化学与技术)
金属铝的生产是以Al2O,为原料,在熔融状态下进行电解:2Al2O3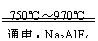
 4Al+3O2↑
4Al+3O2↑
请回答下列问题:
(1)冰晶石(Na3AIF6)的作用是 。
(2)电解生成的金属铝是在熔融液的 (填“上层”或“下层”)。
(3)阴极和阳极均由 材料做成;电解时不断消耗的电极是 (填“阳极”或“阴极”)。
(4)铝是高耗能产品,废旧铝材的回收利用十分重要。在工业上,最能体现节能减排思想的是将回收铝做成 (填代号)。
a.冰晶石 b.氧化铝 c.铝锭 d.硫酸铝
答案:(1)降低Al2O3的熔化温度 (2)下层(3)碳素(或石墨) 阳极(4)c
 解析:Al2O3的熔点很高,熔化得需要较多能量,加入助熔剂就可节约能量,降低熔化温度
解析:Al2O3的熔点很高,熔化得需要较多能量,加入助熔剂就可节约能量,降低熔化温度
 (2)由于冰晶石(Na3AlF6)与氧化铝熔融物密度比铝的小,所以铝在熔融液的下层。
(2)由于冰晶石(Na3AlF6)与氧化铝熔融物密度比铝的小,所以铝在熔融液的下层。
 (3)电解时阳极的碳棒被生成的氧气氧化。
(3)电解时阳极的碳棒被生成的氧气氧化。
 (4)电解产生的铝要尽量以单质形式存在,所以将回收铝做成铝锭最好。
(4)电解产生的铝要尽量以单质形式存在,所以将回收铝做成铝锭最好。
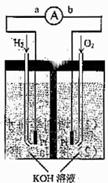
37 .(09年天津理综·10)(14分)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
.(09年天津理综·10)(14分)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
 (1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为
(用a、b表示)。
(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为
(用a、b表示)。
 (2)负极反应式为
。
(2)负极反应式为
。
 (3)电极表面镀铂粉的原因为
。
(3)电极表面镀铂粉的原因为
。
 (4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:
 Ⅰ.2Li+H2
Ⅰ.2Li+H2
 2LIH
2LIH
 Ⅱ.LiH+H2O==LiOH+H2↑
Ⅱ.LiH+H2O==LiOH+H2↑
 ①反应Ⅰ中的还原剂是
,反应Ⅱ中的氧化剂是
。
①反应Ⅰ中的还原剂是
,反应Ⅱ中的氧化剂是
。
 ②已知LiH固体密度为0.82g/cm3。用锂吸收224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为
。
②已知LiH固体密度为0.82g/cm3。用锂吸收224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为
。
 ③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为
mol。
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为
mol。
答案:(1)由化学能转化为电能 由a到b
(2)2H2+4OH--4e-=4H2O或H2+2OH--2e-=2H2O
(3)增大电极单位面积吸附H2、O2分子数,加快电极反应速率
(4)①Li H2O ②或8.71×10-4 ③32
解析:本题考查电化学知识。(1)原电池的实质为化学能转化成电能。总反应为2H2 + O2 =2H2O,其中H2从零价升至+1价,失去电子,即电子从a流向b。(2)负极为失去电子的一极,即H2失电子生成H+,由于溶液是碱性的,故电极反应式左右应各加上OH-。(3)铂粉的接触面积大,可以加快反应速率。(4)I.Li从零价升至+1价,作还原剂。II.H2O的H从+1降至H2中的零价,作氧化剂。由反应I,当吸收10molH2时,则生成20molLiH,V=m/ρ=20×7.9/0.82 ×10-3L=192.68×10-3L。V(LiH)/v(H2)= 192.68×10-3L/224L=8.71×10-4。20mol LiH可生成20mol H2,实际参加反应的H2为20×80%=1.6mol,1molH2转化成1molH2O,转移2mol电子,所以1.6molH2可转移3.2mol的电子。
35.(09年山东理综·29)(12分)Zn-MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液。
(1)该电池的负极材料是 。电池工作时,电子流向 (填“正极”或“负极”)。
(2)若ZnCl2-NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是
。欲除去Cu2+,最好选用下列试剂中的 (填代号)。
a.NaOH b.Zn c.Fe d.NH3·H2O
(3)MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阴极的电极反应式是 。若电解电路中通过2mol电子,MnO2的理论产量为 。
答案:(1)Zn(或锌) 正极
(2)Zn与Cu2+反应生成Cu,Zn与Cu构成原电池,加快反应速率 b
(3)2H++2e-=H2↑ 87g
 解析:(1) 负极上是失电子的一极 Zn失电子有负极经外电路流向正极。(2)锌与还原出来的Cu构成铜锌原电池而加快锌的腐蚀。除杂的基本要求是不能引入新杂质,所以应选Zn将Cu2+
置换为单质而除去。(3)阴极上得电子,发生还原反应, H+得电子生成氢气。因为MnSO4-MnO2-2 e-,通过2mol电子产生1molMnO2,质量为87g。
解析:(1) 负极上是失电子的一极 Zn失电子有负极经外电路流向正极。(2)锌与还原出来的Cu构成铜锌原电池而加快锌的腐蚀。除杂的基本要求是不能引入新杂质,所以应选Zn将Cu2+
置换为单质而除去。(3)阴极上得电子,发生还原反应, H+得电子生成氢气。因为MnSO4-MnO2-2 e-,通过2mol电子产生1molMnO2,质量为87g。
 [考点分析] 原电池原理和电解原理综合运用
[考点分析] 原电池原理和电解原理综合运用
34.(09年宁夏理综·37)[化学-选修化学与技术](15分)
请回答氯碱的如下问题:
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k= (要求计算表达式和结果);
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)③BaCl2,这3种试剂添加的合理顺序是 (填序号)
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
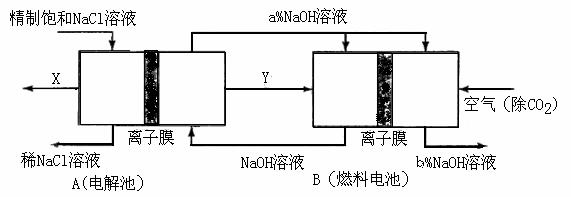 ①图中X、Y分别是
、
(填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小 ;
①图中X、Y分别是
、
(填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小 ;
②分别写出燃料电池B中正极、负极上发生的电极反应正极: ; 负极: ;
③这样设计的主要节(电)能之处在于(写出2处) 、 。
答案:(1)k=M(Cl2)/2 M(NaOH)=71/80=1:1.13或0.89(2)③①② (3)①Cl2 H2 a%小于b% ②O2+4e-+2H2O=4OH- H2-2e-+2OH-=2H2O ③燃料电池可以补充电解池消耗的电能;提高产出碱液的浓度;降低能耗(其他合理答案也给分)
解析:(1)只要了解电解饱和食盐水的化学方程式2NaCl+2H2O 2NaOH+H2↑+Cl2↑即可得到,k=M(Cl2)/2 M(NaOH)=71/80=1:1.13或0.89;(2)只要抓住除钡离子要放在除碳酸根离子前即可得到顺序关系:③①②;(3)本题突破口在于B燃料电池这边,通空气一边为正极(还原反应),那么左边必然通H2,这样Y即为H2 ;再转到左边依据电解饱和食盐水的化学方程式可知唯一未知的就是X,必然为Cl2了;A中的NaOH进入燃料电池正极再出来,依据O2+4e-+2H2O=4OH- 可知NaOH+浓度增大。
2NaOH+H2↑+Cl2↑即可得到,k=M(Cl2)/2 M(NaOH)=71/80=1:1.13或0.89;(2)只要抓住除钡离子要放在除碳酸根离子前即可得到顺序关系:③①②;(3)本题突破口在于B燃料电池这边,通空气一边为正极(还原反应),那么左边必然通H2,这样Y即为H2 ;再转到左边依据电解饱和食盐水的化学方程式可知唯一未知的就是X,必然为Cl2了;A中的NaOH进入燃料电池正极再出来,依据O2+4e-+2H2O=4OH- 可知NaOH+浓度增大。
[点评]本题前半部基本就是课本内容的再现,但后半部很有创意,可以很好的综合考查考生的原电池和电解的相关知识
33.
 (09年江苏化学·16)(8分)以氯化钾和钛白厂的副产品硫酸亚铁为原料生产硫酸钾、过二硫酸钠和氧化铁红颜料,原料的综合利用率较高。其主要流程如下:
(09年江苏化学·16)(8分)以氯化钾和钛白厂的副产品硫酸亚铁为原料生产硫酸钾、过二硫酸钠和氧化铁红颜料,原料的综合利用率较高。其主要流程如下:

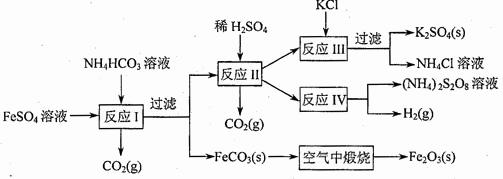
 (1)反应I前需在FeSO4溶液中加入 (填字母),以除去溶液中的Fe3+。
(1)反应I前需在FeSO4溶液中加入 (填字母),以除去溶液中的Fe3+。
 A.锌粉 B.铁屑 C.KI溶液 D.H2
A.锌粉 B.铁屑 C.KI溶液 D.H2
 (2)反应Ⅰ需控制反应温度低于35℃,其目的是
。
(2)反应Ⅰ需控制反应温度低于35℃,其目的是
。
 (3)工业生产上常在反应Ⅲ的过程中加入一定量的醇类溶剂,其目的是
。
(3)工业生产上常在反应Ⅲ的过程中加入一定量的醇类溶剂,其目的是
。
 (4)反应Ⅳ常被用于电解生产(NH4)2S2O8(二硫酸铵)。电解时均用惰性电极,阳极发生地电极反应可表示为
。
(4)反应Ⅳ常被用于电解生产(NH4)2S2O8(二硫酸铵)。电解时均用惰性电极,阳极发生地电极反应可表示为
。
 答案:(1)B
答案:(1)B
 (2)防止NH4HCO3分解(或减少Fe2+的水解)
(2)防止NH4HCO3分解(或减少Fe2+的水解)
 (3)降低K2SO4
的溶解度,有利于K2SO4 析出。
(3)降低K2SO4
的溶解度,有利于K2SO4 析出。
 (4)2SO42-
-2e-
(4)2SO42-
-2e- 2S2O82-
2S2O82-
 解析:(1)在FeSO4溶液中除去溶液中的Fe3+,最好选用铁屑或铁粉,比较简单。(2)如果温度过高会导致NH4HCO3分解同样也会加快Fe2+的水解(温度越高水解速率越快)这样会使原料利用率降低。(3)由题目看出在III反应中生成的K2SO4
为固体,而K2SO4在无机溶剂中溶解度是比较大的,要想使K2SO4析出只能降低其溶解度所以加入醇类溶剂目的降低K2SO4的溶解度。
解析:(1)在FeSO4溶液中除去溶液中的Fe3+,最好选用铁屑或铁粉,比较简单。(2)如果温度过高会导致NH4HCO3分解同样也会加快Fe2+的水解(温度越高水解速率越快)这样会使原料利用率降低。(3)由题目看出在III反应中生成的K2SO4
为固体,而K2SO4在无机溶剂中溶解度是比较大的,要想使K2SO4析出只能降低其溶解度所以加入醇类溶剂目的降低K2SO4的溶解度。
 (4)根据阴阳极反应原理阳极失电子发生氧化反应,此题实质是电解硫酸铵溶液,在根据反应后的产物得出正确的答案。
(4)根据阴阳极反应原理阳极失电子发生氧化反应,此题实质是电解硫酸铵溶液,在根据反应后的产物得出正确的答案。
 [考点分析]此题为化工生产题型,主要考察了化合物性质,电极方程式书写。做此类题要分析清楚每一个环节目的和结果是什么。这样才能判断各反应后的产物分别是什么。
[考点分析]此题为化工生产题型,主要考察了化合物性质,电极方程式书写。做此类题要分析清楚每一个环节目的和结果是什么。这样才能判断各反应后的产物分别是什么。
32. (09年海南化学·15)(9分)
(09年海南化学·15)(9分)
 Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为:4Li+2SOCl2 =4LiCl+S
+SO2。
Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2。电池的总反应可表示为:4Li+2SOCl2 =4LiCl+S
+SO2。
 请回答下列问题:
请回答下列问题:
 (1)电池的负极材料为
,发生的电极反应为
;
(1)电池的负极材料为
,发生的电极反应为
;
 (2)电池正极发生的电极反应为
;
(2)电池正极发生的电极反应为
;
 (3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。 如果把少量水滴到SOCl2中,实验现象是
,反应的化学方程式为
;
(3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。 如果把少量水滴到SOCl2中,实验现象是
,反应的化学方程式为
;
 (4)组装该电池必须在无水、无氧的条件下进行,原因是
。
(4)组装该电池必须在无水、无氧的条件下进行,原因是
。
答案::(9分)


 (1)锂 Li-2e-=Li+(2分)
(1)锂 Li-2e-=Li+(2分)
 (2)2SOCl2+4e-=4Cl-+S+SO2(2分)
(2)2SOCl2+4e-=4Cl-+S+SO2(2分)
 (3)出现白雾,有刺激性气体生成 SOCl2+H2O=SO2↑+2HCl↑(3分)
(3)出现白雾,有刺激性气体生成 SOCl2+H2O=SO2↑+2HCl↑(3分)
 (4)锂是活泼金属,易与H2O、O2反应;SOCl2也可与水反应(2分)
(4)锂是活泼金属,易与H2O、O2反应;SOCl2也可与水反应(2分)
解析:分析反应的化合价变化,可得Li为还原剂 ,SOCl2为氧化剂。
(1)负极材料为Li(还原剂),Li – e- = Li+
(2)负极反应式可由总反应减去负极反应式得到:2SOCl2 + 4 e- = 4Cl- + S + SO2
(3)题中给出有碱液吸收时的产物,则没有碱液吸收时的产物应为SO2和HCl,所以现象应该为出现白雾和有刺激性气体生成。
(4)因为构成电池的两个主要成份Li能和氧气水反应,且SOCl2也与水反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com