
16.(12分)(1)浓硫酸与木炭粉在加热条件下反应的化学方程式为___________。
(2)试用图4-18中所列各装置设计一个实验,验证上述反应所产生的各种产物。这些装置的连接顺序(按产物气流从左至右的方向)是(填装置的编号):________→______→_______→_________。
(3)实验室可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液的作用是_________,B瓶溶液的作用是__________,C瓶溶液的作用是___________。
(4)装置②中所加的固体药品是________,可确证的产物是_________,确定装置②在整套装置中位置的理由是__________。
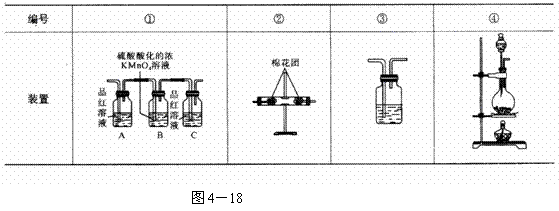
(5)装置③中所盛溶液是__________,可验证的产物是______________。
KClO3Cl2 + 6KOH  5KCl + KClO3
+ 3H2O,试回答下列问题:
5KCl + KClO3
+ 3H2O,试回答下列问题:
15.把SO2通入NaOH溶液中,当SO2和NaOH完全反应时,其质量比为6:5,则下列说法正确的是 ( )
A.反应后SO2有剩余
B.溶液还可吸收SO2
C.溶液中除OH―外,只有一种阴离子
D.溶液中溶质的物质的量之比为1∶2
14.下列说法错误的是
A.将Na2SO3与BaCl2溶液混合,有白色沉淀,加稀硝酸沉淀全部溶解
B.将CO2气体通入过量的Ba(OH)2溶液中有白色沉淀生成
C.将SO2气体通入BaCl2溶液中没有白色沉淀生成
D.将SO2气体通入硝酸酸化的BaCl2溶液中有白色沉淀生成
13.在标准状况下,将1.92g铜粉投入一定量浓度的HNO3中,随着铜粉的溶解,反应生成的气体颜色越来越浅,当铜粉完全溶解后共收集到有NO2和NO组成的混合气体1.12L,则混合气体中NO的体积为 ( )
A.112mL B.108mL C.224mL D.448mL
12.随着科技的飞速发展,出现了许多新型无机非金属材料,如植入人体内的生物陶瓷材料HAP[化学式为Cam(PO4)n(OH)2]已被医疗上用于修补人的骨和牙组织,HAP的化学式中m等于 ( )
A.(3n + 2)/ 2 B.(2n-2)/3 C.(3n-2)/2 D.n + 1
11.有一固体混合物,其中硫元素和氧元素的质量分数为x和(1-3x),则该混合物的组成可能是 ( )
A.CuSO4、FeSO4、CuSO3 B.CuSO4、CuSO3、CuS2O3
C.ZnSO4、FeSO4、CuSO4 D.CuS、Cu2S、CuSO4
10.某温度下将Cl2通入KOH溶液里,反应后得到KCl、KClO、KClO3的混合溶液,经测定ClO―与ClO3―的物质的量浓度之比为11:1,则Cl2与KOH反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为 ( )与测定O3体积相同的气体在水利枢纽温结构陶瓷
A.1:3 B.4:3 C.2:1 D.3:1
9.一定质量的铜与足量的浓硝酸或稀硝酸完全反应,在相同条件下用排水集气法收集产生的气体。下列叙述正确的是 ( )
A.硝酸浓度越大,消耗的硝酸越少
B.硝酸浓度不同,生成Cu(NO3)2物质的量相同
C.硝酸浓度越大,产生的气体越少
D.用排水集气法收集到的气体在相同状况下体积相同
8.在一倒置于水槽且装满水的容器中,依次通入一定体积的NO2、NO和O2,充分反应后,若容器中仍充满水,则通入的NO2、NO和O2体积比可能是 ( )
A.1:1:1 B.4:3:2 C.4:16:13 D.4:3:4
7.Fe与硝酸反应随温度和硝酸的浓度不同而产物不同。已知0.2mol HNO3做氧化剂时,恰好将0.4mol Fe氧化为Fe2+,则HNO3将被还原成 ( )
A.NH4+ B.N2O C.NO D.NO2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com