
29.(07年广东化学·24)(10分)
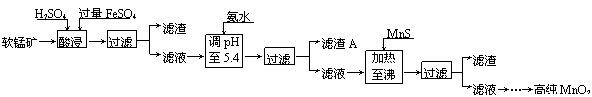 二氧化锰是制造锌锰干电池的基本材料。工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如下:
二氧化锰是制造锌锰干电池的基本材料。工业上以软锰矿为原料,利用硫酸亚铁制备高纯二氧化锰的流程如下:
某软锰矿的主要成分为MnO2,还含有Si(16.72%)、Fe(5.86%)、Al(3.42%)、Zn(2.68%)和Cu(0.86%)等元素的化合物。部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见下表,回答下列问题:
|
沉淀物 |
Al(OH)3 |
Fe(OH)3 |
Fe(OH)2 |
Mn(OH)2 |
Cu(OH)2 |
Zn(OH)2 |
CuS |
ZnS |
MnS |
FeS |
|
pH |
5.2 |
3.2 |
9.7 |
10.4 |
6.7 |
8.0 |
≥–0.42 |
≥2.5 |
≥7 |
≥7 |
(1)硫酸亚铁在酸性条件下将MnO2还原为MnSO4,酸浸时发生的主要反应的化学方程式为 。
(2)滤渣A的主要成分是 。
(3)加入MnS的目的是除去 杂质。
(4)碱性锌锰电池中,MnO2参与的电极反应方程式为 。
(5)从废旧碱性锌锰电池中可以回收利用的物质有 (写出两种)。
答案:(10分)
(1)MnO2+2FeSO4+2H2SO4=MnSO4+Fe2(SO4)3+2H2O
(2)Fe(OH)3 Al(OH)3
(3)Cu2+ Zn2+
(4)MnO2+H2O+e-=MnOOH+OH-(或2MnO2+H2O+2e-=Mn2O3+2OH-)
(5)锌、二氧化锰
解析:考查学生对元素化合物的主要性质的掌握、书写电极反应方程形式的能力以及学生能够从试题提供的新信息中,准确地提取实质内容,并与已有知识模块整合,重组为新知识模块的能力。由反应流程可知:在酸性条件下二氧化锰将Fe2+氧化为Fe3+,将Cu氧化成Cu2+,此外溶液中的还有Zn2+和Al3+,当调pH至5.4时,只有Al(OH)3 和Fe(OH)3会完全沉淀,故滤渣A的主要成分是Fe(OH)3和Al(OH)3。加入MnS后因为酸性条件下CuS 、ZnS更难溶所以会转化为CuS 、ZnS沉淀而除去Cu2+ Zn2+。
24.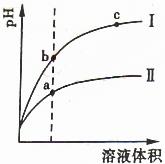 (09年山东理综·15)某温度下,相同pH值的盐酸和酸溶液分别是稀、平衡pH值随溶液体积变化的曲线如右图所示。据图判断正确的是
(09年山东理综·15)某温度下,相同pH值的盐酸和酸溶液分别是稀、平衡pH值随溶液体积变化的曲线如右图所示。据图判断正确的是 学科
学科
A.Ⅱ为盐酸稀释时pH值变化曲线
B.b点溶液的导电性比c点溶液的导电性强
C.a点Ka的数值比c点Ku的数值大
D.b点酸的总浓度大于a点酸的总浓度
答案:B
解析:本题以醋酸为例考查了弱电解质的电离平衡,II应为醋酸稀释时的pH值变化曲线;溶液导电性取决于离子浓度,b点的H+浓度大,导电性强;KW的大小只取决于温度;相同pH值的盐酸和醋酸,醋酸浓度远大于盐酸的浓度,稀释到相同体积时,醋酸(II)浓度大于盐酸(I)浓度。
25 .(09年天津理综·2)25 ℃时,浓度均为0.2 mol/L的NaHCO3和Na2CO3溶液中,下列判断不正确的是
.(09年天津理综·2)25 ℃时,浓度均为0.2 mol/L的NaHCO3和Na2CO3溶液中,下列判断不正确的是
 A.均存在电离平衡和水解平衡
A.均存在电离平衡和水解平衡
 B.存在的粒子种类相同
B.存在的粒子种类相同
 C.c(OH-)前者大于后者
C.c(OH-)前者大于后者
 D.分别加入NaOH固体,恢复到原温度,c(CO33-)均增大
D.分别加入NaOH固体,恢复到原温度,c(CO33-)均增大
答案:C
解析:相同浓度时,Na2CO3的碱性强于NaHCO3,C项错。
26 .(09年天津理综·4)下列叙述正确的是
.(09年天津理综·4)下列叙述正确的是
 A.0.1 mol/LC6H5ONa溶液中:c(Na+)>c(C6H5O-)>c(H+)>c(OH-)
A.0.1 mol/LC6H5ONa溶液中:c(Na+)>c(C6H5O-)>c(H+)>c(OH-)
 B.Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小
B.Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小
 C.pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)不相等
C.pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)不相等
 D.在Na2S溶液中加入AgCl固体,溶液中c(S2-)下降
D.在Na2S溶液中加入AgCl固体,溶液中c(S2-)下降
答案:D
解析:A项,苯酚钠为碱性溶液,故错;B项,温度不变,则Kw是不变的,错;C项,pH=5即代表溶液中c(H+)均为10-5mol/L,错。D项,Ag2S比AgCl更难溶,故加入S2-会与溶液中的Ag+结合的,正确。
27 .(09年海南化学·6)已知室温时,0.1mo1/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是:
.(09年海南化学·6)已知室温时,0.1mo1/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是:
 A.该溶液的pH=4
A.该溶液的pH=4
 B.升高温度,溶液的pH增大
B.升高温度,溶液的pH增大
 C.此酸的电离平衡常数约为1×10-7
C.此酸的电离平衡常数约为1×10-7
 D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍
D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍
答案:B
解析:根据HA在水中的电离度可算出c(H+)=0.1×
0.1%mol·L-1=10-4 mol·L-1,所以pH=4;因HA在水中有电离平衡,升高温度促进平衡向电离的方向移动,所以c(H+)将增大,pH值会减小;C选项可由平衡常数表达式算出K=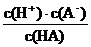 =1×10-7 ,所以C无错误。c(H+)=10-4
mol·L-1 ,所以c(H+,水电离)= 10-10
mol·L-1,前者是后才的106倍。
=1×10-7 ,所以C无错误。c(H+)=10-4
mol·L-1 ,所以c(H+,水电离)= 10-10
mol·L-1,前者是后才的106倍。
28 .(09年海南化学·11)在5mL 0.05 mo1/L的某金属氯化物溶液中,滴加0.1 mo1/L AgNO3溶液,生成沉淀质量与加入AgNO3溶液体积关系如图所示,则该氯化物中金属元素的化合价为:
.(09年海南化学·11)在5mL 0.05 mo1/L的某金属氯化物溶液中,滴加0.1 mo1/L AgNO3溶液,生成沉淀质量与加入AgNO3溶液体积关系如图所示,则该氯化物中金属元素的化合价为:


 A.+1 B.+2 C.+3 D.+4
A.+1 B.+2 C.+3 D.+4
答案:C
解析:设氯化物化学式为MClx
MClx -- x AgNO3
1 x
5mL×0.05 mol·L-1 0.1 mol·L-1×7.5mL
x = 3
23.(09年山东理综·13)下列推断合理的是
A.明矾[KAl(SO4)2·12H2O]在水中能形成Al(OH)3胶体,可用作净水剂
B.金刚石是自然界中硬度最大的物质,不可能与氧气发生反应
C.浓H2SO4有强氧化性,不能与Cu发生剧烈反应
D.将SO2通入品红溶液,溶液褪色后加热恢复原色;将SO2通入溴水,溴水色后加热也能恢复原色
答案:A
解析:明矾[KAl(SO4)2·12H2O]溶于水,电离产生的Al3+在中水解生成能吸附水中悬浮杂质的Al(OH)3胶体,故可用作净水剂;金刚石、石墨均可以燃烧生成二氧化碳;浓H2SO4虽然有强氧化性,只有加热才能与Cu发生反应;SO2通入溴水后发生氧化还原反应,SO2 +Br2 + 2H2O= H2SO4+2HBr,加热不可能生成Br2.
22.(09年宁夏理综·11)将氢氧化钠稀溶液滴加到醋酸稀溶液中,下列各图示意混合溶液有关量或性质的变化趋势,其中错误的是

答案:D
解析:A选项氢氧化钠和醋酸发生中和反应,反应放热,当酸反应完成后,再加碱,相当于往热水中加入冷水,温度降低。B选项醋酸中滴加氢氧化钠酸性减弱pH增大。C选项醋酸中滴加氢氧化钠,相当于弱电解质溶液变成强电解质溶液,因此导电能力增加。D选项醋酸中滴加氢氧化钠,氢氧化钠和醋酸发生反应了,因此氢氧化钠开始时为0.
[点评]本题考查水溶液中的离子反应的相关知识,题目容量大,对考生的能力要求很高。
18.(09年广东理基·33)下列说法正确的是
A.向0.1mol·L-1 Na2CO3溶液中滴加酚酞,溶液变红色
B.Al3+、NO3-、Cl-、CO32-、Na+可以大量共存于pH=2的溶液中
C.乙醇和乙酸都能溶于水,都是电解质
D. 分别于等物质的量的HCl和H2SO4反应时,消耗的NaOH的物质的量相同
答案:A
解析:Na2CO3溶液中存在CO32-的水解CO32-+H2O HCO3-+OH-,使溶液显碱性,因此加入酚酞后溶液变为红色,故A选项正确。B选项中pH=2的溶液显酸性,弱酸跟阴离子CO32-不能存在;C选项中的乙醇不是电解质,只有乙酸是电解质;HCl是一元酸而H2SO4是二元酸,因此等物质的量的HCl和H2SO4消耗的NaOH的物质的量之比为1︰2。
HCO3-+OH-,使溶液显碱性,因此加入酚酞后溶液变为红色,故A选项正确。B选项中pH=2的溶液显酸性,弱酸跟阴离子CO32-不能存在;C选项中的乙醇不是电解质,只有乙酸是电解质;HCl是一元酸而H2SO4是二元酸,因此等物质的量的HCl和H2SO4消耗的NaOH的物质的量之比为1︰2。
19 .(09年江苏化学·5)化学在生产和日常生活中有着重要的应用。下列说法不正确的是
.(09年江苏化学·5)化学在生产和日常生活中有着重要的应用。下列说法不正确的是
 A.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
A.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
 B.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率
B.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率
 C.MgO的熔点很高,可用于制作耐高温材料
C.MgO的熔点很高,可用于制作耐高温材料
 D.电解MgCl2饱和溶液,可制得金属镁
D.电解MgCl2饱和溶液,可制得金属镁
 答案:D
答案:D
 解析:A项,明矾净水的原理是Al3++3H2O
解析:A项,明矾净水的原理是Al3++3H2O Al(OH)3(胶体)+3H+,利用Al(OH)3(胶体)的吸附性进行净水;B项,是因为轮船主要用铁造外壳,铁在海水中易被腐蚀.镀上比铁活泼的锌,形成原电池,锌作负极,失去电子先被腐蚀,从而起到保护铁的作用,从而可减缓船体的腐蚀速率;氧化镁的熔点是2852℃,可用于制作耐高温材料;电解MgCl2饱和溶液,发生地化学反应为MgCl2+2H2O
Al(OH)3(胶体)+3H+,利用Al(OH)3(胶体)的吸附性进行净水;B项,是因为轮船主要用铁造外壳,铁在海水中易被腐蚀.镀上比铁活泼的锌,形成原电池,锌作负极,失去电子先被腐蚀,从而起到保护铁的作用,从而可减缓船体的腐蚀速率;氧化镁的熔点是2852℃,可用于制作耐高温材料;电解MgCl2饱和溶液,发生地化学反应为MgCl2+2H2O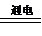 Mg(OH)2+Cl2↑+H2↑,不会产生金属镁,电解熔融的MgCl2能制取单质镁,发生的反应MgCl2(熔融)
Mg(OH)2+Cl2↑+H2↑,不会产生金属镁,电解熔融的MgCl2能制取单质镁,发生的反应MgCl2(熔融) Mg+Cl2↑。
Mg+Cl2↑。
 [考点分析](1)物质的水解反应,以及水解反应的用途;(2)常见生活常识的原理;(3)常见物质在生产生活中的具体用途;(4)常见物质的制备及发生的化学反应方程式。
[考点分析](1)物质的水解反应,以及水解反应的用途;(2)常见生活常识的原理;(3)常见物质在生产生活中的具体用途;(4)常见物质的制备及发生的化学反应方程式。
 20
20 .(09年江苏化学·9)下列化学实验事实及其解释都正确的是
.(09年江苏化学·9)下列化学实验事实及其解释都正确的是
 A.向碘水中滴加CCl4,振荡静置后分层,CCl4层呈紫红色,说明可用CCl4从碘水中萃取碘
A.向碘水中滴加CCl4,振荡静置后分层,CCl4层呈紫红色,说明可用CCl4从碘水中萃取碘
 B.向SO2水溶液中滴加盐酸酸化的BaCl2溶液,有白色沉淀生成,说明BaSO3难溶于盐酸
B.向SO2水溶液中滴加盐酸酸化的BaCl2溶液,有白色沉淀生成,说明BaSO3难溶于盐酸
 C.向0.1mol·L-1FeSO4溶液中滴加少量酸性KMnO4溶液,KMnO4溶液褪色,说明Fe2+具有氧化性
C.向0.1mol·L-1FeSO4溶液中滴加少量酸性KMnO4溶液,KMnO4溶液褪色,说明Fe2+具有氧化性
 D.向2.0mL浓度均为0.1mol·L-1的KCl、KI混合溶液中滴加1~2滴0.01mol·L-1
AgNO3溶液,振荡,沉淀呈黄色,说明AgCl的Ksp比AgI的Ksp
D.向2.0mL浓度均为0.1mol·L-1的KCl、KI混合溶液中滴加1~2滴0.01mol·L-1
AgNO3溶液,振荡,沉淀呈黄色,说明AgCl的Ksp比AgI的Ksp
 答案:AD
答案:AD
 解析:A项,是高中化学必修1一个很重要的实验---萃取实验;B项的叙述是错误的,在该实验中根本得不到白色沉淀,因为亚硫酸不可能制取盐酸;C项只能说明Fe2+具有还原性,因为KMnO4具有强氧化性,常做氧化剂。D项,沉淀呈黄色,说明沉淀是AgI,也就意味着AgCl的Ksp比AgI的大。
解析:A项,是高中化学必修1一个很重要的实验---萃取实验;B项的叙述是错误的,在该实验中根本得不到白色沉淀,因为亚硫酸不可能制取盐酸;C项只能说明Fe2+具有还原性,因为KMnO4具有强氧化性,常做氧化剂。D项,沉淀呈黄色,说明沉淀是AgI,也就意味着AgCl的Ksp比AgI的大。
 [考点分析]
[考点分析]
 ①重要试验的操作过程、实验现象、结论和解释应牢记;
①重要试验的操作过程、实验现象、结论和解释应牢记;
 ②Ksp的运用。
②Ksp的运用。
 21
21 .(09年江苏化学·13)下列溶液中微粒的物质的量浓度关系正确的是
.(09年江苏化学·13)下列溶液中微粒的物质的量浓度关系正确的是
 A.室温下,向0.01mol·L-1NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
A.室温下,向0.01mol·L-1NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
 B.0.1mol·L-1NaHCO3溶液:c(Na+)>c(OH-)>c(HCO3-)>c(H+)
B.0.1mol·L-1NaHCO3溶液:c(Na+)>c(OH-)>c(HCO3-)>c(H+)
 C.Na2CO3溶液:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3)
C.Na2CO3溶液:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3)
 D.25℃时,pH=4.75、浓度均为0.1mol·L-1的CH3COOH、CH3COONa混合溶液: c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+)
D.25℃时,pH=4.75、浓度均为0.1mol·L-1的CH3COOH、CH3COONa混合溶液: c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+)
 答案:AC
答案:AC
 解析:B项,NaHCO3溶液中,OH-是由HCO3- 水解和水的电离所出成的,但是这些都是微弱的。HCO3- 的浓度永大于OH-浓度,故错;D项,由电荷守恒有:c(CH3COO-)+c(OH-)=c(H+)+c(Na+) ,由物料守恒可得:2c(Na+)= c(CH3COO-)+ c(CH3COOH),将两式中的c(Na+) 消去,可得c(CH3COO-)+2c(OH-)=2c(H+)+ c(CH3COOH)。所以c(CH3COO-)+c(OH-)-c(H+)-c(CH3COOH)= c(H+)-c(OH-),因为pH=4.75,故c(H+)-c(OH-)>0,所以D项不等式应为”>”
,故错。
解析:B项,NaHCO3溶液中,OH-是由HCO3- 水解和水的电离所出成的,但是这些都是微弱的。HCO3- 的浓度永大于OH-浓度,故错;D项,由电荷守恒有:c(CH3COO-)+c(OH-)=c(H+)+c(Na+) ,由物料守恒可得:2c(Na+)= c(CH3COO-)+ c(CH3COOH),将两式中的c(Na+) 消去,可得c(CH3COO-)+2c(OH-)=2c(H+)+ c(CH3COOH)。所以c(CH3COO-)+c(OH-)-c(H+)-c(CH3COOH)= c(H+)-c(OH-),因为pH=4.75,故c(H+)-c(OH-)>0,所以D项不等式应为”>”
,故错。
 [考点分析]
[考点分析]
 ①混合溶液中离子浓度的关系,电荷守恒。
①混合溶液中离子浓度的关系,电荷守恒。
 ②等pH的溶液中物质的量浓度的大小关系
②等pH的溶液中物质的量浓度的大小关系
 ③电离和水解的相互关系
③电离和水解的相互关系
 ④酸式盐溶液中离子的浓度大小关系
④酸式盐溶液中离子的浓度大小关系
17.(09年广东理基·27)工业废水中常含有不同类型的污染物,可采用不同的方法处理。以下处理措施和方法
|
选项 |
污染物 |
处理措施 |
方法类别 |
|
A |
废酸 |
加生石灰中和 |
物理法 |
|
B |
Cu2+等重金属离子 |
加硫酸盐沉降 |
化学法 |
|
C |
含苯废水 |
用活性炭吸附 |
物理法 |
|
D |
含纯碱的废水 |
加石灰水反应 |
化学法 |
答案:D
解析:A选项废酸中加生石灰中和是化学处理法,错误。B选项中加硫酸盐不能使Cu2+形成沉淀,错误。C选项中用活性炭不能吸附苯,错误。D选项中加石灰水后纯碱会形成CaCO3沉淀而除去,属于化学处理法,正确。
16.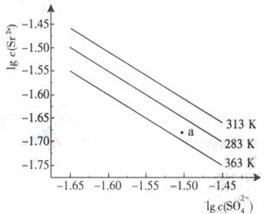 (09年广东化学·18)硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如下,下列说法正确的是
(09年广东化学·18)硫酸锶(SrSO4)在水中的沉淀溶解平衡曲线如下,下列说法正确的是
A.温度一定时,Ksp(SrSO4)随 的增大而减小
的增大而减小
B.三个不同温度中,313K时Ksp(SrSO4)最大
C.283K时,图中a点对应的溶液是不饱和溶液
D.283K下的SrSO4饱和溶液升温到263K后变为不饱和溶液
答案:BC
解析:平衡常数只与温度有关,与物质的浓度无关,A错误;温度一定时Ksp=[Sr2+][SO42-],由图可知,313K时,相同SO42-浓度下,Sr2+的浓度最大,所以平衡常数最大,B正确;283K时,Sr2+的浓度比平衡时要小,Qc小于Ksp(283K),对应为不饱和溶液,C正确;283K下的饱和溶液,突然升温至363K,Ksp减少,析出沉淀,仍然为饱和溶液,D错误。
15.(09年广东化学·16)磷钨酸H3PW12O40等杂多酸可代替浓硫酸用于乙酸乙酯的制备。下列说法不正确的是
A.H3PW12O40在该酯化反应中其催化作用
B.杂多酸盐Na2HPW12O40与Na3PW12O40都是强电解质
C.H3PW12O40、KH2PW12O40与Na3PW12O40中都有相同的原子团
D.硅钨酸H4 SiW12O40也是一种杂多酸,其中W的化合价为+8
答案:CD
解析:因浓硫酸在制备乙酸乙酯中起到催化剂和吸水剂的作用,又杂多酸可代替浓硫酸制备乙酸乙酯,所以杂多酸同样起到催化作用,A正确;因大多数盐属于强电解质,所以杂多酸盐为强电解质,所以杂多酸盐也为强电解质,B正确;磷钨酸又可将其视作为H3PO4与WO3的混合酸,因磷酸为三元中强酸,磷酸盐中含有的酸根不同即原子团不同,C错误;从化合价和代数为0可知W的价态为+6价,D错误。
14.(09年广东化学·9)下列浓度关系正确的是
A.氯水中:c(Cl2)=2c(ClO-)+c(Cl-)+C(HCl)}
B.氯水中:c(Cl-)>c(H+)>c(OH-)>c(ClO-)
C.等体积等浓度的氢氧化钠与醋酸混合:c(Na+)=c(CH3COO-)
D.Na2CO3溶液中:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)
答案:D
解析:氯气在水中与水反应是可逆反应,物料守恒不成立,A错误;Cl2+H2O=HCl+HClO,HCl中电离的H+与Cl-浓度相等,再加上HClO会电离出H+,所以H+浓度一定大于Cl-浓度,B错误;等体积等浓度的氢氧化钠与醋酸混合恰好完全反应生成醋酸钠,因CH3COO-水解,所以Na+浓度大于CH3COO-的浓度,C错误。
13. (09年福建理综·10)在一定条件下,Na2CO3溶液存在水解平衡:CO32-+H2O
(09年福建理综·10)在一定条件下,Na2CO3溶液存在水解平衡:CO32-+H2O HCO3-+OH-。下列说法正确的是
HCO3-+OH-。下列说法正确的是
 A.稀释溶液,水解平衡常数增大 B.通入CO2,平衡朝正反应方向移动
A.稀释溶液,水解平衡常数增大 B.通入CO2,平衡朝正反应方向移动
 C.升高温度,
C.升高温度,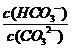 减小 D.加入NaOH固体,溶液pH减小
减小 D.加入NaOH固体,溶液pH减小
答案:B
解析:平衡常数仅与温度有关,故稀释时是不变的,A项错;CO2通入水中,相当于生成H2CO3,可以与OH-反应,而促进平衡正向移动,B项正确;升温,促进水解,平衡正向移动,故表达式的结果是增大的,C项错;D项,加入NaOH,碱性肯定增强,pH增大,故错。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com