
4.下列叙述中可说明酸甲比酸乙的酸性强的是( )
A.溶液导电性酸甲大于酸乙
B.钠盐溶液的碱性在相同物质的量浓度时,酸甲的钠盐比酸乙的钠盐弱
C.酸甲中非金属元素比酸乙中非金属元素化合价高
D.酸甲能与酸乙的铵盐反应有酸乙生成
3.浓度和体积都相同的盐酸和醋酸,在相同条件下分别与足量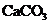 固体(颗粒大小均相同)反应,下列说法中正确的是( )
固体(颗粒大小均相同)反应,下列说法中正确的是( )
A.盐酸的反应速率大于醋酸的反应速率
B.盐酸的反应速率等于醋酸的反应速率
C.盐酸产生的二氧化碳比醋酸更多
D.盐酸和醋酸产生的二氧化碳一样多
2. 是比碳酸还要弱的酸,为了提高氯水中
是比碳酸还要弱的酸,为了提高氯水中 的浓度,可加入( )
的浓度,可加入( )
A. B.
B.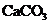 C.
C.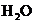 D.
D.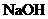
1.足量镁和一定量的盐酸反应,为减慢反应速率,但又不影响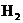 的总量,可向盐酸中加入下列物质中的( )
的总量,可向盐酸中加入下列物质中的( )
A.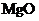 B.
B.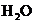 C.
C. D.
D.
3.与化学平衡比较
(1)电离平衡是动态平衡:即弱电解质分子电离成离子过程和离子结合成弱电解质分子过程仍在进行,只是其速率相等。
(2)此平衡也是有条件的平衡:当条件改变,平衡被破坏,在新的条件下建立新的平衡,即平衡发生移动。
(3)影响电离平衡的因素
A.内因的主导因素。
B.外国有:
①温度:电离过程是一个吸热过程,所以,升高温度,平衡向电离方向移动。
②浓度:
问题讨论:在

 的平衡体系中:
的平衡体系中:
①加入 :
:
②加入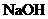 :
:
③加入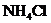 :各离子分子浓度如何变化:
:各离子分子浓度如何变化: 、
、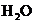 、
、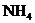 、
、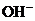 溶液
溶液 如何变化?(“变高”,“变低”,“不变”)
如何变化?(“变高”,“变低”,“不变”)
(4)电离平衡常数
(ⅱ)一元弱酸:




(3)一元弱碱




①电离平衡常数化是温度函数,温度不变K不变。
② 值越大,该弱电解质较易电离,其对应的弱酸弱碱较强;
值越大,该弱电解质较易电离,其对应的弱酸弱碱较强; 值越小,该弱电解质越难电离,其对应的弱酸弱碱越弱;即
值越小,该弱电解质越难电离,其对应的弱酸弱碱越弱;即 值大小可判断弱电解质相对强弱。
值大小可判断弱电解质相对强弱。
③多元弱酸是分步电离的,一级电离程度较大,产生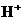 ,对二级、三级电离产生抑制作用。如:
,对二级、三级电离产生抑制作用。如:










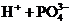
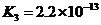
随堂练习
2.当
则弱电解质电离处于平衡状态,叫“电离平衡”,此时溶液中的电解质分子数、离子数保持恒定,各自浓度保持恒定。
1.弱电解质电离过程(用图像分析建立)

3. 了解影响电离平衡的因素
重点、难点: 外界条件对电离平衡的影响,电离平衡常数。
课时安排:共2课时(此为第二课时)。
教学方法:类比、推理等教学方法结合使用。
教学准备:习题及知识的总结、扩展可制作PPT或使用纸板。
教学过程:
今天学习的内容是:“电离平衡”知识。
2. 了解电离平衡常数的概念。
1. 掌握弱电解质的电离平衡。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com