
19.(7分)已知周期表中,元素Q、R、W、Y与元素X相邻。Y的最高化合价氧化物的水化物是强酸,W的氯化物分子呈正四面体结构,W与Q形成高温陶瓷。这5个元素的氢化物分子中:①立体结构类型相同的氢化物的沸点从高到低排列次序是(填化学式) ,其原因是 ;
②(3分)电子总数相同的氢化物的化学式和立体结构分别是
。
18. (4分) 1919年,Langmuir提出等电子原理:原子数相同、电子总数相同的微粒,互称为等电子体。等电子体的结构相似、物理性质相近。
(1)根据上述原理,仅由第2周期元素组成的共价分子中,互为等电子体的是: 和 。(任意写出一组即可)
(2)此后,等电子原理又有所发展。例如,由短周期元素组成的微粒,只要其原子数相同,各原子最外层电子数之和相同,也可互称为等电子体,它们也具有相似的结构特征。在短周期元素组成的物质中,与NO2-互为等电子体的分子有: 。(任意写出一个即可)
17.(8分)已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质。下面给出13种元素的X的数值:
|
元素 |
Al |
B |
Be |
C |
Cl |
F |
Li |
|
X数值 |
1.5 |
2.0 |
1.5 |
2.5 |
2.8 |
4.0 |
1.0 |
|
元素 |
Mg |
Na |
O |
P |
S |
Si |
|
|
X数值 |
1.2 |
0.9 |
3.5 |
2.1 |
2.5 |
1.7 |
|
试结合元素周期律知识完成下列问题:
(1)经验规律:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中的化学键类型是______。
(2)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系_________________________ ;
简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系__________________________________________ 。
(3)某化合物分子中含有S-N键,该共用电子对偏向于________原子(填元素符号)。
16.(8分)1994年度诺贝尔化学奖授予为研究臭氧作出特殊贡献的化学家。O3能吸收有害紫外线,保护人类赖以生存的空间。O3分子的结构如图5,呈V型,键角116.5℃。三个原子以一个O原子为中心,与另外两个O原子分别构成一个非极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个特殊的化学键即三个O原子均等地享有这4个电子(如右图所示)。请回答:
 |
|
图 O3的分子结构 |
(1)臭氧与氧气的关系是___________。
(2)选出下列分子与O3分子的结构最相似的的是( )
A. H2O B. CO2 C. SO2 D. BeCl2
(3)分子中某原子没有跟其他原子共用的价电子对叫孤对电子,那么O3分子有___________对孤对电子。
(4)O3具有强氧化性,它能氧化PbS为PbSO4而O2不能,试配平:
_________PbS +________O3 -- ________PbSO4 + ________O2
15.下列叙述中正确的是( )
A.NH3、CO、CO2都是极性分子
B.CH4、CCl4都是含有极性键的非极性分子
C.HF、HCl、HBr、Hl的稳定性依次增强
D.CS2、H2O、C2H2都是直线型分子
太 原 五 中
2010-2011学年度第一学期月考(8月)
高三化学(理)答卷纸
命题人:尹延刚 2010/8/20
成绩
请将单项选择题答案填入下表(每题3分,共45分)
第二卷(非选择题部分,共55分)
14.下列是几种原子的基态电子排布,电负性最大的原子是( )
A. 1s22s22p4 B. 1s22s22p63s23p3
C. 1s22s22p63s23p2 C. 1s22s22p63s23p64s2
13.既有离子键又有共价键和配位键的化合物是( )
A.NH4NO3 B.NaOH C.H2SO4 D.H2O
12.向盛有硫酸铜水溶液的试管里加入氨水,先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液。下列对此现象说法正确的是( )
A.反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变。
B.沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4] 2+。
C.硫酸铜水溶液里加入氨水生成的沉淀是氢氧化铜,继续加氨水沉淀又溶解,说明氢氧化铜是两性氢氧化物。
D.在[Cu(NH3)4] 2+离子中,Cu2+给出孤对电子,NH3提供空轨道。
11.三种元素的微粒 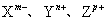 都有相同的电子层结构,已知
都有相同的电子层结构,已知 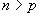 ,则它们核内质子数(依次用
,则它们核内质子数(依次用 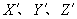 表示)的关系为 (
)
表示)的关系为 (
)
A.
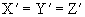 B.
B. 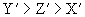
C.
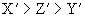 D.
D. 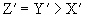
10.据权威刊物报道,1996年科学家在宇宙中发现H3分子。甲、乙、丙、丁四位学生对此报道的认识正确的是( )
A.甲认为上述发现绝对不可能,因为H3分子违背了共价键理论
B.乙认为宇宙中还可能存在另一种氢单质,因为氢元素有三种同位素必然有三种同素异形体
C.丙认为H3分子实质上是H2分子与H+以特殊共价键结合的产物,应写成H3+
D.丁认为如上述发现存在,则证明传统的价键理论有一定的局限性有待继续发展
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com