
45.(5分)隽袆用石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2CO3溶液,他决定利用该废液,测定Na2CO3溶液中溶质的质量分数。他将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如右图所示。
(1)在加入Na2CO3溶液的过程中,开始时没有发现沉淀生成,说明滤液中的溶质有____________________ _;
(2)计算Na2CO3溶液中溶质的质量分数。(计算结果精确到0.1%)
生 物 部 分
44.(4分)酸与碱生成盐和水的反应叫中和反应。实验中学化学小组的同学就中和反应是否放热和中和反应放热与哪因素有关作了如下探究:
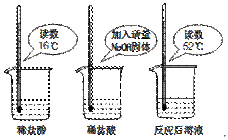 (1)为证明中和反应是放热反应,某小组进行了
(1)为证明中和反应是放热反应,某小组进行了
如图所示的实验操作:根据下图实验,甲同学
认为:NaOH与稀盐酸发生的中和反应是放热
反应。乙同学认为:甲同学得出这个结论的依
据不科学,理由是___ ___;
丙同学认为:通过多个实验才能得出一个普遍
的结论。请你再举出一个中和反应的实例,其化学方程式为___ ___。
(2)为探究影响中和反应放出热量多少的因素,他们又进行了如下实验:在编号为A、B、C、D、E的五只烧杯中各装入36.5g 溶质质量分数为5%、10%、15%、20%、25%的盐酸,再向上述五只烧杯中分别加入40g20% 的氢氧化钠溶液,最后测量其温度,数据记录如下:
|
烧杯编号 |
A |
B |
C |
D |
E |
|
盐酸的溶质质量分数 |
5% |
10% |
15% |
20% |
25% |
|
反应后溶液温度(℃) |
24℃ |
34℃ |
46℃ |
54℃ |
54℃ |
[实验结论]影响中和反应放出热量多少的因素是_______________ __________。
[交流反思]反应后,烧杯内溶液pH最小的是__ __(填烧杯编号)。
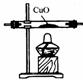
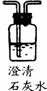
43.(7分)如下图,实验室提供下列盛有药品的仪器,由甲乙两个实验小组各自证明某一混合气体中含有二氧化碳、一氧化碳和水蒸气(假设气体通过装置时均被完全吸收或反应)。
 |
 |
 |
 |
|
A |
B |
C |
D |
(1)甲组:分别证明混合气体中含有某一种气体。
① 证明其中含有水蒸气,选用 ,出现的实验现象是 。
② 证明其中含有二氧化碳,选用 ,反应的化学方程式 。
③ 选择必要的仪器(每种只用一次)证明其中含有一氧化碳,按气体通过的先后顺序
依次是 (用A、B、C、D表示)。
(2)乙组:用上述仪器(可以重复使用)组装一套装置,通过一次实验证明混合气体中含有二氧化碳、一氧化碳和水蒸气。
① 按气体通过的先后顺序,连接的仪器依次是 (用A、B、C、D表示)。
② 从环境保护角度出发,该实验中最后导出的尾气的处理方法是________ ____ 。
42.(6分)某化工厂为了综合利用生产过程中的副产品CaSO4,与相邻的化肥厂联合设计了以下制备(NH4)2 SO4的工艺流程。(提示:在下图流程中,沉淀池里发生的反应有水参加)
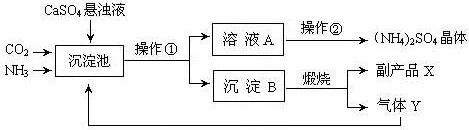
(1)沉淀B高温煅烧反应的化学方程式 ,
反应的基本类型: ,该工艺中可循环使用的物质为 (填化学式)。
(2)操作①如果在实验室中进行时,用到的玻璃仪器除玻璃棒、烧杯外,还需 。操作②的过程是加热浓缩、冷却、结晶,获得(NH4)2 SO4晶体属于 (填:“氮肥”、“磷肥”或“钾肥”)。
(3)从绿色化学和资源综合利用的角度说明上述流程的主要优点是 。
41.(5分)车用乙醇汽油是将乙醇(C2H5OH)与汽油(以C8H18表示)按一定比例混合而成的一种汽车燃料。
(1)乙醇分子中,组成元素的原子个数比C:H:O为 。
(2)在密闭容器中,将少量乙醇置于一定量氧气中燃烧,生成二氧化碳、水蒸气和一种未知物质W。现测得反应前后各物质的质量如下:
|
物质 |
乙醇 |
氧气 |
二氧化碳 |
水蒸气 |
W |
|
反应前质量/g |
23 |
40 |
0 |
0 |
0 |
|
反应后质量/g |
0 |
0 |
22 |
27 |
x |
①根据质量守恒定律,得出表中x的值为 ;
②根据表中数据,可确定未知物W中各组成元素的质量比为 ;
(3)通常可燃物中碳元素质量分数越高,燃烧产生 W越多。则相同条件下,乙醇和汽油分别燃烧时,产生W较多的是 ;为了使乙醇汽油燃烧过程中少产生 W,应采取的措施是 (任写一种)。
40.(5分)按要求回答下列问题:
(1)用适当的数字和符号填空:
①二个钠离子 ;②三个氧分子 ;③硝酸铵中显-3价的氮元素 。
(2)化学源于生活,“柴、米、油、盐”中蕴含着许多化学知识。请你用化学式填空
①在新农村建设中,许多家庭兴建沼气池。沼气的主要成分是 ;
②大米的主要成分是淀粉。淀粉的化学式可写为 。
39.(4分)根据下列要求写出有关反应的化学方程式:
(1)实验室制取氢气最好的原理 ;
(2)“绿色能源”酒精的燃烧 ;
(3)有黑色固体生成的分解反应 ;
(4)有氯化钠参加的复分解反应 。
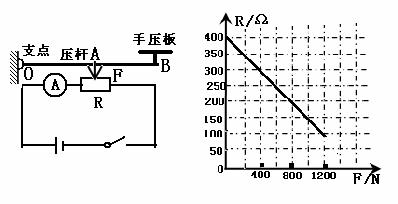
38.同学们研制了一种测量手压力大小的电子称,其测力部分的原理如图甲所示,它主要由手压板、杠杆OAB,压力传感器R(电阻值会随所受压力的大小发生变化的变阻器)和显示压力大小的仪器A(实质是电流表)构成,其中OA∶OB=1∶2,且已知压力传感器R的电阻与它所受的压力F的关系如图乙所示。接通电源后,压力传感器两端的电压横为4.8V。手压板和杠杆的质量不计。求:
(1)若某同学对手压板的压力为400N时,压力传感器上受的压力多大?此时,电流表的示数多大?
(2)若压力传感器R表面能承受的最大压强为4×106pa,压力杆与压力传感器之间的接触面积是3cm2,则压力传感器R表面能承受最大压力为多大?
 (3)该电子称的测量范围。
(3)该电子称的测量范围。
化 学 部 分
37.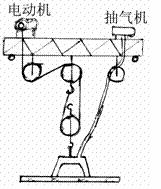 普通玻璃是由炽热的玻璃液体冷却后形成的,我们教室的窗户玻璃又是由大块的平板玻璃切割下来的。大型平板玻璃生产工艺是著名的玻璃生产商皮尔金顿受到油滴在水面均匀分布开来的启示,组织科研人员攻关而发明的“浮法平板玻璃”工艺流程。(g=10N/kg)
普通玻璃是由炽热的玻璃液体冷却后形成的,我们教室的窗户玻璃又是由大块的平板玻璃切割下来的。大型平板玻璃生产工艺是著名的玻璃生产商皮尔金顿受到油滴在水面均匀分布开来的启示,组织科研人员攻关而发明的“浮法平板玻璃”工艺流程。(g=10N/kg)
(1)该工艺关键是找到了能够浮起玻璃的一种溶液,你认为这种液体应该具备怎样的物理特性(说出一点)。
(2)若一块冷凝后的玻璃板长2m,宽1.5m,厚5mm,密度为2.5×103kg/m3,这块玻璃的质量有多少?
(3)吊运玻璃一般用真空吸盘吊车,若当时大气压为1个标准大气压,则吸盘的面积至少是多少?
(4)若电动机对绳的拉力为250N,玻璃上升的速度是20cm/s求吊车提升玻璃时的机械效率和功率。
36.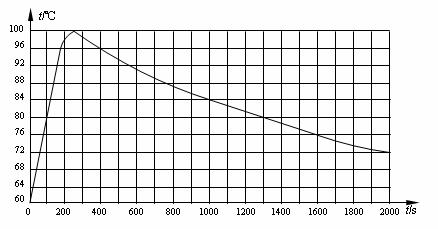 如图所示,是用温度传感
如图所示,是用温度传感
器测量得到的家庭用电
开水壶在加热和冷却过
程中温度随时间变化的
图线,已知壶内盛有1kg
水。请根据图线并通过计
算回答下列问题
(1)在实际加热过程中,
电开水壶消耗的电功率
P1 与水每秒净吸收的热
量P2(即水的实际吸热
功 率)相比较,P1 P2(填“大于”、“等于”或“小于”),主要是因为 。
(2)在从t1=1000s至t2 =1300s的冷却过程中,求水散失的热量和平均散热功率P3(即每秒 散失的热量)。
(3)如果此时(即水温在80℃-84℃之间)需要给电开水壶加装自动保温加热器,补偿此时的热量散失,则自动保温器的功率和电阻是多少?(设:家庭电路的电压不变)
灵敏程度的影响,请你帮他们设计一个实验方案.
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com