
2、乙烯的工业制法和物理性质 6个原子在同一平面上
工业制法: 石油化工
石油炼制:石油分馏、催化裂化、裂解
催化裂化:相对分子量较小、沸点教小的烃
 裂解:乙烯、丙烯老等气态短链烃
裂解:乙烯、丙烯老等气态短链烃
石油的裂解已成为生产乙烯的主要方法
1、乙烯分子式:C2H4 结构简式:CH2==CH2 结构式
2、化学性质
一般情况下,性质稳定,跟强酸、强碱或强氧化剂不反应
(1)、氧化性
CH4+2O2 CO2+2H2O;△H<0
CO2+2H2O;△H<0
CH4不能使酸性高锰酸甲褪色
(2)、取代反应
取代反应:有机化合物分子的某种原子(或原子团)被另一种原子(原子团)所取代的反应
CH4+Cl2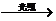 CH3Cl+HCl CH3Cl+Cl2
CH3Cl+HCl CH3Cl+Cl2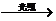 CH2Cl2+ HCl
CH2Cl2+ HCl
CH2Cl2+Cl2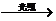 CHCl3+ HCl CHCl3+Cl2
CHCl3+ HCl CHCl3+Cl2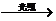 CCl4+ HCl
CCl4+ HCl
(3)主要用途:化工原料、化工产品、天然气、沼气应用
1、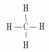 甲烷:分子式:CH4 结构式:
甲烷:分子式:CH4 结构式:
电子式 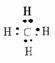 正四面体
正四面体
天然气三存在:沼气、坑气、天然气
化石燃料:煤、石油、天然气
天然气的主要成分:CH4
石油的组成元素主要是碳和氢,同时还含有S、O、N等。主要成分各种液态的碳氢化合物,还溶有气态和固态的碳氢化合物
煤是有机化合物和无机化合物所组成的复杂的混合物。煤的含量是C其次H、O
电能转化为化学能的装置
例如电解CuCl2、电解水、电解食盐水、电解精炼铜
专题七 有机化合物的获得与应用
第一单元化石燃料与有机化合物
 定义:将化学能转化为电能的装置
定义:将化学能转化为电能的装置
原理:氧化还原反应
教活泼的金属发生氧化反应,
电子从较活泼的金属(负极)流向较不活泼的金属或非金属导体(正极)
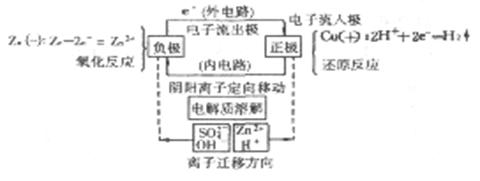
电极反应
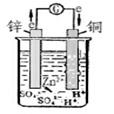
锌--铜原电池
负极: Zn-2e==Zn2+
正极: 2H++2e=H2↑
总反应:Zn+2H+==Zn2++H2↑
氢氧燃烧电池优点:(1)能量转换效率高(2)洁净、无污染、噪音低、隐蔽性强(3)模块结构。适应不同功率要求灵活机动(4)比功率大,比能量高,对负载的适应性能好(5)可实现热、电、纯水、联产
2、吸热反应:化学上吸收热量的化学反应 生成物的总能量>反应物的总能量
断开化学键所吸收的能量大于形成化学键所放出的能量
当△H为“-”或者△H<0时,为放热反应 当△H为“+”或者△H>0时, 为吸热反应
常见的放热反应:燃烧、酸碱中和反应、金属与酸的反应、氧化钙与水
常见的放热反应:通常需要高温或者加热的反应(C+CO2-)、氢氧化钙与氯化铵晶体反应
燃烧放出的热量的大小等于断裂开反应物分子中化学键吸收的总能量与形成生成物分子中化学键放出的总能量之差。
第三单元 化学能与电能的转化
1、放热反应:化学上有热量放出的化学反应 反应物的总能量>生成物的总能量
断开化学键所吸收的能量小于形成化学键所放出的能量
2、 化学平衡状态:在一定条件下的可逆反应里,当正反应速率等于逆反应速率,反应物和生成物的浓度不在变化的状态
特征:
动:动态平衡 V正≠0, V逆≠0
等:V正=V逆
定:各组分的浓度保持不变(不是相等,也不能某种比例)
变;条件改变,平衡发生移动
第二单元 化学反应中的能量
化学反应中的热量变化
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com