
2mol 96g
x mol (33.2g-28.4g)=4.9g
解得:x = 0.1mol 即12.25g
由关系式 MnO2 - Cl2↑可知混合物中MnO2的质量为0.1mol×87g·mol-1=8.7g,故33.2g混合物中KClO3的质量为33.2g-8.7g = 24.5g ,故KClO3的分解率为
(2)由KCl - AgCl可得生成的AgNO3的物质的量为0.1mol,即14.35g 答:略。
22.(1)26.2g (2)1792mL 提示:(1)m(S)=0.2mol·L-1 ×0.1L×32g·mol-1 + 0.8mol×32g·mol-1 = 26.2g
(2)n(Na2SO3) = 12.6g ÷126g·mol-1 =0.1mol ,n(SO2)=0.1mol-0.2mol·L-1 ×0.1L=0.08mol ,V(SO2) = 0.08mol ×22.4L·mol-1= 1.792L即1792mL
22.将12.6g无水亚硫酸钠固体加入100mL 8mol·L-1的硫酸中以制取SO2气体,反应完全后,若溶液中含+4价硫元素的物质的总浓度为0.2mol·L-1,假定溶液体积不变,忽略容器及导管中的气体体积,求:
(1)溶液中硫元素的质量。
(2)收集到SO2气体多少毫升(标准状况下)?
第四章 非金属及其化合物检测题(一)
21.(6分)33.2g KClO3和MnO2的混合物,加热一段时间后,质量变为28.4g。冷却后加水搅拌,溶解完全后过滤,在滤液中加硝酸银。滤纸上的不溶物与足量的浓盐酸反应,可生成0.1molCl2,求:
(1)KClO3的分解百分率。
(2)可生成AgCl沉淀的质量。
20.(8分)一某学生取纯净的50.0g Na2SO3·7 H2O,经600℃以上的强热至恒重,分析及计算结果表明,恒重后的样品质量相当于无水亚硫酸钠的计算值,而且各元素的组成也符合计算值,但将它溶于水,却发现溶液的碱性大大高于期望值。经过仔细思考,这位同学解释了这种反常现象,并设计了一组实验,验证了自己的解释是正确的。
(1)他对反常现象的解释是(请用化学方程式表达) 。
(2)他设计的验证实验是(请用化学方程式表达) 。
19.(6分)有一瓶澄清的溶液,其中可能含有NH4+、K+、Na+、Mg2+、Ba2+、Fe3+、SO42―、CO32―、Cl―和I―。你取该溶液进行了以下实验:
(1)用pH试纸检验,表明溶液呈强酸性;
(2)取部分溶液,加入CCl4及数滴氯水,经振荡后CCl4层呈紫红色;
(3)另取部分溶液,加入稀NaOH 溶液使其变为碱性,溶液中无沉淀生成;
(4)取部分上述碱性溶液,加Na2CO3溶液有白色沉淀生成;
(5)将(3)得到的碱性溶液加热,有气体放出,该气体能使润湿的红色石蕊试纸变蓝;
根据上述实验事实,你可知道该溶液中肯定含有的离子是① ;肯定不存在的离子是② ;还不能确定是否存在的离子是③ 。
18.(13分)(1)在如图4-15所示的装置中,烧瓶中充满干燥气体A,将滴管中的液体B挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹,尖嘴管有液体呈喷泉状喷出,最终几乎充满烧瓶,下列情况满足题意的是 (填代号)。
①NH3-H2O ②HCl-H2O ③CO2-4mol·L-1 NaOH溶液 ④Cl2-饱NaCl溶液
⑤HCl-AgNO3溶液 ⑥Cl2-碘化钾淀粉溶液 ⑦Cl2-溴化钠溶液
⑧NH3-汽油 ⑨NO2-H2O ⑩ NH3-酚酞溶液

(2)500mL烧瓶中充满某种气体(274K、101325Pa)X,烧瓶中盛满水,L =30cm,h =60cm,气体溶解度在此状况下为1:40。通过计算回答:如果能看到喷泉,开始时胶头滴管应先向烧瓶内注入水的体积是 mL。
(3)利用NO2(标准状况下)气体和水做喷泉实验,求烧瓶内HNO3溶质的物质的量浓度。
(4)某学生利用NH3和水做喷泉实验,(NH3为该学生制备和收集),结果未能形成喷泉。请你替他分析实验不成功的可能原因。
(5)①在图4-16的锥形瓶中,分别加入足量的下列物质,反应可能产生喷泉的是 ( )
A.CaCO3和稀H2SO4 B.NH4HCO3和稀盐酸
C.Al和浓HNO3 D.NaHCO3与NaOH溶液
②锥形瓶中加入酒精,水槽中加入冷水,再加入足量下列物质,结果也产生喷泉的是 ( )
A.浓H2SO4 B.NaCl C.NH4NO3 D.CuSO4
③城市中常见的人造喷泉及火山爆发的原理与上述 (填图4-15或图4-16)装置的原理是相同的。
(6)如果只提供如图4-17的装置,请说明引发喷泉的方法。
17.(10分)(1)在浓硝酸中放入铜片。
①开始反应的化学方程式为 。
②若铜有剩余,则反应将要结束时的反应的离子方程式是 。
③待反应停止后,再加入少量的25%的稀硫酸,这时铜片上又有气泡产生,其原因是 。
(2)在100mL混合酸中,c(HNO3) = 0.4mol·L-1 ,c(H2SO4) = 0.2mol·L-1,向其中加入2.56g铜粉,微热,待充分反应后,溶液中Cu2+的物质的量浓度为 。
(3)14g铜、银合金与一定量某浓度的硝酸溶液反应,待放出的气体与1.12L(标准状况下)氧气混合通入水中,恰好全部被水吸收,则合金中铜的质量是 。
16.(10分)(1)硫酸在下列用途或反应中各表现的性质是 (用字母填在横线上)
A.难挥发性 B.强酸性 C.吸水性 D.脱水性 E.强氧化性 F.催化作用
①浓硫酸可用作气体干燥剂 ;
②往晶体硫酸铜中加浓硫酸,晶体变白 ;
③实验室制硝酸 ;
④实验室制二氧化硫 ;
⑤浓硫酸与铜反应 ;
⑥运用铁制槽车和铝制槽车运输浓硫酸 ;
⑦生产过磷酸钙化肥 ;
⑧浓硫酸使润湿蓝色石蕊试纸先变红后又变黑 。
(2)运用硫酸的性质,设计实验方案鉴别两瓶等体积的硫酸,哪瓶是浓硫酸,哪瓶是稀硫酸? 。
(3)用过量的锌与浓硫酸反应时,可能产生的气体有 ,理由是 。
15.某单质能与浓硝酸反应,若每有0.25mol单质反应就消耗1mol HNO3 参加反应的单质与硝酸的物质的量之比为1:4,则该单质元素被氧化后的化合价可能是 ( )
A.+1 B.+2 C.+3 D.+4
14.如图4-14所示,向一定的铁粉中加入一定体积12mol·L-1的HNO3,加热充分反应后,下列微粒在体系中一定大量存在的是 ( )
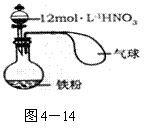 ①NO3- ② Fe3+ ③ H+ ④ NO ⑤ NO2
①NO3- ② Fe3+ ③ H+ ④ NO ⑤ NO2
A.① B.①⑤ C.②④⑤ D.①②③⑤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com