
9.(2010ЁЄЬЦЩНФЃФт)ЯТСаМИзщЮяжЪжаЃЌПЩгУЯрЭЌЕФЗНЗЈФмГ§ШЅЛьгаЕФдгжЪ(РЈКХФкЮЊЩйСПдгжЪ)ЕФЪЧ(ЁЁ )
ЁЁЁЁ AЃЎЕэЗлШмвК(NaCl)ЁЂввЫсШмвК(NaCl)
ЁЁЁЁ BЃЎFe(OH)3НКЬх(KCl)ЁЂЕэЗлШмвК(KI)
ЁЁЁЁ CЃЎNa2CO3ЙЬЬх(NaHCO3)ЁЂNaHCO3ЙЬЬх(Na2CO3)
DЃЎЬњЗл(СђЗл)ЁЂЕт(ЪГбЮ)
[НтЮі]бЁBЁЃГ§ШЅЕэЗлШмвКжаЕФNaClПЩвдгУЩјЮіЗЈЃЌЕЋЪЧГ§ШЅввЫсШмвКжаЕФNaClВЛПЩгУвдЩјЮіЗЈЃЌAбЁЯюДэЮѓЃЛFe(OH)3НКЬхЁЂЕэЗлШмвКЖМЪєгкНКЬхЃЌГ§ШЅРызгЛЏКЯЮяПЩвдгУЩјЮіЕФЗНЗЈЃЌBбЁЯюе§ШЗЃЛCбЁЯюжаЧАепПЩгУМгШШЗНЗЈЃЌКѓепМгШыЬМЫсЧтБЕЃЛDбЁЯюжаЬњЗлжаЕФСђЗлПЩгУЖўСђЛЏЬМГ§ШЅЖјЕтжаЕФЪГбЮПЩгУЩ§ЛЊЗНЗЈГ§ШЅЁЃ
8.(2010ЁЄЗ№ЩНФЃФт)ЯТСаЪЕбщЩшМЦКЭНсТлЯрЗћЕФЪЧ(ЁЁ )
AЃЎНЋЕтЫЎЕЙШыЗжвКТЉЖЗЃЌМгЪЪСПввДМЃЌеёЕДКѓОВжУЃЌПЩНЋЕтнЭШЁЕНввДМжа
BЃЎФГЦјЬхФмЪЙЪЊШѓЕФКьЩЋЪЏШяЪджНБфРЖЃЌИУЦјЬхЫЎШмвКвЛЖЈЯдМюад
CЃЎФГЮоЩЋШмвКжаМгBa(NO3)2ШмвКЃЌдйМгШыЯЁбЮЫсЃЌГСЕэВЛШмНтЃЌдђдШмвКжавЛЖЈгаSO42-
DЃЎдкКЌFeCl2дгжЪЕФFeCl3ШмвКжаЭЈзуСПCl2КѓЃЌГфЗжМгШШЃЌГ§ШЅЙ§СПЕФCl2,МДПЩЕУЕННЯДПОЛЕФFeCl3ШмвК
[НтЮі]бЁBЁЃнЭШЁМСВЛФмгыЫЎЛЅШмЃЌЖјОЦОЋгыЫЎЛЅШмЃЌAбЁЯюДэЮѓЃЛЦјЬхФмЪЙЪЊШѓЕФКьЩЋЪЏШяЪджНБфРЖЃЌЫЕУїЦјЬхШмгкЫЎКѓЯдМюадЃЌBбЁЯюе§ШЗЃЛВЛФмХХГ§вјРызгЕФИЩШХЃЌCбЁЯюДэЮѓЃЛГфЗжМгШШКѓЃЌЛсДйНјFe3+ЕФЫЎНтЃЌгаЧтбѕЛЏЬњГСЕэВњЩњЃЌDбЁЯюДэЮѓЁЃ
7.(2010ЁЄЬЈжнФЃФт)ЯТСаВйзїФмДяЕНдЄЦкФПБъЕФЪЧ(ЁЁ )
AЃЎдкфхввЭщжаЕЮМгЯѕЫсвјШмвКЃЌМьбщфхввЭщЗжзгжаКЌгафхдзг
ЁЁBЃЎдкСНжЇЗжБ№ЪЂгаЩйСПБНКЭЫФТШЛЏЬМЕФЪдЙмжаМгЕтЫЎКѓеёЕДЃЌЧјЗжБНКЭЫФТШЛЏЬМ
CЃЎОЦОЋгыЕтЫЎЛьКЯВЂеёЕДЃЌнЭШЁЕтЫЎжаЕФЕтЁЁЁЁ ЁЁЁЁ
DЃЎдкБНжаМгЬњЗлКѓдйМгфхЫЎВЂеёЕДЃЌжЦШЁфхБН
[НтЮі]бЁBЁЃМьбщТБДњЬўжаЕФТБдзгЃЌЯШМгШыЧтбѕЛЏФЦШмвКЃЌМгШШЃЌдйМгШыЯЁЯѕЫсЫсЛЏЃЌзюКѓМгШыЯѕЫсвјШмвКЃЌAбЁЯюДэЮѓЃЛЪЂЗХБНЕФЪдЙмгаЩЋВудкЩЯЗНЃЌЪЂЗХЫФТШЛЏЬМЕФЪдЙмгаЩЋВудкЯТЗНЃЌBбЁЯюе§ШЗЃЛнЭШЁМСВЛФмгыЫЎЛЅШмЃЌЖјОЦОЋгыЫЎЛЅШмЃЌCбЁЯюДэЮѓЃЛжЦШЁфхБНгІИУгУфхЕЅжЪЃЌDбЁЯюДэЮѓЁЃ
6.(2010ЁЄЬьКгФЃФт)ЯТСагаЙиЪЕбщЕФЫЕЗЈДэЮѓЕФЪЧ(ЁЁ )
AЃЎНЋвЛаЁПщЪджНЗХдкБэУцУѓЩЯЃЌгУВЃСЇАєеКШЁЩйСПД§ВтвКЕудкЪджНЩЯЃЌдйгыБъзМБШ
ЩЋПЈЖдее
B.ЯђввЫсввѕЅжаМгШыБЅКЭNa2CO3ШмвКЃЌеёЕДЃЌЗжвКЗжРыГ§ШЅввЫсввѕЅжаЕФЩйСПввЫс
CЃЎеєСѓЪБеєСѓЩеЦПжавКЬхЕФЬхЛ§ВЛФмГЌЙ§ШнЛ§ЕФ2/3ЃЌвКЬхвВВЛФмеєИЩ
DЃЎНЋЙЬЬхМгШыШнСПЦПжаШмНтВЂЯЁЪЭжСПЬЖШЃЌХфжЦГЩвЛЖЈЮяжЪЕФСПХЈЖШЕФШмвК
[НтЮі]бЁDЁЃВЛФмЙЛжБНгНЋЙЬЬхЛђепХЈШмвКдкШнСПЦПжаШмНтЛђепЯЁЪЭЃЌDбЁЯюДэЮѓЁЃ
5.(2010ЁЄЩиЙиФЃФт)ЯТСагаЙиЪЕбщВйзїЕФЫЕЗЈе§ШЗЕФЪЧ(ЁЁ )
AЃЎSO2ЭЈШыЦЗКьШмвККЭИпУЬЫсМиШмвКжаЃЌШмвКОљЭЪЩЋЃЌЫЕУїSO2ОпгаЦЏАзад
BЃЎгУеєСѓЫЎНЋPHЪджНЯШШѓЪЊЃЌПЩгУгкМьбщАБЦј
CЃЎдкГЃЮТЯТЃЌНЋТШЛЏТСШмвКеєЗЂНсОЇЃЌзюКѓФмЕУЕНТШЛЏТСОЇЬх
DЃЎФГЮоЩЋШмвКжаМгBa(NO3)2ШмвКЃЌдйМгШыЯЁбЮЫсЃЌГСЕэВЛШмНтЃЌдђдШмвКжавЛЖЈгаSO42-
[НтЮі]бЁBЁЃSO2ЪЙЦЗКьШмвКЭЪЩЋЃЌЯдЪОЦЏАзадЃЌSO2ЪЙИпУЬЫсМиШмвКЭЪЩЋЃЌЯдЪОЛЙдадЃЌAбЁЯюДэЮѓЃЛгУеєСѓЫЎНЋPHЪджНШѓЪЊКѓЃЌВХПЩвдМьВтАБЦјЃЌАБЦјШмгкЫЎЩњГЩвЛЫЎКЯАБЃЌЕчРыГіЧтбѕИљРызгЃЌЪЙЪджНБфРЖЃЌBбЁЯюе§ШЗЃЛгЩгкТСРызгЫЎНтЃЌеєЗЂЛсДйНјЫЎНтЃЌеєЗЂКѓЕУЕНЕФЪЧЧтбѕЛЏТСЃЌCбЁЯюДэЮѓЃЛВЛФмХХГ§вјРызгЕФИЩШХЃЌDбЁЯюДэЮѓЁЃ
4.(2010ЁЄеиЧьФЃФт)ЯТСаЖдЪЕбщВйзїЛђЖдЪЕбщЪТЪЕЕФУшЪіе§ШЗЕФЪЧ(ЁЁ )
A. гУДЩлсліШлЛЏИїжжФЦЕФЛЏКЯЮя
B. ЁЁЯђАБЫЎжаЕЮМгAl2(SO4)3ШмвККЭЯђAl2(SO4)3ШмвКжаЕЮМгАБЫЎЯжЯѓЯрЭЌ
C. ХфжЦвЛЖЈХЈЖШЕФШмвКЪБЃЌИЉЪгШнСПЦПЕФПЬЯпЃЌЛсЪЙХфжЦЕФХЈЖШЦЋЕЭ
D. ЪЕбщЪвХфжЦТШЛЏбЧЬњШмвКЪБЃЌНЋТШЛЏбЧЬњЯШШмНтдкЯЁбЮЫсжаЃЌШЛКѓгУеєСѓЫЎЯЁЪЭВЂМгШыЩйСПЬњЗл
[НтЮі]бЁBDЁЃВЛФмгУДЩлсліШлЛЏЧтбѕЛЏФЦЁЂЬМЫсФЦЃЌвђДЫAбЁЯюДэЮѓЃЛЧтбѕЛЏТСМШШмгкЧПЫсвВШмгкЧПМюЃЌЕЋЪЧАБЫЎЪєгкШѕМюЃЌвђДЫAl2(SO4)3ШмвККЭАБЫЎЛЅЕЮЯжЯѓЯрЭЌЃЌBбЁЯюе§ШЗЃЛЖЈШнИЉЪгЃЌЕМжТМгЫЎЩйЃЌХЈЖШЦЋИпЃЌCбЁЯюДэЮѓЃЛХфжЦТШЛЏбЧЬњШмвКЪБЃЌМгЯЁбЮЫсЗРжЙFe2+ЫЎНтЃЌМгШыЬњЗлЗРжЙFe2+БЛбѕЛЏЃЌDбЁЯюе§ШЗЁЃ
3.(2010ЁЄРЅУїФЃФт)Г§дгжЪЪБЃЌЮЊСЫБЃжЄдгжЪОЁСПБЛГ§ШЅЃЌМгШыЕФЪдМСБиаыЩдЙ§СПЃЌзюКѓЕФЙ§СПЮяПЩвдЪЙгУЮяРэЛђЛЏбЇЗНЗЈГ§ШЅЁЃЯжвЊГ§ШЅNaClжаЩйСПЕФCaCl2ЁЂZnCl2ЁЂNa2SO4дгжЪЃЌЯТСабЁгУЪдМСМАЦфЪЙгУЫГађе§ШЗЕФЪЧЁЁЁЁ (ЁЁ )
ЁЁЁЁ AЃЎNa2CO3ЁЂBaCl2ЁЂHCl ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁ BЃЎBaCl2ЁЂNa2CO3ЁЂH2SO4
ЁЁЁЁ CЃЎBaCl2ЁЂNa2CO3ЁЂHCl ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
DЃЎBa(NO3)2ЁЂNa2CO3ЁЂHCl
[НтЮі]бЁCЁЃИљОнГ§дгжЪЕФддђЃЌБОЬтМгШыЪдМСЕФЫГађгІЪЧЃКBa2+ЁњCO32ЃЁњHClЃЌМгЩдЙ§СПBaCl2ПЩГ§ШЅNa2SO4ЃЌЩдКѓМгШыЕФNa2CO3дкГ§ШЅCaCl2ЭЌЪБвВГ§ШЅСЫЙ§СПЕФBaCl2ЃЌзюКѓдйгУбЮЫсГ§ШЅЙ§СПЕФNa2CO3ЃЌЙ§СПЕФбЮЫсПЩвРППМгШШЛгЗЂЖјГ§ШЅЁЃ
2.(2010ЁЄФЯПЊжабЇФЃФт)ФГаЃЛЏбЇаЁзщбЇЩњВтЖЈСђЫсЭОЇЬхРяНсОЇЫЎЕФКЌСПЁЃШєЪЕбщВтЕУСђЫсЭОЇЬхжаНсОЇЫЎЕФКЌСПЦЋЕЭЃЌдьГЩДЫНсЙћПЩФмЕФдвђга(ЁЁ )
ЂйМгШШЧАЫљгУЕФлсліЮДЭъШЋИЩдяЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЂкМгШШЪБгаЩйСПЙЬЬхНІГі
ЂлбљЦЗжаКЌгаМгШШвзЛгЗЂЕФдгжЪЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЂмдкПеЦјжаРфШДКѓГЦСП
ЂнМгШШжСбљЦЗКЌгаЕЕЕФРЖЩЋЪБОЭРфШДГЦСП
AЃЎЂкЂмЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎЂлЂнЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁCЃЎЂйЂмЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁ DЃЎЂмЂн
[НтЮі]бЁDЁЃ w(НсОЇЫЎЕФжЪСП)= w1(МгШШЧАЕФжЪСП)-w2(МгШШКѓЕФжЪСП)ЃЌИљОнЙЋЪНПЩвдЧсЫЩХаЖЯГіЂйУЛгаИЩдяЛсЕМжТw1ЦЋДѓЃЌВтЕУНсОЇЫЎКЌСПЦЋИпЃЛЂкЩйСПЙЬЬхНІГіЃЌЕМжТw2ЦЋаЁЃЌВтЕУНсОЇЫЎКЌСПЦЋИпЃЛЂлбљЦЗжаКЌгаМгШШвзЛгЗЂЕФдгжЪЃЌжТw2ЦЋаЁЃЌВтЕУНсОЇЫЎКЌСПЦЋИпЃЛЂмдкПеЦјжаРфШДКѓГЦСПЃЌЕМжТМгШШКѓЕФлсліЮќЫЎЃЌw2ЦЋДѓЃЌВтЕУНсОЇЫЎКЌСПЦЋЕЭЃЛЂнМгШШжСбљЦЗКЌгаЕЕЕФРЖЩЋЪБЃЌУЛгаНЋЫЎЭъШЋеєЗЂЕєЃЌЕМжТw2ЦЋДѓВтЕУНсОЇЫЎКЌСПЦЋЕЭЃЌвђДЫDбЁЯюе§ШЗЁЃ
1.(2010ЁЄФЯПЊжабЇФЃФт)ЯТСаЮяжЪЗжРыЙ§ГЬжаЩцМАЙВМлМќЖЯСбЕФЪЧ(ЁЁЁЁ )
AЃЎгУЩјЮіЗЈГ§ШЅЕэЗлНКЬхжаЕФЩйСПNaClЁЁ BЃЎгУБЅКЭЪГбЮЫЎЯДШЅCl2жаЕФЩйСПHCl
CЃЎгУCCl4нЭШЁЕтЫЎжаЕФЕтЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎгУЩ§ЛЊЗЈГ§ШЅNaClжаЛьгаЕФЩйСПЕт
[НтЮі]бЁBЁЃAбЁЯюжаЦЦЛЕЕФЪЧРызгМќЃЛBбЁЯюжаЦЦЛЕЕФЪЧЙВМлМќЃЛCЁЂDбЁЯюжаЮоЛЏбЇМќЦЦЛЕЁЃ
|
ађКХ |
дЮя |
ЫљКЌдгжЪ |
Г§дгжЪЪдМС |
жївЊВйзїЗНЗЈ |
|
1 |
N2 |
O2 |
зЦШШЕФЭЫПЭј |
гУЙЬЬхзЊЛЏЦјЬх |
|
2 |
CO2 |
H2S |
CuSO4ШмвК |
ЯДЦј |
|
3 |
CO |
CO2 |
NaOHШмвК |
ЯДЦј |
|
4 |
CO2 |
CO |
зЦШШCuO |
гУЙЬЬхзЊЛЏЦјЬх |
|
5 |
CO2 |
HCl |
БЅКЭЕФNaHCO3 |
ЯДЦј |
|
6 |
H2S |
HCl |
БЅКЭЕФNaHS |
ЯДЦј |
|
7 |
SO2 |
HCl |
БЅКЭЕФNaHSO3 |
ЯДЦј |
|
8 |
Cl2 |
HCl |
БЅКЭЕФЪГбЮЫЎ |
ЯДЦј |
|
9 |
CO2 |
SO2 |
БЅКЭЕФNaHCO3 |
ЯДЦј |
|
10 |
ЬПЗл |
MnO2 |
ХЈбЮЫс(ашМгШШ) |
Й§ТЫ |
|
11 |
ЬПЗл |
CuO |
ЯЁЫс(ШчЯЁбЮЫс) |
Й§ТЫ |
|
12 |
Al2O3 |
Fe2O3 |
NaOH(Й§СП)ЃЌCO2
|
Й§ТЫ |
|
13 |
Fe2O3 |
Al2O3 |
NaOHШмвК |
Й§ТЫ |
|
14 |
Al2O3 |
SiO2 |
бЮЫс`АБЫЎ |
Й§ТЫ |
|
15 |
SiO2 |
ZnO |
HClШмвК |
Й§ТЫЃЌ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ |
|
16 |
BaSO4 |
BaCO3 |
HClЛђЯЁH2SO4 |
Й§ТЫ |
|
17 |
NaHCO3ШмвК |
Na2CO3 |
CO2 |
МгЫсзЊЛЏЗЈ |
|
18 |
NaClШмвК |
NaHCO3 |
HCl |
МгЫсзЊЛЏЗЈ |
|
19 |
FeCl3ШмвК |
FeCl2 |
Cl2 |
МгбѕЛЏМСзЊЛЏЗЈ |
|
20 |
FeCl3ШмвК |
CuCl2 |
Fe ЁЂCl2 |
Й§ТЫ |
|
21 |
FeCl2ШмвК |
FeCl3 |
Fe |
МгЛЙдМСзЊЛЏЗЈ |
|
22 |
CuO |
Fe |
(ДХЬњ) |
ЮќИН |
|
23 |
Fe(OH)3НКЬх |
FeCl3 |
еєСѓЫЎ |
ЩјЮі |
|
24 |
CuS |
FeS |
ЯЁбЮЫс |
Й§ТЫ |
|
25 |
I2ОЇЬх |
NaCl |
-------- |
МгШШЩ§ЛЊ |
|
26 |
NaClОЇЬх |
NH4Cl |
-------- |
МгШШЗжНт |
|
27 |
KNO3ОЇЬх |
NaCl |
еєСѓЫЎ |
жиНсОЇ. |
|
28 |
ввЯЉ |
SO2ЁЂH2O |
МюЪЏЛв |
МгЙЬЬхзЊЛЏЗЈ |
|
29 |
ввЭщ |
C2H4 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ |
фхЕФЫФТШЛЏЬМШмвК |
ЯДЦј |
|
30 |
фхБН |
Br2 |
NaOHЯЁШмвК |
ЗжвК |
|
31 |
МзБН |
БНЗг |
NaOHШмвК |
ЗжвК |
|
32 |
МКШЉ |
ввЫс |
БЅКЭNa2CO3 |
еєСѓ |
|
33 |
ввДМ |
ЫЎ(ЩйСП) |
аТжЦCaO |
еєСѓ |
|
34 |
БНЗг |
БН |
NaOHШмвКЁЂCO2 |
ЗжвК |
ЪдЬтУЖОй
[Р§1]ЬсДПКЌгаЩйСПЯѕЫсБЕдгжЪЕФЯѕЫсМиШмвКЃЌПЩвдЪЙгУЕФЗНЗЈЮЊ
A .МгШыЙ§СПЬМЫсФЦШмвКЃЌЙ§ТЫЃЌГ§ШЅГСЕэЃЌШмвКжаВЙМгЪЪСПЕФЯѕЫс
B.МгШыЙ§СПСђЫсМиШмвКЃЌЙ§ТЫЃЌГ§ШЅГСЕэЃЌШмвКжаВЙМгЪЪСПЕФЯѕЫс
C.МгШыЙ§СПСђЫсФЦШмвКЃЌЙ§ТЫЃЌГ§ШЅГСЕэЃЌШмвКжаВЙМгЪЪСПЕФЯѕЫс
D.МгШыЙ§СПЬМЫсМиШмвКЃЌЙ§ТЫЃЌГ§ШЅГСЕэЃЌШмвКжаВЙМгЪЪСПЕФЯѕЫс
НтЮі AВНжшжаМгШыЙ§СПЬМЫсФЦЃЌФЦРызгЪЧаТдгжЪЃЌДЫЗЈВЛПЩгУЃЛBВНжшжаМгШыЙ§СПСђЫсМиЃЌЙ§СПЕФСђЫсМиЪЧаТдгжЪЃЌДЫЗЈВЛПЩгУЃЛCВНжшМгШыЙ§СПСђЫсФЦЃЌФЦРызгКЭЙ§СПЕФСђЫсИљРызгЃЌЖМЪЧаТдгжЪЃЌДЫЗЈВЛПЩгУ.ЁЃжЛгаDЬМЫсМиПЩЪЙЬМЫсБЕЩњГЩЬМЫсБЕГСЕэЃЌЙ§ТЫГіШЅКѓЃЌЙ§СПЬМЫсМиИњЪЪСПЯѕЫсЩњГЩЯѕЫсМиКЭCO2ЦјЬхЃЌЯѕЫсМиЪЧД§ЬсДПЕФЮяжЪЖјCO2НЋвнГіЁЃЫљвдДЫЗЈПЩгУЃЌгІбЁDЯюЁЃ
Д№АИ D
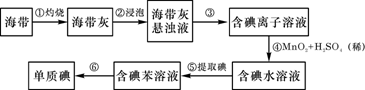
[Р§2](06ЫФДЈИпПМ26) КЃДјКЌгаЗсИЛЕФЕтЃЌЮЊСЫДгКЃДјжаЬсШЁЕтЃЌФГбаОПадбЇЯАаЁзщЩшМЦВЂНјааСЫвдЯТЪЕбщЃК
 ЁЁ
ЁЁ
ЧыЬюаДЯТСаПеАзЃК
(1)ВНжшЂйзЦЩеКЃДјЪБЃЌГ§ашвЊШ§НЧМмЭтЃЌЛЙашвЊгУЕНЕФвЧЦїЪЧЁЁЁЁЁЁЁЁЁЁЁЁ (ДгЯТСавЧЦїжабЁдёЫљашЕФвЧЦїЃЌгУБъКХзжФИЬюаДдкПеАзДІ)
AЁЂЩеБЁЁ BЁЂлсліЁЁ CЁЂБэУцУѓЁЁ DЁЂФрШ§НЧЁЁ EЁЂОЦОЋЕЦЁЁ FЁЂИЩдяЦї
(2)ВНжшЂлЕФЪЕбщВйзїУћГЦЪЧЁЁЁЁЁЁЁЁЁЁ ЃЛВНжшЂоЕФФПЕФЪЧДгКЌЕтБНШмвКжаЗжРыГіЕтКЭЛиЪеБНЃЌИУВНжшЕФЪЕбщВйзїУћГЦЪЧЁЁЁЁ ЁЁЁЁЁЁЁЁЁЃ
(3)ВНжшЂмЗДгІЕФРызгЗНГЬЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(4)ВНжшЂнжаЃЌФГбЇЩњбЁдёгУБНРДЬсШЁЕтЕФРэгЩЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(5)ЧыЩшМЦвЛжжМьбщЬсШЁЕтКѓЕФЫЎШмвКжаЪЧЗёЛЙКЌгаЕЅжЪЕтЕФМђЕЅЗНЗЈЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
НтЮі БОЬтЪЧвдДгКЃДјжаЬсШЁЕтЮЊБГОАЃЌзлКЯПМВщСЫЮяжЪЕФЗжРыЁЂМьбщЕШЛљБОЪЕбщжЊЪЖЁЃ
зЦЩеКЃДјЪБЃЌГ§ашвЊШ§НХМмЭтЃЌЛЙашвЊгалсліЁЂФрШ§НЧКЭОЦОЋЕЦЁЃВНжшЂлЪЧгЩКЃДјЛваќзЧвКЕУЕНКЌЕтРызгЕФШмвКЃЌвђДЫашвЊНјааЙ§ТЫЁЃВНжшЂоЪЧДгКЌЕтБНШмвКжаЗжРыГіЕЅжЪЕтКЭЛиЪеБНЃЌжЛФмВЩгУеєСѓЕФЗНЗЈЁЃВНжшЂмЗДгІЕФРызгЗНГЬЪНРћгУЪЕбщЪвжЦШЁCl2ЕФжЊЪЖЃЛбЁдёгУБНРДЬсШЁЕтЕФРэгЩЪЧвђЮЊБНгыЫЎЛЅВЛЯрШмЧвЕтдкБНжаЕФШмНтЖШБШдкЫЎжаДѓЃЛИљОнЕтЕЅжЪгіЕэЗлБфРЖетвЛЪЕбщЯжЯѓПЩвдЭЈЙ§ШЁЩйСПЬсШЁЕтКѓЕФШмвКЃЌМгШыЕэЗлПДЪЧЗёБфРЖРДМьбщЁЃЁЁ
Д№АИ(1)зЦЩеКЃДјашвЊлслі(ЪЂЗХКЃДј)ЁЂИщЗХлсліЕФФрШ§НЧЁЂЛ№дДОЦОЋЕЦЁЃзЂвтВЛвЊИЩдяЦїЁЃBDE (2)ЗжРыаќзЧвККЭШмвКгІгУЙ§ТЫЁЂЗжРыГіЕтКЭБНгУеєСѓЁЃ
(3)2I-+MnO4-+4H+==Mn2++I2+2H2O(4)БНгыЫЎЛЅВЛЯрШмЃЌЕтдкБНжаЕФШмНтЖШБШдкЫЎжаДѓЁЃ(5)МьбщЕЅжЪЕтЗНЗЈЃКШЁЩйСПЬсШЁЕтКѓЕФЫЎШмвКгкЪдЙмжаЃЌМгШыМИЕЮЕэЗлЪдвКЃЛЙлВьЪЧЗёГіЯжРЖЩЋ(ШчЙћБфРЖЃЌЫЕУїЛЙгаЕЅжЪЕт)ЁЃ
[Р§3]вбжЊЛЏКЯЮяМзКЭввЖМВЛШмгкЫЎЃЌМзПЩШмгкжЪСПЗжЪ§ДѓгкЛђЕШгк98%ЕФСђЫсЃЌЖјввВЛШмЁЃЯжгавЛЗнМзКЭввЕФЛьКЯЮябљЦЗЃЌЭЈЙ§ЪЕбщНјааЗжРыЃЌПЩЕУЕНЙЬЬхМзЁЃ(ЪЕбщжаЪЙгУЕФЙ§ТЫЦїЪЧгУгкЙ§ТЫЧПЫсадвКЬхЕФФЭЫсЙ§ТЫЦїЁЃ)
ЧыЬюаДБэжаПеИёЃЌЭъГЩгЩЩЯЪіЛьКЯЮяЕУЕНЙЬЬхМзЕФЪЕбщЩшМЦЁЃ
|
ађКХ |
ЪЕбщВНжш |
МђЪіЪЕбщВйзї(ВЛБиа№ЪіШчКЮзщзАЪЕбщзАжУ) |
|
Ђй |
ШмНт |
НЋЛьКЯЮяЗХШыЩеБжаЃЌМгШы98%
H2SO4 ЃЌГфЗжНСАшжБЕНЙЬЬхВЛдйШмНтЁЃ |
|
Ђк |
ЁЁ |
ЁЁ |
|
Ђл |
ЁЁ |
ЁЁ |
|
Ђм |
ЁЁ |
ЁЁ |
|
Ђн |
ЯДЕгГСЕэ |
ЁЁ |
|
Ђо |
МьбщГСЕэЪЧЗёЯДОЛ |
ЁЁ |
НтЮі БОЬтЭЈЙ§ЖдЛьКЯЮяЕФЗжРыПМВщЪЕбщЩшМЦКЭЛЏбЇЪЕбщЛљБОВйзїЁЃ
ЬтжаИјГіСЫаХЯЂЁАЛЏКЯЮяМзКЭввЖМВЛШмгкЫЎЃЌМзПЩШмгкжЪСПЗжЪ§ДѓгкЛђЕШгк98%ЕФСђЫсЃЌЖјввВЛШмЁБЃЌгжИјГіСЫЕквЛВНЪЕбщВйзїЁАНЋЛьКЯЮяЗХШыЩеБжаЃЌМгШы98% H2SO4 ЃЌГфЗжНСАшжБЕНЙЬЬхВЛдйШмНтЁБЁЃзлКЯЗжЮіСНИіаХЯЂЃЌгІИУжЊЕРЪЕбщЩшМЦЕФДѓЬхЫМТЗЃКгУХЈСђЫсНЋМзШмНтЃЌЙ§ТЫГіввКѓЃЌТЫвКМгШыЫЎжаЯЁЪЭЭЌЪБЮіГіМзЃЌдйЙ§ТЫЁЃ
жЊЕРСЫЪЕбщЩшМЦЕФДѓЬхЫМТЗжЎКѓЃЌОЭашвЊПМТЧВйзїЕФЯИНкЮЪЬтСЫЃККЌХЈСђЫсЕФТЫвКгыЫЎЛьКЯЪБгІдѕбљВйзїЃПЙ§ТЫЕУЕНЕФГСЕэЮяашвЊЯДЕгЃЌдѕбљЯДЃПдѕбљВХЫуЯДИЩОЛСЫЃПЕШЕШЁЃ
Д№АИЂкЙ§ТЫЁЁЁЁ НЋЩеБжаЮяжЪЕЙШыФЭЫсЙ§ТЫЦїжаЙ§ТЫЃЌЕУТЫвКЁЃ
ЂлЮіГіГСЕэЁЁ НЋТЫвКбиЩеББкТ§Т§ЕЙШызуСПЫЎжаЃЌВЂВЛЖЮНСАшЃЌжБжСЮіГіШЋВПЙЬЬхЁЃ
ЂмЙ§ТЫЁЁЁЁЁЁ НЋДЫЩеБжаЕФЮяжЪЕЙШыЙ§ТЫЦїжаЙ§ТЫЃЌЕУЙЬЬхЁЃ
ЂнгУеєСѓЫЎГхЯДТЫжНЩЯЕФЙЬЬхШєИЩДЮЃЌжБжСЯДОЛЁЃ
ЂоШЁаТЕУЕНЕФЯДГівКЩйаэЃЌЕЮШыгУбЮЫсЫсЛЏЕФBaCl2 ШмвК ЃЌШєУЛгаАзЩЋЛызЧГіЯжЃЌдђЫЕУїГСЕэвбЯДОЛЃЌШєгаАзЩЋЛызЧГіЯжЃЌдђЫЕУїГСЕэУЛгаЯДОЛЁЃЁЁ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com