
8.为确定某溶液的离子组成,进行如下实验:
①测定溶液的pH,溶液显强碱性。
②取少量溶液加入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体。
③在上述溶液中再滴加Ba(NO3)2溶液,产生白色沉淀。
④取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀。
根据实验以下推测正确的是
A.一定有SO32-离子 B.一定有CO32-离子
C能确定Cl-离子存在 D.不能确定HCO3-离子是否存在
7.下列离子方程式中正确的是
A.H2SO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O
B.Ca(HCO3)2与过量Ca(OH)2溶液反应:
Ca2++HCO3-+2OH-=CaCO3↓+CO32-+2H2O
C.Na2CO3溶液中通入少量CO2:CO32-+CO2+ H2O=2HCO3-
D.CH3COOH溶液与NaOH溶液反应:H++ OH-=H2O
6.下列化工生产过程中所发生的主要化学反应不属于氧化还原反应的是 ( )A.用氯气和消石灰制漂白粉 B.铝热法冶炼金属铝
C.用油脂制肥皂 D.电解饱和食盐水制烧碱
5.已知某溶液中存在较多的H+、SO42-、NO3-,则溶液中还可能大量存在的离子组是
A.Al3+、CH3COO-、Cl- B.Na+、NH4+、Cl-
C.Mg2+、Cl-、Fe2+ D.Mg2+、Ba2+、Br-
4.把分别盛有熔融的氯化钾、氯化镁、氯化铝的三个电解槽串联,在一定条件下通电一段时间后,析出钾、镁、铝的物质的量之比为
A.1∶2∶3 B.3∶2∶1 C.6∶3∶1 D.6∶3∶2
3.下列反应中,氧化剂与还原剂物质的量的关系为1∶2的是
A.O3+2KI+H2O=2KOH+I2+O2
B.2CH3COOH+Ca(ClO)2=2HClO+Ca(CH3COO)2
C.I2+2NaClO3=2NaIO3+Cl2
D.4HCl+MnO2 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
2.已知: ①向KMnO4晶体滴加浓盐酸,产生黄绿色气体;②向FeCl2溶液中通入少量实验①产生的气体,溶液变黄色; ③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色。下列判断正确的是
A.上述实验证明氧化性: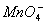 >Cl2>Fe3+>I2
>Cl2>Fe3+>I2
B.上述实验中,共有两个氧化还原反应
C.实验①生成的气体不能使湿润的淀粉KI试纸变蓝
D.实验②证明Fe2+既有氧化性又有还原性
1.在烧杯中加入水和苯(密度:0.88 g/cm3)各50 mL。将一小粒金属钠(密度:0.97 g/cm3)投入烧杯中。观察到的现象可能是
A.钠在水层中反应并四处游动
B.钠停留在苯层中不发生反应
C.钠在苯的液面上反应并四处游动
D.钠在苯与水的界面处反应并可能作上、下跳动
18.为了安全,在公路上行驶的汽车之间应保持必要的距离.已知某高速公路的最高限速v=120 km/h,假设前方车辆突然停止,后车司机从发现这一情况,经操纵刹车,到汽车开始减速所经历的时间(即反应时间)t=0.50 s,刹车时汽车受到阻力的大小f为汽车重力的0.40倍.该高速公路上汽车间的距离s至少应为多少?取重力加速度g=10 m/s2.
答案:1.6×102 m
[1A 2C 3B 4A 5C 6C 7C 8D 9A 10B 11A 12B 13AC 14C]
17. 风洞实验室中可产生水平方向的.大小可调节的风力.现将一套有小球的细直杆放入风洞实验室,小球孔径略大于细杆直径.
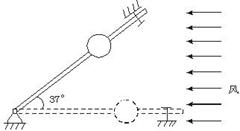 (1)当杆在水平方向上固定时,调节风力的大小,使小球在杆上作匀速运动,这时小球所受的风力为小球所受重力的0.5倍,求小球与杆间的滑动摩擦因数.
(1)当杆在水平方向上固定时,调节风力的大小,使小球在杆上作匀速运动,这时小球所受的风力为小球所受重力的0.5倍,求小球与杆间的滑动摩擦因数.
(2)保持小球所受风力不变,使杆与水平方向间夹角为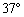 并固定,则小球从静止出发在细杆上滑下距离S所需时间为多少?(sin
并固定,则小球从静止出发在细杆上滑下距离S所需时间为多少?(sin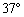 =0.6,cos
=0.6,cos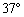 =0.8)
=0.8)
答案 μ=F/mg=0.5 t==
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com