
6.△ABC的三个内角,A,B,C的对边分别为a,b,c,且 ,则A=( )
,则A=( )
A.150° B.120° C.60° D.30°
5.函数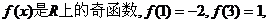 则 ( )
则 ( )
A.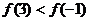 B.
B.
C.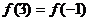 D.
D.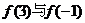 的大小不能确定
的大小不能确定
4.已知函数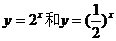 ,则它们的反函数的图象 ( )
,则它们的反函数的图象 ( )
A.关于直线 对称 B.关于x轴对称
对称 B.关于x轴对称
C.关于y轴对称 D.关于原点对称
3. = ( )
= ( )
A.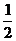 B.-
B.-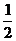 C.
C.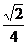 D.-
D.-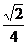
2.已知向量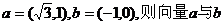 的夹角为 ( )
的夹角为 ( )
A. B.
B.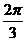 C.
C. D.
D.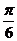
1.复数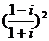 = ( )
= ( )
A.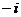 B.
B. C.-1 D.1
C.-1 D.1
25.(15分)
 某芳香族化合物A发生以下反应:(已知B的相对分子质量为108.有机玻璃的结构简式为
某芳香族化合物A发生以下反应:(已知B的相对分子质量为108.有机玻璃的结构简式为 。)
。)
回答下列问题:
(1)A的分子式为 。
(2)G的结构简式 。
(3)B→D的反应类型 ,H-→I的反应类型 。
(4)C→H的反应方程式 。
D→E的反应方程式 。
(5)符合以下条件的M的同分异构体有 种(不包括M)
①含有苯环结构 ②含有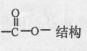
写出其中一种的结构简式 。
24.(15分)
请设计实验:用MnO2与浓盐酸制备纯净、干燥的Cl2,其他药品与试剂任选。
(1)写出该反应的化学方程式 。
(2)在下面方框中,A表示有分液漏斗和圆底烧瓶组成的气体发生器,请在虚线框内的A后完成该反应的实验装置示意图(夹持装置、连接胶管不必画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母B、C……;其他可选用的仪器(数量不限)简易表示如下:
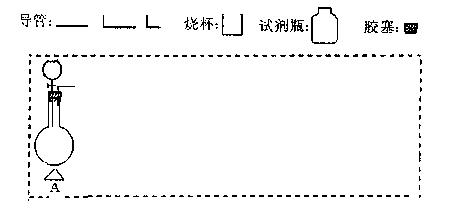
(3)根据方框中的装置图,完成下表(若无需填写,则在表格中写“无”)
|
仪器符号 |
仪器中所加物质 |
作用 |
|
A |
MnO2、浓盐酸 |
MnO2与浓盐酸生成Cl2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(4)KMnO2与浓盐酸在常温下反应也可以得到Cl2,请写出该反应的离子方程式 。
(5)请写出Cl2在工业、农业、医疗、卫生等方面的用途 。(写出两种即可)
(6)将Cl2与SO4分别通人品红溶液,都能使品红褪色。简述用褪色的溶液区别二者的实验方法。
23.(12分)某温度时,在2L密闭容器中气态物质CO和H2反应生成气态物质Z,它们的物质的量随时间的变化如下表所示。
|
t/min |
CO/mol |
H2/mol |
Z/mol |
|
0 |
1.00 |
1.00 |
0.00 |
|
1 |
0.90 |
0.80 |
0.10 |
|
3 |
0.75 |
0.50 |
0.25 |
|
5 |
0.65 |
0.30 |
0.35 |
|
7 |
0.55 |
0.10 |
0.45 |
|
9 |
0.55 |
0.10 |
0.45 |
|
10 |
0.55 |
0.10 |
0.45 |
 (1)(根据上表中数据,在下图中画出CO、z的物质的量的浓度(c)随时间(t)变化的曲线:
(1)(根据上表中数据,在下图中画出CO、z的物质的量的浓度(c)随时间(t)变化的曲线:
(2)体系中发生反应的化学方程式是 。
(3)在3-5 min时间内产物Z的平均反应速率: 。
(4)图2表示该反应进行过程中能量的变化。曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化。该反应是 (填“吸热”或“放热”)反应,反应的热化学方程式是 。
(5)恒容条件下,下列措施中能使n(CH3OH)/n(CO)增大的有 (选填序号)。
a.升高温度 b.使用催化剂 C.再充人2 mol H2 d.再充人2 mol He
22.(14分)
电子总数均为14的微粒有X、Y、Z、Q、R、W 6种,按要求填空:
(1)x、Y为两种单质,X的氧化物是制造光导纤维的主要原料,X的晶体类型为 ,该氧化物的化学式为 ;Y为分子晶体,其电子式为 。
(2)Z分子中含有4个原子,其分子的空间构型是 。
(3)Q为低价氧化物,请写出有Q生成的置换反应 。
(4)R为-2价阴离子,请写出R与钙离子组成的离子化合物与水反应的化学方程式 。
(5)W为两种相邻元素构成的-1价阴离子,其钠盐水溶液显碱性的原因是 。(用离子方程式表示)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com