
1、实验原理:2NH4Cl+Ca(OH)2 CaCl2+2NH3 ↑+2H2O
CaCl2+2NH3 ↑+2H2O
 [讲]反应是离子反应,但此反应为非水溶液中进行,因而写不出离子反应方程式。所用铵盐不能用NH4NO3和NH4HCO3,因为加热过程中NH4NO3可能发生爆炸性分解反应,发生危险,而NH4HCO3受热易分解产生O2,使生成的NH3中混有较多杂质。另外选用消石灰Ca(OH)2,不能用NaOH和KOH代替,其主要原因是:NaOH、KOH具有易湿性,易结块,不利于产生NH3。NaOH、KOH在高温下能腐蚀玻璃管。除了用NH4Cl和消石灰固体共热易NH3外,还可以在常温下用浓氨水与固体烧碱或生石灰混合快速制取NH3。
[讲]反应是离子反应,但此反应为非水溶液中进行,因而写不出离子反应方程式。所用铵盐不能用NH4NO3和NH4HCO3,因为加热过程中NH4NO3可能发生爆炸性分解反应,发生危险,而NH4HCO3受热易分解产生O2,使生成的NH3中混有较多杂质。另外选用消石灰Ca(OH)2,不能用NaOH和KOH代替,其主要原因是:NaOH、KOH具有易湿性,易结块,不利于产生NH3。NaOH、KOH在高温下能腐蚀玻璃管。除了用NH4Cl和消石灰固体共热易NH3外,还可以在常温下用浓氨水与固体烧碱或生石灰混合快速制取NH3。
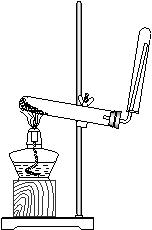
[讲]实验装置如图,与O2的制备装置相似。是典型的固体与固体热反应制备气体的装置。那么,作为一种典型的碱性气体,可以用什么来干燥氨气呢?
[板书]2、干燥剂:碱石灰
[讲]不能选用浓硫酸、硅胶等酸性干燥剂,是因为酸碱反应,而不能选用CaCl2,是因为CaCl2与NH3反应生成CaCl2·8NH3
[板书]3、收集方法:向下排空气法
2、氨气在纯氧中点燃
9、将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L。(1)NO的体积为多少?(2)NO2的体积为多少?
8、1.92gCu投入到一定量浓HNO3中,铜完全溶解,生成的气休颜色由深变成浅(不考虑2NO2 N2O4),共收集到672mL气体(标况),通入一定体积的O2恰好使气体完全溶于水,求通入O2的体积(标况)。
7、常温时,将a mol Cu和 a mol Fe 投入含 b mol HNO3的浓硝酸中,经一段时间后,使它们恰好完全反应。已知反应后溶液中Fe3+和Fe2+的物质的量相等,HNO3的还原产物为NO和NO2,且不考虑NO2转化为N2O4。反应中可产生气体560 mL,将该气体溶于水,充分反应后,气体体积减少224 mL(气体体积均为标准状况下体积)。求a,b的值。
6、将1.28克Cu跟一定量的浓HNO3反应,铜消耗完全时,共产生0.56L(标准状况)气体。所消耗HNO3的物质的量为多少?
5、在 4mol/L 的H2SO4和2 mol/L的HNO3混合溶液 10 mL中,加入0.96克铜粉,充分反应后,最多可收集到标准状况下的气体的体积为多少?
4、将Mg、Cu组成的2.64克混合物投入适量稀HNO3中恰好反应,固体完全溶解时收集到的还原产物NO气体0.896L(标准状况),向反应后溶液中加入2mol/L NaOH溶液60 mL时,金属离子恰好沉淀完全,则形成沉淀的质量为多少?
3、30 mL 一定浓度的硝酸溶液与5.12克铜片反应,当铜片全部反应完毕后,共收集到气体2.24L(S.T.P),则该HNO3溶液的物质的量浓度至少为多少?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com