
1.(14分)下图I中放一盆正常生长的大豆,II处为-U型管,III处放一只健康的小白鼠,V使装置中的空气以一定速度按箭头方向流动。根据装置图分析回答问题。
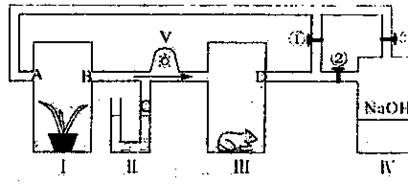
(1)开关①打开,②③关闭,如果不给光照,装置内空气中 (物质)含量增加。
(2)与(1)相同条件,给装置I中的植物适量的水、矿质元素,同时给以适宜光照,一段时间后,B、D两处的成分差别是 。
(3)开关①关闭,②③打开,同样光照条件下,I中生物叶肉细胞的C3含量 ;C5含量 ;C处液面 。(上升、下降)
(4)在(3)中条件下,I中生物刚开始产生O2较多,但随时间延长,O2产生量越来越少,原因是 。一段时间后,III中的小白鼠体内 (填物质的名称)将会略有积累。
3、3mol Cu和含7mol H2SO4的浓H2SO4共热,未被还原的H2SO4有( )
A、3mol B.4mol C、少于4mol D、一定多于4mol
2.下列关于浓硫酸的叙述正确的是( )
A.浓硫酸具有吸水性,因而能使蔗糖碳化
B.浓硫酸在常温下可迅速与铜片反应放出SO2气体
C.浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
D.浓硫酸在常温下能够使铁、铝等金属钝化
1、在下列用途或反应中,硫酸表现出的性质为:A、高沸点性 B、强酸性 C、吸水性 D、脱水性 E、强氧化性
(1)实验室制取氢气___
(2)实验室制取氯化氢气体___
(3)干燥二氧化硫____
(4)浓硫酸溶解金属铜 ___
(5)浓硫酸用钢瓶保存__
(6)浓硫酸与蔗糖反应___
2、把Al放入浓H2SO4中,1-2分钟后,无明显现象。
1、用热的NaOH溶液处理Al表面的氧化膜,迅速放入饱和硫酸铜溶液的试管中,过一会儿取出,
现象:Al表面变红,2Al+3Cu2+== 2Al3++3Cu
3.能够干燥:SO2、CO2、H2 、HCl、O2等
[视频实验]浓硫酸与胆矾的反应
操作:在表面皿里放入少量胆矾,并滴加少量浓硫酸
现象:固体由蓝变白,
[问]白色固体可能是什么呢?
无水硫酸铜。
[讲]浓硫酸不仅能吸收游离态的H2O还能吸收某些结晶水合物中的水。
[视频实验]浓硫酸与棉花的反应
现象:变黑
[讲]黑色物质为炭,浓H2SO4使它们逐渐变黑的现象称为炭化,这是浓H2SO4的脱水性。
[板书]2、脱水性:
浓硫酸可以按水中H、O原子个数比2:1夺取有机物中的H、O,脱水后生成碳。
浓硫酸的脱水性导致了它的强腐蚀性
[投影小结]吸水性与脱水性的对比小结
|
|
吸水性 |
脱水性 |
|
对象 |
游离态的H2O、结晶水合物中的H2O |
一般含H、O的有机物,H、O按物质的量比为2:1脱去 |
|
类型 |
化学变化 |
化学变化 |
|
能量 |
放热 |
放热 |
|
现象 |
无明显现象 |
得到黑色固体 |
|
关系 |
有脱水则必吸水 |
[视频实验]蔗糖与浓硫酸的反应
操作:将预先称量的20g蔗糖放入100 mL 烧杯中,加几滴H2O搅拌均匀,再加15 mL 浓硫酸,用玻璃棒迅速搅拌


现象:蔗糖由白变黑,体积膨胀,呈疏松海绵状,有刺激性气味气体生成,放出大量的热
[思考与交流]根据实验现象,推测可能发生了哪些化学反应?浓硫酸体现了哪些化学性质?反应后的产物是什么?
蔗糖变黑说明有炭生成;“体积膨胀,呈疏松多孔状”说明有大量气体生产;刺激性气味的气体有可能是SO2 ;在此过程中,炭可能和浓硫酸发生了反应,生成了CO2 和SO2 气体。
[思考与交流]将浓硫酸滴到干燥的蓝色石蕊试纸上,可能会出现什么现象?
变黑
[思考与交流]万一不慎将浓硫酸溅到皮肤上,眼睛上、衣服上或桌面上,如何处理?
先用干抹布擦,再用大量水洗。
[讲]蔗糖为含C、H、O元素的有机物遇浓H2SO4会炭化变黑,那么有何种气体生成呢?要想知道答案,就必须学习浓硫酸的另一个特性
[板书]3、强氧化性
[问]有酸的能性可知,稀硫酸与Cu不反应,那么与浓硫酸呢?
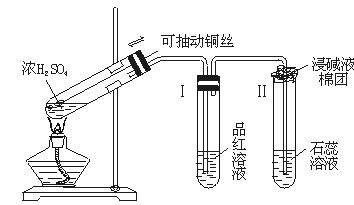
[视频实验]铜与浓硫酸的反应
实验现象:
①试管A中Cu片的表面有气泡产生,溶液由无色变为蓝色,说明Cu与浓硫酸反应时,Cu被氧化(氧化或还原)成了Cu2+ ;
②试管B中的品红溶液由红色变为无色,说明Cu与浓硫酸反应时,H2SO4被还原(氧化或还原),生成了SO2 气体
③试管C中石蕊溶液由紫色变为 红 色
[讲]在这装置中,浸碱液的棉团起尾气吸收的作用。
[问]Cu与浓硫酸反应需要什么条件?据实现现象推测反应物,并写方程式。
[板书](1) 与金属反应
Cu +2H2SO4(浓) CuSO4 +SO2
↑+2H2O
CuSO4 +SO2
↑+2H2O
[练习]请同学们用双线桥标出电子转移,并指出氧化剂和还原剂。
氧化剂:浓H2SO4 还原剂:Cu
[问]在这个反应中,浓硫酸都起什么作用?
浓硫酸中的硫被还原,因而表现强氧化性;有硫酸铜生成,表面硫酸的酸性。
[思考与交流]稀H2SO4是否具有氧化性?这与浓硫酸的强氧化性有何区别?
浓硫酸的氧化性是由+6价的S元素表现的,稀H2SO4也有氧化性,是由H+表现出来的,是酸的通性。
[讲]酸的氧化性是指电离出H+所表现的氧化性,是酸的共性。而氧化性的酸是指组成酸的具有变价的元素所表现出的氧化性。
[过]H之后的Cu可以被浓H2SO4氧化,那么,H之前的金属能否被氧化呢?
[探究性实验]
2.不能干燥还原性气体:H2S、HI、HBr
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com