
4.t℃时,向硝酸钠饱和溶液中加入一定量的水后,下列有关该溶液的叙述正确的是( )
A.仍为饱和溶液 B.溶质的质量变小
C.溶质的溶解度不变 D.溶质的质量分数不变
3.某学生要配制质量分数为10%的食盐溶液,他读量筒内水的体积刻度时,视线仰视,而调整天平平衡时,指针偏左,称量食盐时天平平衡,则他配制的食盐溶液的质量分数是( )
A.等于10% B.小于10% C.大于10% D.无法确定
2.对100克溶质质量分数为10%的某物质的溶液,分别进行如下操作:①加入10g水 ②加入10g同种溶质,且完全溶解 ③加入溶质质量分数为10%的同种溶质的溶液10g ④蒸发掉10g水,无晶体析出。操作后的四种溶液中溶质的质量分数由小到大的顺序是( )
A.①②③④ B.①③④②
C.④③②① D.④②③①
1.知道溶质的质量分数是是溶质的质量与溶液的质量之比。
2.能进行有关溶质质量分数的简单计算。
3.初步学会配制一定溶质质量分数的溶液。
二、命题落点
1.以选择、填空等形式来考查有关溶质质量分数的简单计算。如例1。
2.联系生活实际,考查溶液知识及其有关计算,如例2。
3.分析、判断不同“溶质”溶于水时所引起的溶质质量分数的变化情况,如例3。
4.依据公式进行溶液配制实验误差的分析,如例4。
[典例精析]
例1.将一瓶80g 溶质质量分数为10%的NaCl溶液平均分为2等份,每份溶液中溶质的质量分数为 ;若将其中的一份溶液中溶质的质量分数减小一半,应加水 g,若将另一份溶液中溶质的质量分数增大一倍,应加入NaCl g。
解析:根据溶液的均一性可知,无论将原来的溶液怎么样来分,只要条件不改变,其溶质的质量分数是不会发生变化的。增加溶剂的质量能使溶质的质量变小,加入多少水才能使40g(原溶液质量的一半)10%的NaCl溶液的溶质质量分数减小一半(即5%)呢?显然,所加水的质量应该和对应溶液的质量一样多(40g);通过加入溶质的方法肯定能使溶液中溶质的质量分数增大,那么,所加入的溶质质量怎样计算呢?很简单:依据溶质质量分数的计算公式。但要注意,加入这部分溶质后,不仅能使溶质的质量增大,同样也使溶液的质量增大。若设加入的溶质质量为x,则由题意可得:
(x+40g×10%)÷(40+x)=20% 解之,x=5g。
答案:10%;40;5 。
例2.(2003年南京市中考题)日常生活中我们要科学地节约用水。现有一件刚用洗涤剂洗过的衣服,“拧干”后湿衣服上残留的溶液为100g,其中洗涤剂的质量分数为1%,则湿衣服上残留的洗涤剂质量为 g。现用5700g清水对这件衣服进行漂洗,有以下两种漂洗方法(假设每次“拧干”后湿衣服仍残留100g溶液):
方法一:用5700g清水漂洗,"拧干"后残留在衣服上的洗涤剂质量为(用分数表示,下同) g;
方法二:用5700g清水均匀分成质量相等的三份(每份1900g),分三次漂洗:
第1次,用1900g清水漂洗,“拧干”后残留在衣服上的洗涤剂质量为 g;
第2次,用1900g清水漂洗,“拧干”后残留在衣服上的洗涤剂质量为 g;
第3次,用1900g清水漂洗,“拧干”后残留在衣服上的洗涤剂质量为 g。
由以上计算分析,用相同质量的水漂洗衣服,是一次漂洗效果好,还是将水分成三份,分三次漂洗效果好?
解析:这是一道密切联系生活实际的简单计算题。试题旨在通过简单计算,使大家明白并掌握节约用水的一种方法。通过这种方法的介绍,引导我们进一步树立节约水、爱惜水的观念,做到合理地利用水、科学地节约和保护水。其实,该题的实质是关于溶质溶解、溶液稀释的计算。它以日常生活中的小事为背景,将漂洗衣服时为什么要“少量多次”的科学道理让学生通过计算加以感受,既考查了分析与计算能力,又进行了节约用水的方法教育,真可谓“匠心独具”,是一道难得的好题。
解答时要注意:题中“拧干后湿衣服上残留的溶液仍为100g”,这就意味着不论用什么方法、进行哪一次漂洗,这“100g溶液”始终应跟随在计算的过程中。如用方法2进行第一次漂洗,漂洗时所用“水”的总质量就应当是:1900g+100g=2000g,“拧干”后残留在衣服上的洗涤剂质量的质量分数为:100g×1%÷2000g=0.05%,因此,残留在衣服上的洗涤剂的质量为:0.05%×100g=1/20 g。
例3.在t ℃时,将 10 g某纯净物完全溶解在90 g水中,你认为所得溶液中溶质的质量分数可能出现哪些情况?试举例说明。
解析 :解答此题,既要掌握溶质质量分数的计算公式,又要熟悉物质溶于水的三种情况:①物质溶解于水后,溶质本身没变,像氯化钠、硝酸钠等,溶质的质量为 10 g,溶质的质量分数: ×100%=10%。
×100%=10%。
②物质溶于水时,与部分水发生化合反应,溶质不再是加入的物质,而是化合后生成的新物质,这时其质量肯定大于 10 g,因此所得溶液中溶质的质量分数也一定大于 10%。如三氧化硫溶于水就是这种情况。
③结晶水合物溶于水时,结晶水转化为溶剂水,这样一来,溶液中溶质的质量小于 10 g,而溶剂质量却大于90 g,因此,溶质的质量分数必定小于 10%。如兰矾(CuSO4·5H2O)溶于水就是这种情况。
例4.配制10%的氯化钠溶液时,不会引起溶液中氯化钠的质量分数偏小的是( )
A.用量筒量取水时仰视读数
B.配制溶液的烧杯用少量蒸馏水润洗
C.氯化钠晶体不纯
D.转移已配好的溶液时,有少量溶液溅出
解析:配制一定溶质质量分数的溶液是一个定量实验,所用试剂不当或操作错误都会给实验结果带来一定的影响。影响的结果如何,我们是可以通过溶质质量分数的计算公式来作出判断的。对于A,这样量取的水的体积要比理论上的体积大一些,其质量也相应变大,因此配得的溶液中氯化钠的质量分数将偏小;对于B,此时相当于所用水的质量增大了,会引起溶液中氯化钠的质量分数偏小;当氯化钠晶体不纯时,相当于溶质的质量减小,这样就会引起溶液中氯化钠的质量分数偏小;在将溶液配制完成之后,即便有少量溶液溅出,但不会影响其中氯化钠的质量分数。
答案:D。
[常见误区]
1.认为只要加入溶质就能使溶液中溶质的质量分数变大。仔细想一想,如果溶液本来就是某一定温度下的饱和溶液,再加入溶质后还能继续溶解吗?此时溶质的质量分数还会变大吗?答案是显而易见的。
2.在计算加入溶质所得溶液的质量分数时,只看到溶质质量的增加,未想到溶液的质量也同样增加,从而导致计算结果的错误。
3.不能全面考虑物质溶于水时所发生的变化,认为加入水中的物质都是溶质,生搬硬套公式进行计算。如例3。
4.分析配制一定溶质质量分数的溶液所可能造成的误差时,找不准正确的判断依据,只凭主观想像加以判断。如例4。
[基础演练]
1.对于溶液的有关叙述,正确的是( )
A.在两种溶液中,含溶质较多的,其溶质的质量分数就大
B.在一定量的溶液中,再加入一些溶剂后,其溶质的质量分数就变小
C.将50℃时的硝酸钾的饱和溶液降温,有可能变成不饱和溶液
D.一切溶液中的溶剂都是水
9.一木块漂浮于50g的KNO3饱和溶液中(见下图A),当温度改变时(不考虑由此引起的木块和溶液体积的变化),木块排开液体的体积(V排)随时间(t)发生了变化(如图B所示)。
由此推测出温度的改变是(填:“升温”或“降温”) 。
同时观察到烧杯底部KNO3晶体(填“增多”或“减少”) 。

课题3 溶质的质量分数
[考点透视]
8.大多数固体物质的溶解度随着温度的升高而__________;少数固体物质的溶解度受温度的影响很小,如_____________;极少数固体物质的溶解度随着温度的升高而____________,如_____________。
7.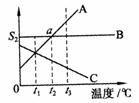 右图是A、B、C三种物质的溶解度曲 线,根据该图回答:
右图是A、B、C三种物质的溶解度曲 线,根据该图回答:
①t3℃时A、B、C三种物质的溶解度, 由高到低的顺序是 。
②随温度升高溶解度降低的是 。
③等质量的三种物质的饱和溶液均由t3℃降到t1℃时,析出溶质的质量最大的是 ,变成不饱和溶液的是 。
④a点表示的含义是 。
⑤当A、B、C三物质的溶液都接近饱和时,采用增加溶质、蒸发溶剂、升高温度的方法,可以达到饱和的是 物质的溶液。
6.20℃时,向100g水中不断加入KNO3固体,充分搅拌后过滤,称量所得溶液的质量,如下表所示。试分析下列四组溶液哪些是饱和溶液?哪些是不饱和溶液?
|
选项 |
A |
B |
C |
D |
|
加入KNO3质量(g) |
5 g |
15 g |
31.6 g |
35 g |
|
所得溶液质量(g) |
105 g |
115 g |
131.6 g |
131.6 g |
5.20℃时,下列四种物质分别溶解在水里恰好制成饱和溶液。其中易溶物质是( )
A.1g物质溶解在100g水里 B.15g物质溶解在1000g水里
C.20g物质溶解在150g水里 D.100g水里溶解0.5g物质
4.常温下,向一未知质量分数的硝酸钾溶液中加入少量硝酸钾晶体,经充分搅拌,发现有部分硝酸钾晶体溶解。原溶液是( )
A.饱和溶液 B.不饱和溶液
C.各部分性质不相同的液体 D.无法确定
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com