
17.⑴ N;Si;S;Ca ⑵ K;F;Ar
⑶ HClO4;KOH;Al(OH)3 ; 3HClO4 + Al(OH)3 = Al(ClO4)3 + 3H2O
HClO4 + KOH = KClO4 + H2O ; KOH + Al(OH)3 = KAlO2 + 2H2O ⑷.K;F
⑸.方案一:用Mg条和Al片分别和同浓度的盐酸反应反应,观察其反应速率的快慢。
方案二:分别向AlCl3溶液、MgCl2溶液中加入NaOH溶液,观察其沉淀及其溶解情况。
(或其他合理答案)
⑹.氯 H2S + Cl2 = 2HCl + S↓
16.⑴ Li2O Li3N
⑵ Be(OH)2 Be(OH)2 + 2OH- = BeO2- 2 + 2H2O Be(OH)2 + 2H+ = Be2+ + 2H2O
⑶ Al4C3 + 4OH- + 4H2O = 4AlO- 2 + 3CH4↑
⑷ 加热至熔融状态,测量其导电性。
6、BC 7、D 8、D 9、B 10、CD 11、AC 12、B 13、D 14、AD 15、BC
1、B 2、B 3、A 4、D 5、B
20.(A)
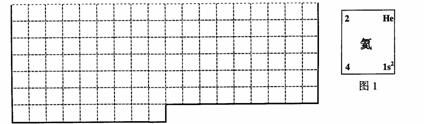
 ⑴.上表中的实线是元素周期表部分边界,请在表中用实线补全元素周期表边界。
⑴.上表中的实线是元素周期表部分边界,请在表中用实线补全元素周期表边界。
⑵.元素甲是第三周期ⅥA族元素,请在右边方框中按氦元素(图1)的式样,写出元素甲的原子序数、元素符号、元素名称、相对原子质量和最外电子层排布。
⑶.元素乙的3p亚层中只有1个电子,则乙原子半径与甲原子半径比较:________>________。
甲、乙的最高价氧化物水化物的酸性强弱为:________>________(用化学式表示)。
⑷.元素周期表体现了元素周期律,元素周期律的本质是原子核外电子排布的__________,请写出元素在元素周期表中的位置与元素原子结构的关系:____________________________________________________。
19.不同元素的气态原子失去最外层一个电子所需要的能量(设其为E)如右图所示。试根据元素在周期表中的位置,分析图中吗线的变化特点,并回答下列问题。
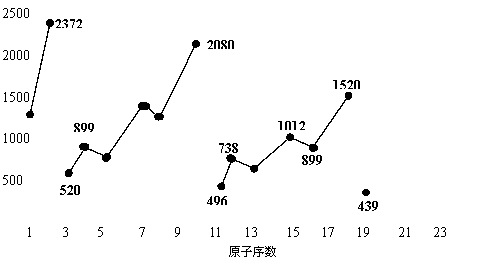
⑴.同主族内不同元素的E值变化的特点是:__________________________。各主族中E值的这种变化特点体现了元素性质的__________变化规律。
⑵.同周期内,随原子序数增大,E值增大。但个别元素的E值出现反常。现试预测下列关系式中正确的是______(填写编号,多选倒扣)
① E(砷)>E(硒) ② E(砷)<E(硒)
③ E(溴)>E(硒) ④ E(溴)<E(硒)
⑶.估计1mol气态Ca原子失去最外层一个电子所需能量E值的范围:________< E <__________。
⑷.10号元素E值较大的原因是___________________。
18. X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:① 元素周期表中,Z与Y相邻,Z与W也相邻; ② Y、Z和W三种元素的原子最外层电子数之和为17。 请填空:
⑴.Y、Z和W三种元素是否位于同一周期(填“是”或“否”) ,理由是
。
⑵.Y是 、Z是 、W是 (填元素符号)。
⑶.X、Y、Z和W可组成一种化合物,其原子个数之比为8:2:4:1。写出该化合物的名称及化学式 。
17.下表是元素周期表的一部分,回答下列有关问题:
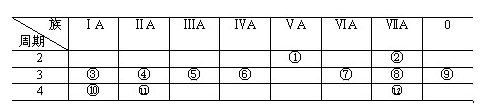
⑴.写出下列元素符号:①
,⑥ ,⑦ , 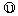 。
。
⑵.在这些元素中,最活泼的金属元素是 ,最活泼的非金属元素是 ,最不活泼的元素是 (用元素符号做答)。
⑶.在这些元素的最高价氧化物对应水化物中,酸性最强的是(填化学式) ,碱性最强的是 ,呈两性的氢氧化物是 ,写出三者之间相互反应的化学方程式:
; ;
。
⑷.在这些元素中,原子半径最小的是(填元素符号) ,原子半径最大的是 。
⑸.在⑤与④中,化学性质较活泼的是(填元素名称) ,设计两个原理不同的简单实验(只要写出实验方案即可),用化学实验证明。
方案一: ;
方案二: 。
⑹.在⑧与 ⑦ 中,化学性质较活泼的是 ,写出可以验证该结论的一个离子反应方程式 。
16.在元素周期表中,同一主族元素化学性质相似。目前也发现有些元素的化学性质和它在周期表中左上方或右下方的另一主族的元素性质相似,称为对角线规则。据此回答:
⑴.锂在空气中燃烧,除生成 外,也生成微量的 (用化学式做答)。
⑵.铍的最高价氧化物对应的水化物的化学式是 ,它属于两性氧化物,可以证明这一结论的离子方程式是 ; 。
⑶.已知反应 Be2C + 4H2O = 2Be(OH)2 + CH4↑,则Al4C3遇足量强碱溶液反应的离子方程式为 。
⑷.科学家证实,BeCl2属于共价化合物,设计一个简单实验证明这一点,你想到的可行的方法是 。
15.第IIA族元素R的单质及其相应氧化物的混合物12g,加足量水经完全反应后蒸干,得固体16g,试推测该元素可能为
A.Mg B.Ca C.Sr D.Ba
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com