
13.(09海南卷 13)(9分)
13)(9分)
 有关物质存在如图所示的转化关系(部分产物已省略)。通常C为气体单质,G为紫黑色固体单质。实验室中,常用固体E在B的催化下加热制取气体单质H。
有关物质存在如图所示的转化关系(部分产物已省略)。通常C为气体单质,G为紫黑色固体单质。实验室中,常用固体E在B的催化下加热制取气体单质H。




 请回答下列问题:
请回答下列问题:
 (1)反应①的化学方程式为
(1)反应①的化学方程式为
 (2)反应②的离子方程式为
(2)反应②的离子方程式为
 (3)写出另外一种实验室制取H的化学方程式
(3)写出另外一种实验室制取H的化学方程式
 (4)D溶液与Pb(NO3)2溶液混合可形成沉淀,此沉淀的Ksp=7.0×10-9。将等体积的D溶液与Pb(NO3)2溶液混合,若D的浓度为1×10-2mo1/L ,则生成沉淀所需Pb(NO3)2溶液的最小浓度为
。
(4)D溶液与Pb(NO3)2溶液混合可形成沉淀,此沉淀的Ksp=7.0×10-9。将等体积的D溶液与Pb(NO3)2溶液混合,若D的浓度为1×10-2mo1/L ,则生成沉淀所需Pb(NO3)2溶液的最小浓度为
。
答案:
 (1)
(1) (2分)
(2分)
 (2)
(2) (2分)
(2分)
 (3)
(3)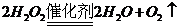 或
或 (其他合理答案也给分)(2分)
(其他合理答案也给分)(2分)
 (4)
(4) (3分)
(3分)
12.(09重庆卷26)(14分)工业上电解饱和食盐能制取多种化工原料,其中部分原料可用于制备多晶硅。
(1)题26图是离子交换膜法电解饱和食盐水示意图,电解槽阳极产生的气体是 ;NaOH溶液的出口为 (填字母);精制饱和食盐水的进口为 (填字母);干燥塔中应使用的液体是 。
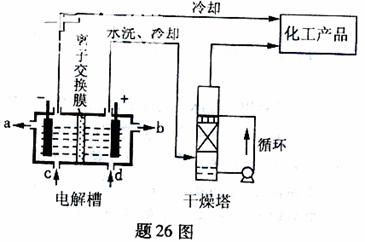
(2)多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4的综合利用收到广泛关注。
①SiCl4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl4与H2和O2反应,产物有两种,化学方程式为 。
②SiCl4可转化为SiHCl3而循环使用。一定条件下,在20L恒容密闭容器中的反应:
3 SiCl4(g)+2H2(g)+Si(s) 4SiHCl3(g)
4SiHCl3(g)
达平衡后,H2与SiHCl3物质的量浓度分别为0.140mol/L和0.020mol/L,若H2全部来源于离子交换膜法的电解产物,理论上需消耗纯NaCl的质量为 kg。
(3)采用无膜电解槽电解饱和食盐水,可制取氯酸钠,同时生成氢气,现制得氯酸钠213.0kg,则生成氢气
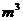 (标准状况)。
(标准状况)。
答案:
(1)①氯气;a;d;浓硫酸
(2)①SiCl4+2H2+O2 SiO2+4HCl②0.35
SiO2+4HCl②0.35
(3)134.4
解析:
(1)电解饱和食盐时阳极阴离子Cl-、OH-放电,Cl-的放电能力强于OH-,阳极发生的方程式为:2Cl--2e-===Cl2↑;阴极:2H++2e-===H2↑;总反应为:2NaCl+2H2O Cl2↑+H2↑+2NaOH。H2、2NaOH在阴极,NaOH溶液的出口为a,Cl2在阳极,精制饱和食盐水从阳极进入,选d;要干燥Cl2需要用酸性干燥剂H2SO4或P2O5等,中性干燥剂无水CaCl2。
Cl2↑+H2↑+2NaOH。H2、2NaOH在阴极,NaOH溶液的出口为a,Cl2在阳极,精制饱和食盐水从阳极进入,选d;要干燥Cl2需要用酸性干燥剂H2SO4或P2O5等,中性干燥剂无水CaCl2。
(2)①SiCl4与H2和O2反应,产物有两种,光导纤维的主要成分是SiO2,H、Cl元素必在另一产物中,H、Cl元素结合成HCl,然后配平即可。发生的化学方程式为:SiCl4+2H2+O2 SiO2+4HCl。
SiO2+4HCl。
②
由3 SiCl4(g)+2H2(g)+Si(s) 4SiHCl3(g)
4SiHCl3(g)
起始量(mol) n 0
变化量(mol) 3x 2x x 4x
平衡量(mol) n-2x 4x
4x=0.020mol/L×20L=0.4mol,n-2x=0.140mol/L20L=2.8mol,n=3.0mol,由2NaCl+2H2O Cl2↑+H2↑+2NaOH,(2×58.5)g:1mol=m(NaCl)g:3mol;m(NaCl)=351g=0.351kg。
Cl2↑+H2↑+2NaOH,(2×58.5)g:1mol=m(NaCl)g:3mol;m(NaCl)=351g=0.351kg。
(3)由NaCl转化为NaClO3,失去电子数为6,H2O转化为H2,得到的电子数为2,设产生的H2体积为V,由得失电子守恒有:
6× ;V=134.4m3。
;V=134.4m3。
11.(09浙江卷 26)(14分)各物质之间的转换关系如下图,部分生成物省略。C、D是由X、Y、Z中两种元素组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子量外层电子数之和为10。D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,l有漂白作用,反应①常用于制作印刷电路板。
26)(14分)各物质之间的转换关系如下图,部分生成物省略。C、D是由X、Y、Z中两种元素组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子量外层电子数之和为10。D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,l有漂白作用,反应①常用于制作印刷电路板。



 请回答下列问题:
请回答下列问题:
 (1)写出A的化学式
, C的电子式
。
(1)写出A的化学式
, C的电子式
。
 (2)比较Y与Z的原子半径大小
> (填写元素符号)。
(2)比较Y与Z的原子半径大小
> (填写元素符号)。
 (3)写出反应②的化学方程式(有机物用结构简式表示)
,举出该反应的一个应用实例
。
(3)写出反应②的化学方程式(有机物用结构简式表示)
,举出该反应的一个应用实例
。
 (4)已知F溶于稀硝酸,溶液变成蓝色,并放出无色气体。请写出该反应的化学方程式
。
(4)已知F溶于稀硝酸,溶液变成蓝色,并放出无色气体。请写出该反应的化学方程式
。
 (5)研究表明:气体D在一定条件下可被还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出N及其2种同素异形体的名称 、 、 。
(5)研究表明:气体D在一定条件下可被还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出N及其2种同素异形体的名称 、 、 。
 答案:
答案:
(1)Cu2(OH)2CO3
[Cu(OH)2·CuCO3]或CuCO3 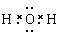
 (2) C>O
(2) C>O
 (3)CH2OH(CHOH)4CHO
+ 2Cu(OH)2
(3)CH2OH(CHOH)4CHO
+ 2Cu(OH)2  CH2OH(CHOH)4COOH
+ Cu2O↓+ 2H2O
CH2OH(CHOH)4COOH
+ Cu2O↓+ 2H2O
 医学上可用这个反应检验尿液中的葡萄糖。
医学上可用这个反应检验尿液中的葡萄糖。
 (4)3Cu2O
+ 14HNO3
(4)3Cu2O
+ 14HNO3  6Cu(NO3)2
+ 2NO↑+ 7H2O
6Cu(NO3)2
+ 2NO↑+ 7H2O
 (5)金刚石、石墨、富勒烯(C60)或碳纳米管等。
(5)金刚石、石墨、富勒烯(C60)或碳纳米管等。
解析:
从反应图中寻找突破口,E与葡葡糖生成红色沉淀F,则E应为Cu(OH)2,而B为Cu2+,反应①为印刷电路板,L为棕黄色溶液,由此可推出:M应为Cu,L为FeCl3 。G为黄绿色气体,则为Cl2,K为浅绿色,则为Fe2+溶液。X的原子半径最小,则为H,D为非可燃性气体,可推为CO2,C和O的最外层电子之和刚好为10。C为H、C、O中的两种组成的化合物,且可以与Cl2反应,故应为H2O,生成H为HCl,I为HClO(具有漂白性),HCl与J(Fe)可生成FeCl2溶液。
(1)A + HCl Cu2+ + H2O
+ CO2,由元素守恒可知,A可以CuCO3或碱式碳酸铜均可。
Cu2+ + H2O
+ CO2,由元素守恒可知,A可以CuCO3或碱式碳酸铜均可。
(2)Y为C,Z为N,两者位于同一周期,前者的半径大,即C>N。
(3)葡萄糖含有醛基,可以与Cu(OH)2生成砖红色沉淀。
(4)F为Cu2O,与HNO3反应,生成Cu(NO3)2,且生成无色气体,应为NO,然后根据得失电子守恒配平即可。
(5)CO2可以还原成正四面体结构的晶体N,即化合价降低,显然生成C,应为金刚石。它的同素异形体必须为含碳的单质。
10.(09天津卷 9)(18分)海水是巨大的资源宝库,在海水淡化及综合利用方面,天津市位居全国前列。从海水中提取食盐和溴的过程如下:
9)(18分)海水是巨大的资源宝库,在海水淡化及综合利用方面,天津市位居全国前列。从海水中提取食盐和溴的过程如下:


 (1)请列举海水淡化的两种方法: 、 。
(1)请列举海水淡化的两种方法: 、 。
 (2)将NaCl溶液进行电解,在电解槽中可直接得到的产品有H2、 、 、或H2、 。
(2)将NaCl溶液进行电解,在电解槽中可直接得到的产品有H2、 、 、或H2、 。
 (3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br,其目的为 。
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br,其目的为 。
 (4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为 ,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是 。
(4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为 ,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是 。
 (5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,了如下装置简图:
(5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,了如下装置简图:


 请你参与分析讨论:
请你参与分析讨论:
 ①图中仪器B的名称: 。
①图中仪器B的名称: 。
 ②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是 。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是 。
 ③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件: 。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件: 。
 ④C中液体产生颜色为 。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是
。
④C中液体产生颜色为 。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是
。
答案:

解析
本题考查海水中提取溴的实验。电解NaCl溶液的方程式为:2NaCl + 2H2O
 2NaOH
+ H2↑+ Cl2↑,其中Cl2有可能与NaOH会生成NaClO。步骤I中的Br2的浓度很小,多次用SO2反复吸收,最终用Cl2处理,则可获得大量的工业溴。溴具有强氧化性可以氧化SO2,生成H2SO4,因此要注意酸对设备的腐蚀问题。溴具有腐蚀性,可以腐蚀橡胶。蒸馏的目的,就是通过沸点不同而提纯Br2,所以要通过温度计控制好Br2沸腾的温度,尽可能使Br2纯净。
2NaOH
+ H2↑+ Cl2↑,其中Cl2有可能与NaOH会生成NaClO。步骤I中的Br2的浓度很小,多次用SO2反复吸收,最终用Cl2处理,则可获得大量的工业溴。溴具有强氧化性可以氧化SO2,生成H2SO4,因此要注意酸对设备的腐蚀问题。溴具有腐蚀性,可以腐蚀橡胶。蒸馏的目的,就是通过沸点不同而提纯Br2,所以要通过温度计控制好Br2沸腾的温度,尽可能使Br2纯净。
9. (09上海理综14)生活中难免会遇到一些突发事件,我们要善于利用学过的知识,采取科学、有效的方法保护自己。如果发生了氯气泄漏,以下自救方法得当的是
A.只要在室内放一盆水
B.向地势低的地方撤离
C.观察风向,顺风撤离
D.用湿毛巾或蘸有石碱水的毛巾捂住口鼻撤离
答案:D
8.(09上海卷 19)已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下(
19)已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下( 、
、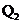 均为正值):
均为正值):


 有关上述反应的叙述正确的是
有关上述反应的叙述正确的是
 A.
A.
 B.生成物总能量均高于反应物总能量
B.生成物总能量均高于反应物总能量
 C.生成1molHCl气体时放出
C.生成1molHCl气体时放出 热量
热量
 D.1mol HBr(g)具有的能量大于1mol HBr(1)具有的能量
D.1mol HBr(g)具有的能量大于1mol HBr(1)具有的能量
答案:AD
7.(09北京卷9)已知 有相同容积的定容密封容器甲和乙,甲中加入
有相同容积的定容密封容器甲和乙,甲中加入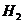 和
和 各0.1mol ,乙中加入HI 0.2mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是
各0.1mol ,乙中加入HI 0.2mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是
A.甲、乙提高相同温度 B 甲中加入0.1mol He,乙不改变
C.甲降低温度,乙不变 D 甲增加0.1mol  ,乙增加0.1mol
,乙增加0.1mol 
答案:C
6.(09广东化学 12) 下列离子方程式正确的是
12) 下列离子方程式正确的是
 A. 向盐酸中滴加氨水:H+ + OH- = H2O
A. 向盐酸中滴加氨水:H+ + OH- = H2O
 B. Fe(OH)3溶于氢碘酸:Fe(OH)3
+ 3H+ = Fe3+ + 3H2O
B. Fe(OH)3溶于氢碘酸:Fe(OH)3
+ 3H+ = Fe3+ + 3H2O
 C. 铜溶于稀硝酸:3Cu + 8H+
+ 2NO3- = 3Cu2+ + 2 NO ↑+ 4H2O
C. 铜溶于稀硝酸:3Cu + 8H+
+ 2NO3- = 3Cu2+ + 2 NO ↑+ 4H2O
 D. 向Na2S2O3溶液中通入足量氯气:S2O32-+2Cl2+3H2O=2SO32-+4Cl-+6H+
D. 向Na2S2O3溶液中通入足量氯气:S2O32-+2Cl2+3H2O=2SO32-+4Cl-+6H+
 答案:C
答案:C
 解析:
解析:
A项中的氨水应写成分子式,
B项发生的是氧化还原反应;
C项正确;
氯气具有强氧化性将S2O32-氧化成SO42-,正确的离子方程式应为S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+,故D错。
5. (09广东化学 9)下列浓度关系正确的是
9)下列浓度关系正确的是
 A. 氯水中:c(Cl2)=2[c(
A. 氯水中:c(Cl2)=2[c( )+c(
)+c( )+C(HClO)]
)+C(HClO)]
 B. 氯水中:c(
B. 氯水中:c( )>c(
)>c( )>c(
)>c(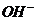 )>c(
)>c( )
)
 C. 等体积等浓度的氢氧化钠与醋酸混合:c(
C. 等体积等浓度的氢氧化钠与醋酸混合:c( )=c(
)=c(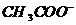 )
)
 D.
D.  溶液中:c
溶液中:c
 答案:D
答案:D
 解析:
解析:
根据氯水中所含粒子的种类可知氯水中也含有氯气分子A设置了一个貌似物料守恒的式子而忽视了氯气分子的存在,故A错;
根据Cl2+H2O HClO+H++Cl-,HCl完全电离 而HClO部分电离,可知正确的顺序c(H+)>c(Cl-)>c(ClO-)>c(OH-),B错;
HClO+H++Cl-,HCl完全电离 而HClO部分电离,可知正确的顺序c(H+)>c(Cl-)>c(ClO-)>c(OH-),B错;
C项等物资的量的强碱与弱酸混合生成强碱弱酸盐溶液显碱性c(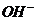 )>c(
)>c( ),再根据溶液中电荷守恒可以判断c(
),再根据溶液中电荷守恒可以判断c( )>c(
)>c(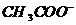 ;
;
D项比较简单
4.(09江苏卷 14)I2在KI溶液中存在下列平衡:
14)I2在KI溶液中存在下列平衡:




 某I2、、KI混合溶液中,
某I2、、KI混合溶液中, 的物质的量浓度c(
的物质的量浓度c( )与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是
)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是


A. 反应
反应

 的△H>0
的△H>0
 B.若温度为
B.若温度为 ,反应的平衡常数分别为
,反应的平衡常数分别为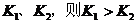
 C.若反应进行到状态D时,一定有
C.若反应进行到状态D时,一定有
 D.状态A与状态B相比,状态A的c(I2)大
D.状态A与状态B相比,状态A的c(I2)大
答案:BC
解析:
随着温度的不断升高, 的浓度逐渐的减小,说明反应向逆方向移动,也就意味着该反应是放热反应,所以
的浓度逐渐的减小,说明反应向逆方向移动,也就意味着该反应是放热反应,所以 ,所以A项错;
,所以A项错;
因为 ,
, ,所以当温度升高时,反应向逆方向移动,即
,所以当温度升高时,反应向逆方向移动,即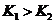 ;C项,从图中可以看出D点并没有达到平衡状态,所以它要向A点移动,这时
;C项,从图中可以看出D点并没有达到平衡状态,所以它要向A点移动,这时 的浓度在增加,所以
的浓度在增加,所以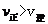 ,C项正确;
,C项正确;
D项,从状态A到状态B, 的浓度在减小,那么
的浓度在减小,那么 的浓度就在增加。
的浓度就在增加。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com