
6.苯(溴)[或溴苯(溴)]
错例:加碘化钾溶液。
错因:溴和碘化钾生成的单质碘又会溶于苯。
正解:加氢氧化钠溶液充分振荡,使溴转化为易溶于水的盐,分液。
5.苯(甲苯)[或苯(乙苯)]
错例:加酸性高锰酸钾溶液,将甲苯氧化为苯甲酸后,分液。
错因:苯甲酸微溶于水易溶于苯。
正解:加酸性高锰酸钾溶液后,再加氢氧化钠溶液充分振荡,将甲苯转化为易溶于水的苯甲酸钠,分液。
4.溴乙烷(乙醇)
错例:蒸馏。
错因:溴乙烷和乙醇都易挥发,能形成恒沸混合物。
正解:加适量蒸馏水振荡,使乙醇溶于水层后,分液。
3.乙醇(乙酸)
错例A:蒸馏。(乙醇沸点78.5℃,乙酸沸点117.9℃)。
错因:乙醇、乙酸均易挥发,且能形成恒沸混合物。
错例B:加入碳酸钠溶液,使乙酸转化为乙酸钠后,蒸馏。
错因:乙醇和水能形成恒沸混合物。
正解:加入适量生石灰,使乙酸转化为乙酸钙后,蒸馏分离出乙醇。
2.乙醇(水)
错例A:蒸馏,收集78℃℃时的馏分。
错因:在78℃时,一定浓度(95.57%)的乙醇和水会发生“共沸”现象,即以恒定组成共同气化,少量水无法被蒸馏除去。
错例B:加生石灰,过滤。
错因:生石灰和水生成的氢氧化钙能溶于乙醇,使过滤所得的乙醇混有新的杂质。
正解:加生石灰,蒸馏。(这样可得到99.8%的无水酒精)。
依据有机物的水溶性、互溶性以及酸碱性等,可选择不同的分离方法达到分离、提纯的目的。在进行分离操作时,通常根据有机物的沸点不同进行蒸馏或分馏;根据物质的溶解性不同,采取萃取、结晶或过滤的方法。有时也可以用水洗、酸洗或碱洗的方法进行提纯操作。
下面就有机物提纯中常见的错误操作进行分析。(括号中物质为杂质)
1.乙烷(乙烯)
错例A:通入氢气,使乙烯反应生成乙烷。
错因:①无法确定加入氢气的量;②反应需要加热,并用镍催化,不符合“操作简单”原则。
错例B:通入酸性高锰酸钾溶液,使乙烯被氧化而除去。
错因:乙烯被酸性高锰酸钾溶液氧化可生成二氧化碳气体,导致新的气体杂质混入。
正解:将混合气体通入溴水洗气,使乙烯转化成1,2-二溴乙烷液体留在洗气瓶中而除去。
13. 常见有机化学物质的俗名
|
化学名称 |
俗名 |
化学名称 |
俗名 |
|
乙炔 |
电石气 |
CaC2 |
电石 |
|
2-甲基-1,3-丁二烯 |
异戊二烯 |
三硝基甲苯 |
TNT |
|
CHCl3 |
氯仿 |
乙酸 |
醋酸 |
|
酚醛树脂 |
电木 |
苯甲酸 |
安息香酸 |
|
丙三醇 |
甘油 |
乙醇 |
酒精 |
|
甲醛 |
蚁醛 |
甲醇 |
木精 |
|
苯酚 |
石炭酸 |
乙二酸 |
草酸 |
|
甲酸 |
蚁酸 |
|
|
4. 课本中出现的性质检验的实验的注意事项
|
检验物质 |
检验方法 |
|
烯烃、炔烃 |
Br2、KMnO4(H+) |
|
醛基 |
银铵溶液、Cu(OH)2 |
|
酚 |
溴水(白色沉淀)、FeCl3(紫色) |
|
葡萄糖 |
银铵溶液、Cu(OH)2 |
|
蔗糖、淀粉、纤维素 |
加硫酸水解,加氢氧化钠中和酸,然后用银铵溶液或Cu(OH)2 |
|
麦芽糖 |
银铵溶液、Cu(OH)2 |
|
蛋白质 |
浓硝酸(变黄)、灼烧(烧焦羽毛味) |
|
卤代烃 |
在氢氧化钠的水溶液加热,用硝酸酸化,加入硝酸银 |
|
淀粉 |
碘水 |
(1)水中的溶解性
①不溶于水的有:
大部分烃、卤代烃、含C12个以上的醇、酯、硝基苯、溴苯、TNT、三溴苯酚、酯、高级脂肪酸、纤维素等;
②微溶于水的:乙炔、苯甲酸等。
③溶于水的有:C原子数≤11的醇,低级醛、醚、酸,有机钠盐,葡萄糖,蔗糖,麦芽糖等
④苯酚溶解的特殊性:常温时苯酚在水中溶解度不大,当高于65℃时能跟水以任意比互溶。
3. 常见物质的制备(乙烯、乙炔、溴苯、硝基苯、乙酸乙酯、酚醛树脂)原理、仪器、除杂、收集以及注意事项。
|
物质 |
仪器 |
除杂及收集 |
注意事项 |
|
乙烯 |
 |
可能含有杂质气体(CO2、SO2)可用NaOH溶液除去。 |
1、沸石(暴沸) 2、温度计位置 3、升高温度要快 4、控制温度 5、浓硫酸作用(催化剂、脱水剂) 6、乙醇与浓硫酸体积比为1:3 |
|
乙炔 |
 |
可能会含有H2S等杂质气体,可用硫酸铜溶液(氢氧化钠溶液)除去。 |
1、水可用饱和NaCl 2、不能用启谱发生器 3、该反应为放热反应 |
|
溴苯 |
 |
溴、FeBr3等,用氢氧化钠溶液处理后分液、然后蒸馏。 |
1、催化剂(FeBr3) 2、长导管的作用冷凝回流、导气 3、右侧导管不能伸入溶液中 4、右侧锥形瓶有白色烟雾 |
|
硝基苯 |
 |
可能含有未反应完的苯、硝酸、硫酸,用氢氧化钠溶液中和酸,分液,然后用蒸馏的方法除去苯。 |
1、导管1的作用冷凝 2、仪器2为温度计 3、用水浴控制温度为50~60°C 4、浓硫酸的作用催化剂和脱水剂 |
|
乙酸乙酯 |
 |
|
1、浓硫酸的作用催化剂和脱水剂 2、左边导管导气冷凝 3、饱和碳酸钠吸收乙醇、乙酸,降低乙酸乙酯的溶解度 4、右边导管不能接触试管中的液面 |
|
酚醛树脂 |
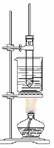 |
|
1、试管上的长导管作用冷凝回流 2、用沸水浴进行加热 3、残留物可用酒精洗 |
2. 有机化合物官能团的引入
(C-C、C=C、-X(卤素原子)、-OH、-CHO或羰基、-COOH、-COOR、高分子化合物、-NO2)
|
官能团 |
引入方法 |
|
C-C |
C=C、C≡C的加成 |
|
C=C |
卤代烃和醇消去、C≡C按1:1加成 |
|
-X |
C=C、C≡C加成、醇与HX取代、烷烃取代、苯环取代 |
|
-OH |
卤代烃水解、醛(酮)加成、酯水解、C=C加成、葡萄糖分解 |
|
-CHO |
醇氧化、乙烯催化氧化、 |
|
-COOH |
醛氧化、酯水解(酸性)、蛋白质水解 |
|
-COOR |
醇与羧酸酯化 |
|
高分子化合物 |
C=C、C≡C加聚、氨基酸脱水、缩聚反应、 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com